Para evitar confusiones, le informamos de que ESTE NO ES el formulario para enviar PREGUNTAS SOBRE VACUNAS al comité. Si esa fuera su intención, diríjase a la sección de preguntas de profesionales o de preguntas de familias.
A través de este formulario, el responsable del mismo, la Asociación Española de Pediatría (AEP) y su Comité Asesor de Vacunas, recaba los datos necesarios para gestionar el envío de sus comentarios y sugerencias sobre el Manual de Inmunizaciones en línea de la AEP, que ponemos a su disposición en nuestra página web.
Los campos marcados con asterisco son obligatorios y, sin ellos, no se tramitará su comentario o sugerencia.
Este tratamiento de datos no puede realizarse sin su consentimiento, por lo que deberá validar la casilla de protección de datos antes de enviar la consulta.
Sus datos no serán cedidos a otras entidades, ni transmitidos a otros países. Tiene derecho a acceder, rectificar y suprimir los datos, así como otros derechos, como se explica en la información común a los tratamientos que efectúa la AEP.
Puede consultar la información detallada sobre protección de datos, así como la información común a los tratamientos que efectúa la AEP.
6. Transporte y conservación de las inmunizaciones
Capítulo 6 - Transporte y conservación de las inmunizaciones
- Puntos clave
- Cadena de frío
- Transporte
- Conservación
- Almacenamiento: frigorífico
- Recursos humanos
- Decálogo de la cadena de frío
- Mantenimiento de la cadena del frío para inmunizaciones adquiridas en farmacias comunitarias
- Bibliografía
- Enlaces de interés
- Historial de actualizaciones
- Tablas y figuras incluidas en el capítulo:
Tabla 6.1. Termoestabilidad de las inmunizaciones comercializadas en España
Tabla 6.2. Lista de errores más frecuentes en el almacenamiento, manipulación y conservación de las inmunizaciones (en PDF)
Tabla 6.3. Decálogo de la cadena del frío
Figura 6.1. Gráfica de temperaturas máximas y mínimas
Figura 6.2. Hoja de registro de temperaturas máximas y mínimas
Sugerencia para la citación: Comité Asesor de Vacunas e Inmunizaciones (CAV-AEP). Transporte y conservación de las inmunizaciones. Manual de inmunizaciones en línea de la AEP [Internet]. Madrid: AEP; may/2025. [consultado el dd/mmm/aaaa]. Disponible en: http://vacunasaep.org/documentos/manual/cap-6
1. Puntos clave
- El mantenimiento de la cadena de frío en todo el proceso de transporte, conservación, manipulación y almacenamiento es fundamental para asegurar el éxito de la inmunización.
- La pérdida de la capacidad inmunizante es acumulativa, irreversible y se incrementa con el tiempo de exposición.
- La temperatura ideal de conservación de las inmunizaciones existentes en España debe estar entre +2 °C y +8 °C.
- Ante la sospecha de la rotura de la cadena de frío, en cualquiera de sus eslabones, se deberá comunicar de forma inmediata a los responsables del área o distrito sanitario y dichas inmunizaciones quedarán inmovilizadas hasta que se determine su idoneidad.
- Los controladores de temperatura tienen la propiedad de comprobar el funcionamiento correcto de las cadenas fija y móvil.
- El frigorífico debe permanecer conectado directamente a la red general, señalizado como de uso exclusivo para inmunizaciones, debe disponer de un termostato y de un sistema de alarma.
- Se deben usar termómetros digitales para la medición de las temperaturas máximas y mínimas.
- La lectura de la temperatura del frigorífico debe realizarse dos veces al día y anotarse posteriormente en sus gráficas o documentos correspondientes.
- Para mantener la temperatura interior del frigorífico se colocarán acumuladores de frío en el congelador, si lo hay, y botellas de agua o de suero fisiológico en la parte inferior y en la puerta.
- Se procederá a la limpieza del frigorífico cuando se produzca en el congelador una capa de escarcha de hielo mayor de 0,5 cm.
- Almacenar las inmunizaciones más sensibles al calor (termolábiles) en la zona más fría (inmunizaciones atenuadas) y en la zona menos fría, aquellas que pierden su actividad a temperaturas inferiores a 0 °C (inmunizaciones inactivadas sobre todo las adsorbidas).
- Las inmunizaciones se almacenarán, según su frecuencia de uso y su fecha de caducidad.
- El eje principal del proceso de la cadena de frío son los profesionales sanitarios y no sanitarios que intervienen en toda la red de frío.
- Es obligatorio que en todo centro de inmunización haya un responsable-coordinador de todo este proceso, que además debe contar con la ayuda de un sustituto con experiencia en el mismo. Todo el personal implicado debe conocer los protocolos de actuación y para evitar errores disponemos de un pdf en este capítulo de obligada lectura.
- Para las inmunizaciones no incluidas en el calendario financiado y adquiridas en las farmacias comunitarias deberá explicarse el mantenimiento correcto de la cadena del frío a los padres (ver sección 8).
2. Cadena de frío
Concepto
Se denomina cadena de frío a un proceso organizado de distribución, transporte, manipulación, conservación y almacenamiento en condiciones óptimas de luz y temperatura, garantizando en todo momento la inmunogenicidad y la eficacia protectora de las inmunizaciones, desde que se produce la salida del laboratorio fabricante hasta el momento de la administración de la inmunización a los pacientes.
En este proceso intervienen la industria farmacéutica, el nivel autonómico, los distritos o áreas sanitarias y los centros de inmunización.
Partes o elementos
- Recursos o equipamientos materiales:
– Cadena móvil: vehículos frigoríficos, cajas isotérmicas, neveras portátiles, portavacunas, acumuladores de frío (ice-packs) y controladores de temperatura.
– Cadena fija: cámaras frigoríficas, congeladores y frigoríficos. Termómetro digital para interior del frigorífico.
- Recursos humanos.
3. Transporte
Forma parte de la cadena móvil de la cadena de frío. Teniendo en cuenta que romper la cadena de frío durante el transporte reduce la efectividad de la inmunización, para evitar esta reducción, son requisitos imprescindibles los siguientes:
- Respetar y hacer cumplir las normas recomendadas por el laboratorio fabricante.
- Se debe realizar en contenedores especiales que garanticen la temperatura estable de conservación durante todo el trayecto.
- Deben quedar registrados en un albarán los siguientes datos: fecha de salida, lugar de destino, tipo de inmunizaciones y presentación, cantidad de dosis, fecha de caducidad y lotes.
Vehículos frigoríficos
Utilizados para el transporte y distribución de grandes suministros de inmunizaciones y entre niveles situados a media y larga distancia.
Cajas o contenedores isotérmicos
El material utilizado es poliestireno expandido o poliuretano. Tienen que ser compactos, sólidos, aislados y herméticos. Mantienen el frío durante el transporte y permiten el almacenamiento en caso de avería eléctrica del frigorífico. Tienen la propiedad de conservar el frío aproximadamente entre 2 y 6 días. Es recomendable que cada centro de inmunización tenga siempre, al menos, una unidad.
Neveras portátiles
Utilizadas para el transporte de pocas unidades y trayectos cortos desde el punto de inmunización hasta otros lugares periféricos como consultorios locales, colegios o domicilios. Usadas también como material de almacenaje de inmunizaciones cuando se produce un corte aislado del suministro eléctrico o una limpieza del frigorífico.
Tienen capacidad de conservación de frío entre 3 y 7 días. Para lograr un buen funcionamiento es recomendable que se abra lo menos posible.
Portavacunas
Reservado para cuando se transportan mínimas cantidades de inmunizaciones y en un trayecto corto, desde el punto de vacunación hasta el lugar de la administración. Su capacidad de enfriamiento oscila entre 12 y 36 horas.
Acumuladores de frío
Utilizados en la cadena móvil en los contenedores isotérmicos, neveras portátiles y portavacunas y en la cadena fija, principalmente, en el frigorífico. Se trata de recipientes de material plástico rígido indeformable, rellenos de un líquido no tóxico como agua, glicoles o gel viscoso. No se deforma una vez congelado. Son reutilizables indefinidamente y en caso de rotura no manchan.
Para un uso correcto y evitar la congelación de las inmunizaciones, no deben entrar en contacto directo con las cajas de los preparados, para ello, se dispondrá la separación entre ambos de cartones rígidos y gruesos, papel arrugado o placas de poliestireno. Mantienen la temperatura adecuada de conservación hasta 24 horas.
Existen en el mercado distintos formatos disponibles entre 200 y 1700 cc. Para inmunizaciones, los que más frecuentemente se usan son los que tienen una capacidad de 400 y 600 cc.
Controladores de temperatura
Su principal característica será comprobar el funcionamiento correcto de las cadenas móvil y fija. Existen diferentes tipos siendo los más utilizados los siguientes:
- Termógrafos
Miden la temperatura de forma continua y automática. Las mediciones quedan registradas en gráficas de papel. Permiten conocer los cambios de temperatura sufridos en el interior del refrigerador.
- Indicadores químicos
- Indicadores de umbral crítico de temperatura: tienen la propiedad de advertir cuando la inmunización ha sido sometida a una temperatura superior de la deseada durante el transporte. Es una etiqueta autoadhesiva que se fija a la vacuna y que cambia de color cuando se produce dicha eventualidad.
- Indicadores de congelación: se utilizan para monitorizar las inmunizaciones que ven sus propiedades alteradas por la congelación durante el almacenamiento y el transporte. Se trata de indicadores de un solo uso o irreversibles, disponibles a dos temperaturas (-4 °C y 0 °C), constando de una ampolla rellena de un líquido azul oscuro pegada a un papel de filtro blanco que se coloca directamente sobre los embalajes de las inmunizaciones. Cuando la ampolla se rompe, tiñe de color azul oscuro el papel de filtro e indica que las inmunizaciones han estado sometidas a temperaturas por debajo de 0.°C.
- Indicadores para acumuladores de frío: de tipo reversible, tienen la función de advertir de la congelación de las inmunizaciones por contacto con el acumulador. Se trata de una etiqueta autoadhesiva que se coloca sobre el acumulador de frío, que debe estar descongelado. El resultante es:
– Apto para el transporte: cuando no existe riesgo de congelación sucede un viraje en la coloración pasando de amarillo a violeta-morado, indica por tanto que el acumulador ha estado expuesto a temperaturas por encima de +4.°C.
– No apto para el transporte: existe riesgo de congelación, se produce un cambio de coloración de violeta-morado a amarillo e indica que el acumulador ha estado sometido a temperaturas por debajo de -4.°C.
Los colores pueden variar de una casa comercial a otra. Este tipo de monitores son utilizados para aquellas inmunizaciones que son muy sensibles a la congelación como tétanos-difteria de carga antigénica reducida (Td), DTPa y sobre todo la hepatitis B, cuyo punto de congelación es -0,5 °C.
- Indicadores de tiempo y temperatura: se trata de un dispositivo fijado a la mercancía y que permite el registro de la temperatura durante el tiempo que dura el transporte. La lectura de estos indicadores debe hacerse en el momento de la recepción, tan pronto se abra el pedido y comprobar que las inmunizaciones se han mantenido de forma correcta durante el transporte. Pueden usarse para controlar cualquier inmunización expuesta a temperaturas, tiempos o ambos fuera del rango aceptable.
La base del funcionamiento es una tira de papel poroso y un reservorio de producto químico pigmentado en color azul; ambos se encuentran separados por una tira reactiva que es necesario que el usuario retire para que entren en contacto directo entre ellos. En un primer momento la tira reactiva es de color blanco, pero a medida que las temperaturas exceden el umbral de respuesta, el producto químico se funde y comienza su recorrido por la tira. La aparición de cualquier coloración azul en la primera ventana del indicador es una estimación del tiempo de exposición por encima de la temperatura umbral (10.°C). En el caso de que esto ocurriera, el fabricante aporta plantillas que facilitan la estimación directa y sencilla de la sobreexposición.
- Termómetros
- Termómetro digital: debe situarse en el exterior del frigorífico, visible y alejado de cualquier fuente de calor.
Consta de un cable con un sensor en su extremo que por su elevada sensibilidad ha de colocarse en la zona central del frigorífico separado de la puerta y de las paredes. Se recomienda sumergir el sensor de temperatura en un líquido (mejor con un punto de congelación más bajo que el agua, como el suero salino o una solución alcohólica), para que los registros de variaciones de temperaturas máximas y mínimas sean "significativos" y que no respondan a cambios térmicos de muy corta duración, que resultan irrelevantes (la más frecuente, la subida instantánea de la temperatura debida a la apertura de la nevera para retirar envases). El sensor sumergido (a falta de un registro continuo) amortigua esos picos y valles de corta duración, en la temperatura del aire interior de la nevera y ofrece, de esta forma, una lectura "tamponada" de qué es lo que pasa realmente con las variaciones de la temperatura en los materiales líquidos y sólidos que están almacenados en el interior del frigorífico, como las inmunizaciones.
Este tipo de termómetro permite conocer una doble lectura de la temperatura del frigorífico, por un lado mide la temperatura actual del exterior e interior y por otro la temperatura máxima y mínima alcanzada desde la última medición.
Existen en el mercado distintos tipos, siendo difícil abarcar el funcionamiento de todos, para ello, es conveniente seguir las instrucciones de uso del fabricante, según el modelo.
El modelo estándar consta de un botón de MAX/MIN y otro RESET/MEM y en la pantalla se visualizan dos términos ingleses: IN, que expresa la temperatura de la consulta donde está ubicado el frigorífico, y OUT, que representa la temperatura obtenida por el sensor ubicado en el interior del frigorífico. Justo al contrario de lo que significan los vocablos ingleses, pues son termómetros diseñados para medir temperaturas en el interior y exterior de edificios.
Interpretación de las medidas:
– Temperatura actual del exterior e interior del frigorífico: la parte superior de la pantalla muestra la temperatura exterior del frigorífico en ese instante y la parte inferior indica la temperatura del interior en ese momento.
– Temperatura máxima y mínima: presionar una vez el botón MAX/MIN, se obtienen las temperaturas máxima y mínima del exterior del frigorífico. Se trata de la temperatura ambiental y en la pantalla aparece el término IN.
Volver a presionar el botón MAX/MIN, se obtienen las temperaturas máxima y mínima del interior del frigorífico. En la pantalla aparece el término OUT.
Al presionar otra vez el botón MAX/MIN, se vuelve a la temperatura actual del frigorífico.
Para borrar la memoria, se pulsa el botón RESET/MEM durante 1-2 segundos, desde la pantalla de MAX/MIN y nunca desde la pantalla inicial.
Es muy importante resetear el termómetro una vez anotadas las mediciones del día.
Ambas mediciones, una vez concluidas, se deben anotar en una gráfica (figura 6.1) o bien en una hoja de control mensual (figura 6.2). Resulta muy útil colocarlas en una zona visible y accesible para todos, como puede ser la puerta o el lateral del frigorífico.
Figura 6.1. Gráfica de temperaturas máximas y mínimas
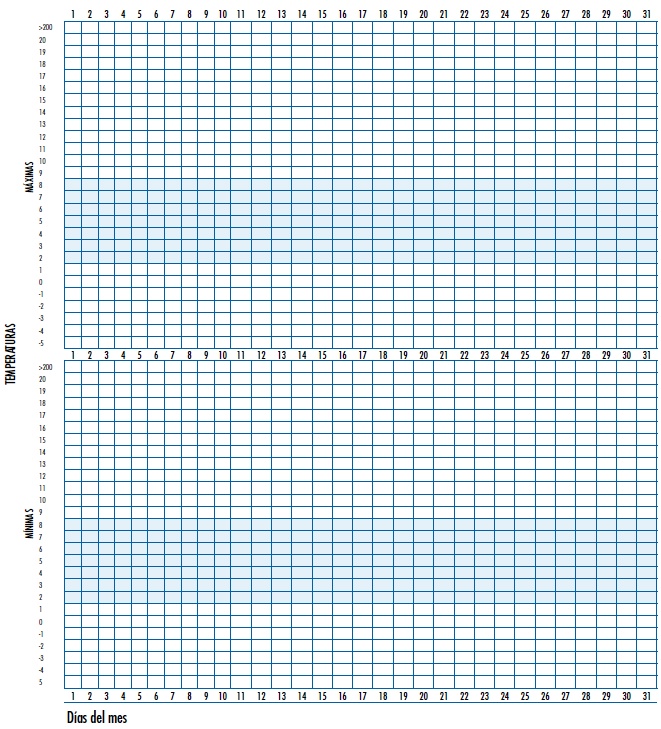
Figura 6.2. Hoja de registro de temperaturas máximas y mínimas
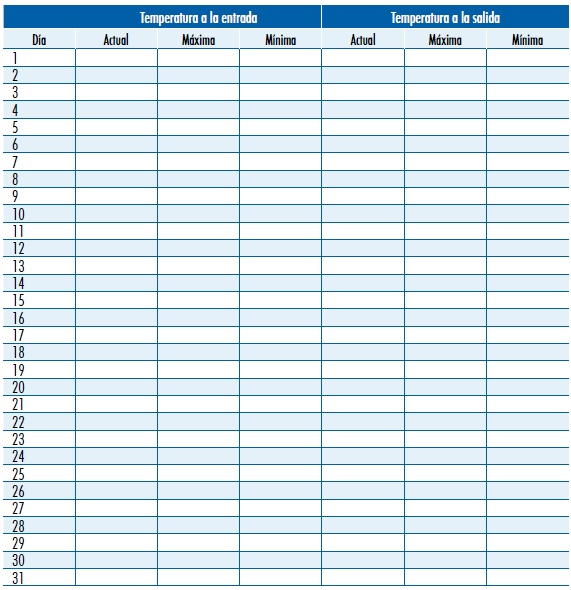
- • Termómetro de mercurio de máxima y mínima: era el más utilizado para monitorizar la temperatura, ya que medía la temperatura actual y la máxima y mínima alcanzadas desde la última lectura o comprobación. Actualmente en desuso ya que por la normativa sobre el mercurio no se fabrican y quedan muy pocos o ninguno.
Formado por un tubo en forma de U, disponía de dos columnas, la de la derecha representaba la temperatura máxima y la de la izquierda la temperatura mínima. La parte inferior del tubo era de mercurio, de color gris-plata y en la parte superior tenía unos fiadores o índices de color azul o rojo.
Cuando se producía un cambio de temperatura, el mercurio empujaba hacia arriba los fiadores produciéndose una separación entre ambas barras, alcanzando la temperatura máxima o mínima. La temperatura máxima venía dada por el extremo inferior del fiador (color azul-rojo) en la columna derecha y la temperatura mínima se medía por el extremo inferior del fiador (color azul-rojo) situada en la columna izquierda. La temperatura actual del frigorífico era la que se visualizaba en el extremo superior de la columna de mercurio, debiendo indicar la misma temperatura tanto en la columna de las máximas como de las mínimas.
Una vez realizada la medición, se procedía a resetear el termómetro hasta la siguiente lectura poniendo los fiadores en contacto con el mercurio mediante un imán.
4. Conservación
Para mantener la estabilidad óptima de las inmunizaciones es necesario que se realicen adecuadamente la conservación y el almacenamiento de las mismas (tabla 6.1).
| Tabla 6.1 (1 de 2). Termoestabilidad de las inmunizaciones comercializadas en España | |||||
| Vacunas/Anticuerpos | Temperatura de almacenamiento | Observaciones | |||
| 2-8 ºC | 22-25 ºC | 25-37 ºC | >37 ºC | ||
| Hepatitis B (ENGERIX B) |
Estable 3·años | Estable 168·horas | Estable 72·horas | Se desconoce | No debe congelarse Tras la reconstitución se debe desechar si no se utiliza en un plazo de 8 horas |
| Hepatitis B (HB VAXPRO) |
Estable 3·años | Estable 72·horas | Se desconoce | Se desconoce | Puede administrarse siempre que el tiempo total (acumulado) a 8 a 25 °C o 0·a 2·°C no sea superior a 72 horas No debe congelarse Conservar en el embalaje original para protegerlo de la luz |
| Hepatitis B adyuvada (FENDRIX) |
Estable 3·años | Estable 72·horas entre 8 y 37·ºC | Estable 72·horas entre 8 y 37 ºC | Se desconoce | No debe congelarse. Proteger de la luz |
|
Nirsevimab (Ac VRS) |
Estable 3 años | Estable 8·horas entre 20 y 25·ºC | Se desconoce | Se desconoce | Se puede mantener a temperatura ambiente (20°C - 25°C) protegido de la luz durante un máximo de 8 horas. Después de este tiempo, la jeringa se debe desechar. No congelar |
| DTPa (INFANRIX) No comercializada | Estable 3·años | Estable 168·horas | Se desconoce | Se desconoce | No debe congelarse |
| DTPa-VHB; DTPa-Hib; DTPa-VPI-Hib; DTPa-VPI-Hib-HB (excepto VAXELIS) | Estable 3 a 4·años | Estabilidad variable según preparado comercial y combinación de vacunas | INFANRIX HEXA entre 8 y 25·ºC estable 72 horas e INFANRIX-IPV+Hib entre 8 y 30·ºC estable 72 horas Tras la reconstitución desechar si no se utiliza en un plazo de 8 horas No deben congelarse |
||
| DTPa-VPI-Hib-HB (VAXELIS) | Estable 4·años | Estable 228·horas | Se desconoce | Se desconoce | La vacuna es estable a temperaturas de hasta 25 °C durante 150 horas No debe congelarse Conservar el envase en el embalaje exterior para protegerlo de la luz |
| DTPa-VPI (INFANRIX-IPV) | Estable 3 años | Se desconoce | No debe congelarse Conservar en el embalaje original para protegerla de la luz |
||
| DTPa-VPI (TETRAXIM) | Estable 3 años | Se desconoce | No debe congelarse | ||
| Td | Estable de 2·a·7·años | Estable de 6 a 12 meses | Estable hasta 6·semanas | Actividad satisfactoria durante pocos días a 45 ºC. Inestable a más de 55·ºC | No debe congelarse |
| Tdpa y Tdpa-VPI (BOOSTRIX y BOOSTRIX POLIO) | Estable 4 y 3·años, respectivamente | 7 días | Se desconoce | No debe congelarse Conservar en el embalaje original para protegerlo de la luz. |
|
| Tdpa (TRIAXIS) | Estable 3 años | Estable hasta 25°C durante 72·horas | Se desconoce | No debe congelarse. Desechar la vacuna si se ha congelado. Conservar la jeringa en el embalaje exterior para protegerla de la luz |
|
| Haemophilus influenzae tipo b (HIBERIX) | Estable 3·años | Estable 168·horas | Estable 168 horas | Se desconoce | Conservar en el embalaje original para protegerla de la luz El polvo no se ve afectado por la congelación El disolvente no debe congelarse |
| Polio inactivada | Estable·1·a·4·años | Descenso del Antígeno D del tipo 1 después de 20·días | Pérdida total del Antígeno D del tipo·1 tras 20·días | No disponible | No debe congelarse Fotosensible |
| Neumococo conjugado (SYNFLORIX) |
Estable 4·años | Estable 168·horas | Se desconoce | Se desconoce | No debe congelarse |
| Neumococo conjugado (PREVENAR 13) | Estable 3·años | Es estable a temperaturas de hasta 25·ºC durante 4·días | Se desconoce | Es estable a temperaturas de 40·ºC durante 4·días | No debe congelarse |
| Neumococo conjugado (PREVENAR 20) | Estable 2·años | Es estable a temperaturas de hasta 25·ºC durante 4·días | Se desconoce | Se desconoce | Estable 72 horas cuando se conserva a temperaturas de 0 °C a 2 °C No debe congelarse |
| Neumococo conjugado (VAXNEUVANCE) | Estable 30·meses | Es estable a temperaturas de hasta 25·ºC durante 48 horas | Se desconoce | Se desconoce | No debe congelarse |
| Neumococo polisacárido (PNEUMOVAX 23) | Estable 28·meses | Se desconoce | No debe congelarse | ||
| Rotavirus (ROTATEQ) |
Estable 2·años | Estable 36·horas | Se desconoce | Puede administrarse siempre que el tiempo total (acumulado) a 20-25 °C no sea superior a 36 horas. Si el tiempo a 20-25 °C es inferior a 36 horas, puede volver a guardarse en la nevera y usarse más tarde Conservar el tubo dosificador en el embalaje exterior para protegerlo de la luz |
|
| Rotavirus (ROTARIX) |
Estable 3·años | Estable 72·horas entre 8 y 25·ºC | Estable 24·horas entre 25 y 37 ºC | Se desconoce | Una vez abierta, la vacuna debe usarse inmediatamente No debe congelarse, aunque permanece estable hasta -18 ºC Conservar en el embalaje original para protegerla de la luz |
| Meningococo·B (BEXSERO) |
Estable 4·años | Estable 48·horas | Se desconoce | No congelar Estable entre 0 ºC y 2 ºC máximo 48 horas |
|
| Meningococo B (TRUMENBA) |
Estable 3·años | Se desconoce | Se desconoce | No debe congelarse | |
| Meningococo C conjugado (NEISVAC-C) |
Estable 3·½·años | Estable, al·menos, 9·meses | Conserva hasta un 90 % de su actividad durante 30 días a 40 ºC | Fotosensible. No debe congelarse, ni permanecer a menos de 2 ºC | |
| Meningococo C conjugado (MENINGITEC) |
Estable 2·años | Estable a 25.ºC durante 3·meses | No puede superar 25 ºC durante más de 24·horas | Fotosensible No debe congelarse, ni permanecer a menos de 2 ºC |
|
| Meningococo C conjugado (MENJUGATE) |
Estable 3·años | Estable 120·horas | Se desconoce | Estable entre 0 ºC y 2 ºC máximo 48 horas No debe congelarse |
|
| Meningococo A,C,W,Y (MENQUADFI) |
Estable 3·½·años | Estable a 25·ºC durante 72·horas | Se desconoce. Contactar con laboratorio | No debe congelarse | |
| Meningococo A,C,W,Y (MENVEO) |
Estable 4·años | Estable 120·horas | Se desconoce | Entre 0 y 2 ºC es estable 72 horas Tras la reconstitución administrar inmediatamente, aunque es estable 8 horas a menos de 25·ºC Evitar la luz No debe congelarse |
|
| Meningococo A,C,W,Y (NIMENRIX) |
Estable 4·años | Soporta temperaturas de hasta 37 °C ± 2 °C durante 30 días | Se desconoce | Evitar la luz Tras la reconstitución administrar inmediatamente, aunque es estable durante 8 horas a 30 ºC |
|
| Tabla 6.1 (2 de 2). Termoestabilidad de las inmunizaciones comercializadas en España (continuación) | |||||
| Vacunas/Anticuerpos | Temperatura de almacenamiento | Observaciones | |||
| 2-8 ºC | 22-25 ºC | 25-37 ºC | >37 ºC | ||
| Triple vírica (MMRVAXPRO) |
Estable 24·meses | Se desconoce | Después de la reconstitución, la vacuna debe utilizarse inmediatamente; sin embargo es estable 8 horas a 2-8 °C No debe congelarse Conservar el vial de polvo en el embalaje exterior para protegerlo de la luz |
||
| Triple vírica (PRIORIX) |
Estable 24·meses | Estable 72·horas | Se desconoce | Estable hasta -20 ºC Proteger de la luz La vacuna se debe inyectar rápidamente después de la reconstitución. Si no fuese posible, se debe conservar entre 2 y 8 ºC y utilizar antes de 8 horas tras la reconstitución |
|
| Varicela (VARILRIX) |
Estable 24·meses | Estable 72 horas | Se desconoce | Estable tras congelación hasta -20 ºC Fotosensible Tras la reconstitución no congelar la vacuna y se puede mantener hasta 90 minutos a 25·ºC y hasta 8 horas en nevera (entre 2·ºC y 8 ºC) antes de su uso |
|
| Varicela (VARIVAX) |
Estable 24·meses | Estable a 20-25·ºC 30·minutos | Se desconoce | Después de la reconstitución, la vacuna debe utilizarse inmediatamente; sin embargo es estable 30 minutos a 20-25 °C No debe congelarse Conservar el vial en el embalaje exterior para protegerlo de la luz |
|
| Tetravírica (PRIORIX TETRA) No comercializada |
Estable 18·meses | Estable 72·horas | Se desconoce | Estable hasta menos -20 ºC Proteger de la luz La vacuna se debe inyectar rápidamente después de la reconstitución. Si no fuese posible, se debe conservar entre 2 y 8 ºC y utilizar antes de 24 horas tras la reconstitución |
|
| Tetravírica (PROQUAD) |
Estable 18·meses | Estable a 20-25·ºC 30·minutos | Se desconoce | Después de la reconstitución, la vacuna debe utilizarse inmediatamente; sin embargo es estable 30 minutos a 20-25 °C No debe congelarse Conservar en el embalaje original para protegerlo de la luz |
|
| Papilomavirus (CERVARIX) |
Estable 5·años | Estable 72·horas | Estable 24·horas entre 25 y 37 ºC | Se desconoce | No debe congelarse |
| Papilomavirus (GARDASIL) No comercializada |
Estable 3·años | Estable 96 horas entre 8 y 40 ºC | Los datos de los estudios de estabilidad indican que los componentes de la vacuna son estables durante 96 horas cuando se almacena a temperaturas desde 8°C a 40°C. Al final de este período Gardasil se debe utilizar o desechar. No debe congelarse Conservar el envase en el embalaje exterior para protegerlo de la luz |
||
| Papilomavirus (GARDASIL 9) | Estable 3·años | Estable 96 horas entre 8 y 40 ºC | Los datos de estabilidad indican que los componentes de la vacuna son estables durante 96 horas cuando se almacena a temperaturas de 8 °C a 40 °C o durante 72 horas cuando se almacena a temperaturas de 0 °C a 2 °C. Al final de este período Gardasil 9 se debe utilizar o desechar. No debe congelarse Conservar el envase en el embalaje exterior para protegerlo de la luz |
||
| Vacuna covid. Bimervax (Hipra) | Vial sin abrir multidosis 21 meses entre 2 ºC y 8 ºC Vial perforado multidosis Estable 6 horas entre 2 ºC y 8·ºC desde el momento de la primera punción de la aguja. Tras la primera apertura (primera punción de la aguja), la vacuna debe usarse de manera inmediata Vial unidosis 1 año entre 2 ºC y 8 ºC |
||||
| Vacuna covid. Comirnaty (Pfizer) | Cada una de las presentaciones de esta vacuna tiene distintas formas de conservación, por lo que se debe acudir a su ficha técnica para conocer sus características | Una vez descongelada, la vacuna no se debe volver a congelar Durante la conservación, reduzca al mínimo la exposición a la luz ambiente y evite la exposición directa a la luz del sol y a la luz ultravioleta |
|||
| Vacuna covid. Janssen | El vial sin abrir es estable 2 años entre –25 y –15 °C Una vez extraída del congelador, la vacuna sin abrir se puede conservar refrigerada entre 2 y 8 °C, protegida de la luz, durante un periodo único de hasta 11 meses, sin superar la fecha de caducidad impresa. También sin abrir es estable durante un total de 12 horas entre 9 y 25 °C Una vez descongelada, la vacuna no se debe volver a congelar |
Se ha demostrado la estabilidad química y física de la vacuna durante el uso, incluso durante el transporte, hasta 6 horas entre 2 y 25·°C después de la primera punción del vial. Desde un punto de vista microbiológico, el producto se debe utilizar preferiblemente inmediatamente después de la primera punción del vial; sin embargo, el producto se puede conservar entre 2 y 8 °C durante un máximo de 6 horas o permanecer a temperatura ambiente (25·ºC como máximo) hasta 3 horas después de la primera punción del vial Conservar los viales en la caja original para protegerlos de la luz |
|||
|
Vacuna covid. Nuvaxovid (Novavax) |
El vial sin abrir es estable 12 meses entre 2 y 8 ºC Sin abrir ha demostrado ser estable durante un máximo de 12 horas a 25 °C. La conservación a 25 °C no se ajusta a las condiciones de conservación o envío recomendadas, pero puede guiar las decisiones para su uso en caso de oscilaciones temporales de la temperatura durante el almacenamiento de 9 meses a una temperatura de entre 2 y 8 °C |
Se ha demostrado una estabilidad química y física en uso durante 6 horas a una temperatura de entre 2 y 25 °C desde el momento de la primera perforación con la aguja hasta la administración, pero desde un punto de vista microbiológico, después de la primera apertura (primera perforación con la aguja), la vacuna debe utilizarse inmediatamente No deben congelarse Conservar los viales en la caja original para protegerlos de la luz |
|||
| Vacuna covid. Spikevax (Moderna) | El vial sin abrir es estable 9 meses entre –50 y –15 °C La vacuna sin abrir puede almacenarse refrigerada entre 2 y 8·°C, protegida de la luz, durante un máximo de 30 días. Dentro de este periodo, se puede transportar durante 12 horas. La vacuna sin abrir puede almacenarse entre 8 y 25 °C durante 24 horas tras extraerla de las condiciones de refrigeración. Una vez descongelada, la vacuna no se debe volver a congelar |
La estabilidad química y física en uso ha sido demostrada durante 19 horas entre 2 y 25 ºC después de la primera perforación (dentro del periodo de uso permitido de 30 días entre 2 y 8·ºC y de 24 horas entre 8 y 25 ºC) Conservar en la caja original para protegerlo de la luz |
|||
| Vacuna covid. Vaxzevria (AstraZeneca) | El vial sin abrir es estable 9 meses si se conserva en nevera (2 - 8 °C) El período de validez de viales sin abrir incluye las siguientes desviaciones imprevistas de la conservación entre 2 y 8 °C por un período único de 12 horas hasta 30 °C y de 72 horas hasta –3 °C. Los viales sin abrir deben siempre retornarse a su conservación entre 2 y 8 °C, tras una desviación de temperatura |
Se ha demostrado la estabilidad química y física durante el uso durante 6 horas si se conserva a temperaturas de hasta 30·°C y durante 48 horas si se conserva entre 2 y 8 °C. Después de este tiempo, el vial se debe desechar. No lo devuelva a la nevera después de haberlo conservado fuera de la misma De forma alternativa, un vial abierto puede conservarse entre 2 y 8 °C por un máximo de 48 horas si es devuelto inmediatamente a la nevera tras cada punción Conservar los viales en el cartonaje exterior para protegerlos de la luz |
|||
| Gripe inactivada | Validez limitada al año en curso | Estable durante escasos días. No debe superar los 20·ºC | Se desconoce | FLUARIX TETRA estable 72 horas entre 8 y 25·ºC Fotosensible No debe congelarse |
|
| Gripe viva (FLUENZ) |
Estable 18·semanas | Estable 12·horas entre 8·°C y 25·°C | Se desconoce | Fotosensible No debe congelarse |
|
| Hepatitis A (HAVRIX 720 y 1440) | Estable 3·años | Estables 72·horas | Se desconoce | Se desconoce | No deben congelarse |
| Hepatitis A (VAQTA 25 y 50) | Estable 3·años | Se desconoce | No deben congelarse (la congelación destruye la potencia de la vacuna) | ||
| Hepatitis A+B (TWINRIX PEDIÁTRICO Y ADULTOS) |
Estable 3·años | Estable 168·horas entre 8 y 25·ºC | Se desconoce | Se desconoce | No deben congelarse |
| BCG Problemas de suministro | Estable 18·meses | Estabilidad variable. 20-30·% de pérdida de viabilidad en 3·meses | Estabilidad variable. 20·% de pérdida de viabilidad en 3·a·14·días | Inestable | A 70 ºC pérdida de viabilidad en 30 minutos Fotosensible No congelar Una vez reconstituida permanece estable 4 horas |
|
VRS |
Estable 3·años |
Estable 5 días entre 8 y 30 ºC. |
Se desconoce |
El vial sin abrir es estable durante 5 días cuando se conserva a temperaturas de 8·ºC a 30 ºC. Al final de este período, Abrysvo debe utilizarse o desecharse |
|
| Cólera (DUKORAL) Problemas de suministro |
Estable 3·años | Estable a temperaturas no superiores a 25.ºC durante un período de 14 días | Se desconoce | No debe congelarse Una vez que se ha disuelto el granulado efervescente en agua y se ha añadido la suspensión que contiene la vacuna, la mezcla debe ingerirse en un plazo máximo de 2 horas |
|
| Cólera (VAXCHORA) |
Estable 18·meses | En su embalaje exterior, es estable hasta 12 horas a 25°C. | Se desconoce | Conservar en el embalaje original No exponer a temperaturas superiores a 25°C Tras la reconstitución, la suspensión debe ingerirse en un plazo de 15 minutos |
|
| Encefalitis japonesa (IXCHIARO) |
Estable 3·años | Se desconoce | Conservar en el embalaje original Fotosensible No debe congelarse |
||
| Fiebre amarilla (STAMARIL) |
Estable 3·años | Se desconoce. Contactar con laboratorio | No debe congelarse Conservar el vial de polvo y la jeringa de disolvente en el embalaje exterior para protegerlo de la luz Después de la reconstitución, usar inmediatamente |
||
| Fiebre tifoidea atenuada (VIVOTIF) |
Estable 18·meses | Estable 24·horas a 25·ºC | Inestable | Inestable | Fotosensible Estable hasta 72 h entre -19 ºC y +1 ºC |
| Fiebre tifoidea inactivada (TYPHIM VI) |
Estable 3·años | Se desconoce. Contactar con laboratorio | No debe congelarse Conservar la jeringa en el embalaje exterior para protegerlo de la luz. |
||
| Rabia (células diploides humanas) (VACUNA ANTIRRÁBICA MERIEUX) |
Estable 3·años | Se desconoce. Contactar con laboratorio | No debe congelarse La vacuna reconstituida debe administrarse inmediatamente Conservar el vial en el embalaje exterior para protegerlo de la luz. |
||
| Rabia (RABIPUR) |
Estable 48·meses | Estable 48 horas entre 8 y 30·ºC | Se desconoce | Tras la reconstitución permanece estable 6 a 8·horas entre 2 ºC y 8 ºC No debe congelarse |
|
En rojo las que no están comercializadas en España en el momento actual
Fuentes:
- Datos obtenidos de los laboratorios fabricantes.
- CAV-AEP. Fichas técnicas de los preparados.
- Manual de Vacunas Euskadi. Termoestabilidad de vacunas. Mayo de 2024.
- Portal Murcia Salud. Termoestabilidad de las vacunas. Mayo 2019.
- PATH. Summary of stability data for licensed vaccines. 2012.
- World Health Organization. Temperature sensitivity of vaccines. March 2014.
- Immunize.org. Ask the Experts: Storage & Handling. 2023.
- NHS. Refrigerated medicines stability tool. 2025.
La temperatura óptima de conservación está entre +2 °C y +8 °C; cualquier exposición fuera de este rango puede acarrear una pérdida de respuesta inmunitaria de la inmunización, que no es deseable.
Además hay 3 cosas importantes que se deben recordar: la inmunización debe conservarse en el embalaje original para protegerlo de la luz; no se debe utilizar una inmunización después de la fecha de caducidad indicada en la misma (último día del mes y año que figura en el envase, o en el caso de vacuna de la gripe atenuada, el día exacto de fecha de caducidad) y dado que los datos de estabilidad pueden actualizarse con nuevos estudios, se recomienda siempre ponerse en contacto con el titular de la comercialización.
La pérdida de la estabilidad puede ser debida a tres factores externos: la temperatura por congelación o por calor, por la luz y por el tiempo de exposición, pero también pueden ser provocados por factores intrínsecos de la vacuna. De cualquier manera supone que la pérdida de la capacidad inmunizante es siempre permanente, acumulativa e irreversible.
Factores intrínsecos de la inmunización
Inducidos por el tipo de cepa, los estabilizantes, los conservantes, los diluyentes y los residuos, la forma de presentación (envases multidosis que deben ser administrados en la misma sesión, así como las inmunizaciones liofilizadas que, para no perder sus propiedades, deben ser utilizadas antes de las 8 horas, la triple vírica a los 30 minutos de la reconstitución) y la caducidad.
Factores extrínsecos de la inmunización
- Termoestabilidad (tabla 6.1)
- Sensibles a la congelación: toxoide diftérico; toxoide tetánico; tosferina; polio inactivada; Haemophilus influenzae tipo b; gripe; neumococo; meningococo C; hepatitis A; hepatitis B; tifoidea inactivada; triple vírica (disolvente) y todas las combinaciones de estas inmunizaciones.
- No sensibles a la congelación: triple vírica (liofilizado); rabia; rotavirus (Rotarix), varicela (liofilizado); BCG; polio oral; fiebre amarilla.
- Test de agitación o floculación (en desuso): se puede realizar cuando existe sospecha de congelación, por su aspecto externo, en las inmunizaciones adsorbidas. La prueba consiste en agitar enérgicamente el vial de referencia y compararlo con otro no congelado. En el vial sospechoso de congelación aparecen una serie de partículas granulosas o flóculos, el líquido se presenta menos turbio y comienza a depositarse en el fondo, mientras que el vial bien conservado aparece sin gránulos y turbio. Al cabo de 60 minutos, los cristales de hielo forman partículas en suspensión que al ser más pesadas sedimentan de manera compacta en el fondo y al inclinarlo se mueven con mucha dificultad.
- Sensibles al calor: triple vírica; varicela; gripe y polio oral.
- No sensibles al calor (termoestables): toxoide diftérico; toxoide tetánico; hepatitis B, meningococo C, neumococo conjugada, rabia y VPH (Gardasil 9).
- Fotoestabilidad
Las inmunizaciones que presentan mayor riesgo de afectación por el efecto de la exposición a la luz son: triple vírica; varicela; gripe; Haemophilus influenzae tipo b; BCG; meningococo C; hepatitis A; polio oral y polio inactivada.
5. Almacenamiento: frigorífico
Considerado como la parte esencial del almacenamiento de la cadena fija en los centros de vacunación. El éxito de su uso correcto estriba en que las presentaciones vacunales han pasado de ser multidosis a monodosis en forma de jeringas precargadas y el aumento de inmunizaciones sistemáticas aprobadas por los distintos calendarios autonómicos hace imprescindible una buena logística.
Recomendaciones generales
- Debe estar conectado a la red general eléctrica de forma directa mediante enchufe de fuerza y con toma de tierra y como medida de seguridad nunca debe estar enchufado simultáneamente con otros aparatos eléctricos y esto debe estar señalizado en el enchufe con una pegatina que ponga “uso exclusivo”.
- Debe disponer de sistema de alarma y de un generador eléctrico de emergencia para casos de desconexión, avería o corte del suministro eléctrico. Estos 2 requisitos casi nunca se cumplen en los centros de salud.
- Debe disponer de un termostato que mantenga la temperatura ideal entre +2 °C y +8 °C y de congelador que proporcione temperaturas de –15 °C a –25 °C.
- De igual manera, debe poseer un termógrafo que permita registrar la temperatura de forma continuada y saber las oscilaciones de temperatura que haya tenido el frigorífico en un periodo de tiempo. Esta condición tampoco se cumple en la mayoría de los frigoríficos que contienen inmunizaciones.
- Los burletes de goma de la puerta deben estar intactos para que faciliten el cierre hermético del electrodoméstico. Se colocará sobre un plano recto y firme, separado unos 15-20 cm de la pared, que permita la libre circulación del aire y evite el sobrecalentamiento del aparato. Permanecerá alejado de la exposición directa del sol o de cualquier otra fuente de calor.
- Se pueden usar los dos termómetros comentados anteriormente, ambos miden las temperaturas máximas y mínimas:
– Digital, colocar en el exterior, en lugar seguro y fijo para evitar caídas accidentales, siendo la parte superior la zona mejor.
– Mercurio (ya no se fabrican, ni se encuentran), situado en el interior, en la zona central, bien visible y nunca en la puerta.
- La recomendación de sumergir el sensor de temperatura en un líquido (mejor con un punto de congelación más bajo que el agua, como el suero salino o una solución alcohólica), busca que los registros de variaciones de temperaturas máximas y mínimas sean "significativos" y que no respondan a cambios térmicos de muy corta duración, que resultan irrelevantes. La más frecuente, la subida instantánea de la temperatura debida a la apertura de la nevera para retirar envases. El sensor sumergido (a falta de un registro continuo) amortigua esos picos y valles de corta duración, en la temperatura del aire interior de la nevera y ofrece, de esta forma, una lectura "tamponada" de qué es lo que pasa realmente con las variaciones de la temperatura en los materiales líquidos y sólidos que están almacenados en el interior del frigorífico, como las inmunizaciones.
- En el exterior de la puerta deben colocarse documentos importantes como:
– Aviso: NO ABRIR y NO DESCONECTAR.
– Teléfonos de contacto, fax y correos electrónicos de los responsables con los que se contactaría en caso de rotura de la cadena de frío.
– Hoja de registro de las temperaturas máximas y mínimas.
– Protocolo de actuación de la cadena de frío (debe ser conocido por todos los profesionales).
- Se descongelará cada 6-12 meses o siempre que la pared del congelador produzca una capa de escarcha superior a 0,5 cm, si el frigorífico no tiene el sistema no frost.
- Para estabilizar la temperatura interna del frigorífico y mantener el frío entre 6 y 12 horas (siempre con la puerta cerrada) en caso de corte de suministro eléctrico se debe haber hecho previamente:
– Colocar en el congelador (si lo hay) de forma ordenada los acumuladores de frío.
– Colocar botellas de plástico con agua, agua con sal y/o solución salina fisiológica en la puerta y en los estantes más alejados del congelador.
- No se deben utilizar los frigoríficos tipo no frost (sistema que incorporan algunos frigoríficos, consistente en un sistema de enfriamiento por aire que evita la formación de escarcha en el aparato y, por tanto, que haya que descongelarlo dos veces al año) porque no mantienen la temperatura estable ni uniforme en su interior y en determinados lugares pueden alcanzar temperaturas por debajo de 0·°C.
- Las bandejas deben ser de rejilla o estar perforadas para evitar la humedad y el depósito de agua que puede afectar a la integridad del envase de la vacuna.
- Debe ser de uso exclusivo para el almacenamiento de las inmunizaciones, evitando el uso compartido con alimentos, bebidas, medicamentos y muestras de laboratorio.
Distribución de las inmunizaciones
El volumen de las inmunizaciones almacenadas no debe exceder del 50·% de la capacidad total del frigorífico (en las campañas de gripe no se cumple nunca). La colocación de los preparados inmunizantes debe permitir de forma óptima la circulación del aire por el interior.
Los envases no deben tocar las paredes, guardando una distancia mínima de 5 cm para evitar la congelación y posible degradación. Deben conservarse en su envase original hasta el mismo momento de la administración.
Se deben colocar de forma agrupada por tipos y lotes, facilitando su visión mediante el etiquetado donde se indique el nombre del compuesto (cuidado con los colores de las cajas que son muy semejantes entre inmunizaciones de la misma casa comercial y pueden llevar a confusión). Colocar en la parte de delante, las inmunizaciones que tengan la fecha de caducidad más próxima. Retirar las inmunizaciones caducadas (expresado por el último día del mes y año que aparece en el envase y en el caso de la vacuna antigripal atenuada, en el día concreto de caducidad).
Las inmunizaciones de uso más frecuente se ubicarán en la parte más accesible y se garantizará la rotación de todas las inmunizaciones contenidas en el frigorífico. No deben guardarse en las puertas, porque la temperatura es superior al resto del frigorífico y son más frecuentes los cambios de temperatura.
Colocar en los estantes más fríos (en general, cercanos al congelador) las inmunizaciones de los gérmenes más sensibles al calor como varicela, triple vírica, gripe, polio oral, BCG y fiebre amarilla. En los estantes más alejados al frío, las inmunizaciones de toxoides (tétanos y difteria), tosferina, polio inactivada, hepatitis B, hepatitis A, neumocócica conjugada y polisacárídica, Haemophilus influenzae tipo b, virus del papiloma humano (VPH) y todos los diluyentes o disolventes vacunales.
En el estante inferior, colocar las botellas de agua y/o de suero fisiológico para mantener la temperatura en caso de avería o corte de suministro.
Actuación ante la rotura de la cadena de frío
Cuando se sospecha que las inmunizaciones han estado sometidas a temperaturas superiores a 15 °C o menores a 0 °C, se deben consultar las tablas de termoestabilidad (tabla 6.1) de las inmunizaciones afectadas y en caso de duda, notificar de forma inmediata la incidencia al coordinador responsable del área o distrito sanitario. Envío por fax o correo electrónico de una hoja de notificación de incidencias de rotura en la cadena de frío, indicando el puesto de inmunización y la persona responsable. En dicha hoja, se le informará acerca de:
- Tiempo aproximado del corte del suministro eléctrico, que haya provocado la descongelación. Tiempo aproximado del mal funcionamiento que haya supuesto la congelación. En ambos casos, si se desconoce el tiempo real, será el del tiempo que haya transcurrido desde el último registro.
- Indicación de la temperatura máxima y mínima, así como la actual dentro del interior y exterior del frigorífico.
- Tipo de inmunizaciones afectadas, indicando los nombres comerciales, número de dosis, lotes y fecha de caducidad, así como el aspecto físico de las mismas.
- Breve descripción de los motivos de las posibles causas del problema y de las medidas tomadas.
Cuando se prevea que la avería del frigorífico pueda ser de larga duración o de duración indefinida, se deben trasladar a otro frigorífico auxiliar, neveras portátiles o cajas isotérmicas que contengan acumuladores de frío e indicadores de monitorización de temperatura.
Mantener la puerta cerrada y con un aviso de forma ostensible que prohíba su apertura y la administración de las inmunizaciones.
Informar al servicio de mantenimiento para que corrija la avería a la mayor brevedad posible.
Inmovilizar las inmunizaciones hasta la comprobación de su viabilidad, hasta entonces es fundamental rotularlas con el mensaje “NO USAR”.
Una vez realizada su comprobación y si se consideran APTAS es recomendable que sean administradas lo antes posible, ya que puede haberse reducido su periodo de caducidad.
En el caso que sean consideradas NO APTAS, se procederá a su devolución, lo antes posible, al almacén de origen, haciendo mención sobre la temperatura máxima y mínima, el tiempo transcurrido de interrupción de la cadena de frío a la que han estado sometidas, así como la temperatura actual.
Este protocolo debe estar al alcance de todo el equipo y debe ser de obligado cumplimiento darlo a conocer a todo el personal sustituto.
A continuación, en la tabla 6.2, se muestra una relación de los principales errores evitables relacionados con el almacenamiento, manipulación y conservación de las inmunizaciones (descargar en PDF).
Tabla 6.2. Lista de errores prevenibles más frecuentes en el almacenamiento, manipulación y conservación de las inmunizaciones
|
ERROR |
Designar a una sola persona en lugar de, al menos, dos como responsable del almacenamiento y manipulación de las inmunizaciones
|
|
ERROR |
Guardar la inmunización incorrectamente
|
|
ERROR |
La puerta de la nevera ha quedado abierta de forma inadvertida
|
|
ERROR |
Almacenar alimentos, bebidas y otros medicamentos en la nevera de las inmunizaciones
|
|
ERROR |
Desconectar de forma inadvertida la fuente de alimentación de la nevera
|
|
ERROR |
Registrar temperaturas un número insuficiente de veces cada día
|
|
ERROR |
Registrar temperaturas fuera de rango, pero no hacer nada
|
|
ERROR |
Desechar registros de temperatura recientes Conserve sus registros de temperatura durante, al menos, 3 años. ¿Por qué? Porque…
|
|
ERROR |
No usar la inmunización con la fecha de caducidad más próxima primero Al almacenar un nuevo envío de inmunizaciones:
|
|
ERROR |
Manipular incorrectamente las inmunizaciones caducadas
|
|
ERROR |
Desechar viales multidosis prematuramente Casi todos los viales multidosis de inmunizaciones contienen un conservante y se pueden usar hasta la fecha de vencimiento que figura en el vial, a menos que haya contaminación real o los viales no estén almacenados en condiciones apropiadas. Para algunas inmunizaciones, el fabricante puede especificar que una vez que el vial haya sido manipulado o el tapón de goma perforado, la inmunización debe usarse dentro de un cierto número de horas o días. |
Lista de errores prevenibles descargable en formato PDF (0,1 MB)
Fuente: modificado y adaptado de the Immunization Action Coalition. Storage and Handling. Don't be guilty of these preventable errors in vaccine storage and handling! Actualizado en enero de 2025.
6. Recursos humanos
El personal sanitario es la parte principal del complejo proceso de la cadena de frío. En todo punto de inmunización debe existir un profesional responsable y un sustituto que pueda asumir su rol, cuando sea oportuno por necesidad del servicio; ambos tienen que tener una amplia formación en la cadena de frío y ser referentes del resto del personal.
Además, todos los profesionales que pertenezcan al programa de inmunización deben conocer no solo la técnica de administración, sino todo el proceso de almacenamiento, conservación, estabilidad y pautas de actuación frente a la rotura de la cadena de frío.
En concreto y referente a la cadena de frío, las tareas que debe realizar la persona responsable serán:
- Comprobar la correcta recepción de las inmunizaciones:
– Fecha de recepción y procedencia.
– Número de dosis recibidas que figuran en el albarán. Deben ser coincidentes con las solicitadas.
– El estado del embalaje, envases y etiquetados correctos sin presentar deterioros.
– Fecha de caducidad y laboratorio fabricante.
– La temperatura a la que han estado sometidas si son las correctas, para ello es imprescindible la verificación de los indicadores de temperatura.
– Notificar cualquier incidencia ocurrida en dicha recepción.
- Proceder a su almacenamiento de forma adecuada tan pronto como sea posible.
- Realizar la manipulación de forma correcta y segura.
- Comprobar las existencias y proceder a su petición si se precisa.
- Controlar las fechas de caducidad, de forma periódica.
- Devolución de las inmunizaciones caducadas al almacén principal.
- Comprobar el funcionamiento de los termómetros (digital o mercurio) de máxima y mínima y realizar la lectura de la temperatura, actual, máxima y mínima, al principio y al final del día y su posterior anotación en la gráfica mensual de temperaturas.
- Comprobar que la temperatura interior del frigorífico se encuentre entre +2 °C y +8 °C y que nunca exceda de +10 °C y revisar, en caso de frigorífico sin tecnología no frost, que la capa de hielo de las paredes del congelador no supere los 0,5 cm de espesor.
- Comprobar el adecuado almacenamiento de los acumuladores de frío en el congelador, si existieran, y de la presencia de botellas de agua o suero fisiológico en los estantes inferiores y en la puerta, que garanticen el mantenimiento adecuado de la temperatura en caso de avería eléctrica.
- Revisar periódicamente el estado y mantenimiento de todos los aparatos frigoríficos que contengan preparados relacionados con las inmunizaciones.
- Comprobar la disposición de cámaras auxiliares, cajas isotérmicas y neveras necesarias para el traslado de inmunizaciones, por si fuesen necesarias en caso de avería.
- Notificar cualquier incidencia acaecida con la rotura de la cadena de frío a los responsables directos del área o distrito sanitario y mantener un sistema de registro de incidencias. Todo el personal implicado, sin excepción alguna, que intervenga de una manera u otra durante el transporte, almacenamiento y manipulación de las inmunizaciones debe ser consciente de la importancia que tiene el cumplimiento del mantenimiento de la cadena de frío, como único garante de la efectividad e inmunogenicidad de las inmunizaciones frente a la enfermedad, en la comunidad.
7. Decálogo de la cadena de frío
A continuación, se relatan los 10 puntos considerados más importantes para un correcto mantenimiento de la cadena del frío en el manejo, transporte y almacenamiento de inmunizaciones:
Tabla 6.3. Decálogo de la cadena del frío.
|
1. El mantenimiento de la cadena de frío de las inmunizaciones es una condición fundamental para garantizar la efectividad del programa de inmunización. 2. Las inmunizaciones son medicamentos biológicos, termosensibles y fotosensibles que pueden verse degradados por el frío, el calor y la luz, lo que puede ocasionar una pérdida en su capacidad inmunizante. 3. La temperatura óptima de conservación para lograr el efecto protector y evitar reacciones no deseables se encuentra entre +2 °C y +8 °C. 4. Cualquier alteración en la cadena de frío puede ocasionar la pérdida de la capacidad inmunizante, que es acumulativa, permanente, no se recupera y se incrementa con el tiempo de exposición. 5. Debe existir en cada centro sanitario la figura de un coordinador (y un sustituto) que sea responsable de la conservación, manipulación y almacenamiento de las inmunizaciones. 6. Se debe realizar el control de las temperaturas por medio de las lecturas de los termómetros y su registro correspondiente, dos veces al día, al comienzo y al final de la jornada laboral. 7. Cualquier anomalía de la temperatura que se produzca deberá ser comunicada lo antes posible al responsable del distrito o área sanitaria, quedando dichas inmunizaciones inmovilizadas hasta que se notifique si se pueden utilizar o no. 8. El protocolo de actuación sobre la cadena de frío debe ser consensuado y actualizado por todo el equipo integrante del programa y dado a conocer a todo el personal sustituto. 9. De la misma forma, debe colocarse en lugar visible, los teléfonos, fax y correo electrónico de la persona responsable superior a la que dirigirse en caso de rotura de la cadena de frío. 10. Los fallos en el transporte, conservación y almacenamiento de las inmunizaciones constituyen un riesgo real y son más habituales de lo deseable. Consulte la tabla 6.2 para evitarlos. |
8. Mantenimiento de la cadena del frío para inmunizaciones adquiridas en farmacias comunitarias
En ocasiones, las familias han de adquirir inmunizaciones en las farmacias comunitarias y encargarse del adecuado transporte y conservación en sus propios domicilios hasta la administración. Es el caso de ciertas inmunizaciones sistemáticas que están recomendadas por el CAV-AEP, pero que por el momento no son financiadas por la sanidad pública en algunas comunidades autónomas y, por lo tanto, no están disponibles en los centros de salud, como las inmunizaciones frente al rotavirus (faltan Andalucía y Extremadura, que la incorporarán lo largo de 2025) o la vacuna tetravalente frente a los meningococos ACWY a los 4 y 12 meses de edad.
De la misma manera, otras inmunizaciones no sistemáticas también pueden ser adquiridas con receta médica en las farmacias, especialmente algunas relacionadas con viajes internacionales y la de la gripe destinada a personas no incluidas en grupos de riesgo. Estas inmunizaciones también han de ser custodiadas y transportadas de forma segura hasta que llegue el momento de su aplicación, que ha de ser llevada a cabo preferiblemente en un centro sanitario.
Nuestra web dispone de un apartado monográfico con recomendaciones prácticas sobre estos aspectos, que puede resultar de utilidad para la población general.
9. Bibliografía
- Alberta Health Services. Immunization Program Standards Manual. Standard on Vaccine Storage and Handling. Published April 15, 2025.
- Alcántara González MA, et al. Transporte, conservación y almacenamiento de las vacunas. En: Comité Asesor de Vacunas de la Asociación Española de Pediatría (CAV-AEP). Vacunas en Pediatría. Manual de la AEP 2012, 5.ª ed. Madrid: Exlibris ediciones SL; 2012. p. 23-40.
- Batalla J, et al. Cadena de frío y logística de los programas de inmunización. En: Salleras Sanmartí LI. Vacunaciones Preventivas. Principios y Aplicaciones, 2.ª ed. Barcelona: Masson; 2003. p. 681-733.
- Blenke E, et al. The Storage and In-Use Stability of mRNA Vaccines and Therapeutics: Not A Cold Case. J Pharm Sci. 2023;112:386-403.
- Centers for Disease Control and Prevention (CDC). Guidelines for Storage and Temperature Monitoring of Refrigerated Vaccines.
- Centers for Disease Control and Prevention (CDC). Package Inserts for US Licensed Vaccines – Reources for Health Professionals.
- Centers for Disease Control and Prevention (CDC). Pink Book. Chapter 5: Vaccine Storage and Handling.
- Centers for Disease Control and Prevention (CDC). Vaccine Storage & Handling TOOLKIT. March 2024.
- FDA US FOOD & DRUG. Vaccines Licensed for Use in the United States.
- Grupo de Trabajo de Buenas Prácticas del Consejo General de Colegios Oficiales de Farmacéuticos. Adquisición, almacenamiento, custodia y conservación de medicamentos y productos sanitarios. 2016.
- Canadá. National Advisory Committee on Immunization. National Vaccine Storage and Handling Guidelines for Immunization Providers (2015).
- Canadá. National Advisory Committee on Immunization. Canadian Immunization Guide. Part 1 General Guidelines. Storage and Handling of Immunizing Agents, Sep. 2022.
- Dumpa N, et al. Stabilyti of vaccines. AAPS PharmSciTech. 2019;20:42.
- Immunize.org. Ask the Experts: Storage & Handling. 2023.
- Kumar R, et al. Thermostable vaccines: an innovative concept in vaccine development. Expert Rev Vaccines. 2022;21:811-24.
- NHS. Immunisation against infectious disease: The Green Book. Cap 3 Storage, distribution and disposal of vaccines.
- NHS. Refrigerated medicines stability tool. 2025.
- NZ Health System. National Standards for Vaccine Storage and Transportation for Immunisation Providers.
- NZ Inmunisation Advisory Centre. Cold chain. Last updated: August 2024
- Ontario. Ministry of Health and Long-Term Care. Vaccine Storage and Handling Guidelines. Revised March 2025.
- Ortega P, et al. Problemática de la ruptura de la cadena del frío: congelación y calentamiento. Pérdida del efecto vacunal. En: De Juanes JR (ed.). Actualización en vacunas. 2005. Madrid: Marco Gráfico; 2005. p. 83-90.
- PATH. Summary of stability data for investigational formulations of vaccines.
- PATH. Summary of stability data for licensed vaccines.
- Región de Murcia. Consejería de Sanidad y Consumo. Dirección General de Salud Pública. Servicio de Prevención y Protección de la Salud. Logística Vacunal. Cadena de Frío. Murcia, 2013.
- Rhode Island. Department of Health. Vaccine Storage & Handling Guide Updated September 2024
- The Nacional Storage Guidelines. Strive for 5. 3nd edition. Australian Government. Department of Health and Ageing, última actualización: April 2020.
- World Health Organization. Controlled temperature chain: Strategic Roadmap for Priority Vaccines 2017-2020, 4 July 2018
- World Health Organization. How to monitor temperatures in the vaccine supply chain. July 2015.
- World Health Organization. Temperature sensitivity of vaccines. March 2014.
- World Health Organization. WHO/KFDA Workshop on Stability Evaluation of Vaccines.
10. Enlaces de interés
- Canadian Immunization Guide: Storage and handling of immunizing agents
- Centers for Disease Control and Prevention (CDC). Vaccine Storage & Handling Reosurces
- Comité Asesor de Vacunas e Inmunizaciones de la AEP. Fichas técnicas de las inmunizaciones comercializadas en España
- Comité Asesor de Vacunas e Inmunizaciones de la AEP. Noticias sobre la conservación de las inmunizaciones
- Immunisation against infectious disease: The Green Book. Storage, distribution and disposal of vaccines: the green book, chapter 3
- Portal Murcia Salud. Pautas y protocolos
11. Historial de actualizaciones
| 7 de mayo de 2018 | Actualización del apartado "Conservación" en varicela y vacunas tetravíricas |
| 24 de agosto de 2018 | Nuevas citas bibliográficas |
| 10 de febrero de 2020 | Actualización del apartado "Conservación" con nuevos datos de laboratorios |
| 4 de octubre de 2021 | Actualización del apartado "Conservación" con las vacunas covid |
| 9 de noviembre de 2021 | Actualización del apartado "Conservación" con nueva información de las vacunas Sanofi-Pasteur |
| 27 de enero de 2022 | Actualización de todos los apartados |
| 7 de marzo de 2022 | Actualización del apartado "Conservación" con Nuvaxovid |
| 1 de julio de 2022 | Actualización de la tabla 6.1 con datos de Gardasil, Gardasil 9 y Vaqta facilitados por MSD |
| 1 de septiembre de 2022 | Actualización de la tabla 6.1 con Vaxchora y cese de comercialización de Gardasil |
| 25 de enero de 2023 | Cambio de nombre a Manual de Inmunizaciones |
| 15 de noviembre de 2023 | Actualización de la tabla 6.1 y revisión de todos los apartados. Nuevas citas bibliográficas |
| 1 de noviembre de 2024 | Actualización de la tabla 6.1 con Nirsevimab y Abrysvo |
| 14 de mayo de 2025 | Actualización de todos los apartados. Nuevas citas bibliográficas y enlaces de interés |
-oOo-



