Manual de inmunizaciones: nuevo capítulo sobre inmunizaciones frente a enfermedades tropicales
| Contenido |
|---|
| ● Introducción [ver]. ● Inmunizaciones frente al dengue [ver] | Dengvaxia [ver] | Qdenga [ver] | Nueva inmunización frente al dengue [ver]. ● Inmunizaciones frente al paludismo [ver] | RTS,S/AS01 (Mosquirix) [ver] | R21/Matrix-M [ver]. ● Inmunizaciones frente al chikunguña [ver] | Nueva inmunización frente al ckikunguña [ver]. ● Inmunizaciones frente a otras enfermedades tropicales [ver]. ● Más información en esta web, referencias y enlaces recomendados [ver] | Dengue [ver] | Paludismo [ver] | Chikunguña [ver]. ● Otras referencias [ver] | Chikunguña | Dengue | Paludismo (malaria). |
| En pocas palabras |
|---|
| ● Las enfermedades tropicales transmitidas por vectores siguen su expansión hacia zonas templadas. El cambio climático es, sin duda, un factor determinante para ello. ● La OMS viene haciendo un llamamiento para preservar la salud aplicando un enfoque de «Una Sola Salud» (One Health) que abarque la interconexión de la salud humana, la salud animal y del medio ambiente en general (incluidos los ecosistemas), fundamental para el control de las enfermedades tropicales. ● Están autorizadas dos inmunizaciones atenuadas intramusculares frente al dengue, con una eficacia al año de la última dosis en torno al 80 %. Los datos de un ensayo fase III de otra inmunización atenuada por vía subcutánea se han publicado en febrero de 2024, mostrando también una eficacia global del 80 %, pero con la ventaja de una única dosis. ● La OMS ha precalificado 2 inmunizaciones para la prevención del paludismo en países con alta endemicidad: RTS,S/AS01 en julio de 2022, y R21/MATRIX-M el 21 de diciembre de 2023. Esta última es la primera inmunización candidata que cumple con el objetivo del 75 % de eficacia planteado por la OMS. ● Hay una inmunización aprobada (FDA) frente a la chikunguña, para uso en personas a partir de 18 años. En febrero de 2024, el Comité de Medicamentos de Uso Humano (CHMP) de la EMA, ha concedido una evaluación acelerada de otra inmunización, para personas a partir de 12 años. Ambas son atenuadas y han demostrado ser muy inmunogénicas. ● El capítulo que ahora se presenta, ha sido realizado gracias a la colaboración entre la Sociedad Latinoamericana de Pediatría (SLIPE) y la Asociación Española de Pediatría a través de su Comité Asesor de Inmunizaciones (CAV-AEP). |
Introducción
 Las enfermedades tropicales son enfermedades infecciosas transmitidas por vectores especialmente prevalentes en regiones tropicales y subtropicales, siendo menos frecuentes en climas templados.
Las enfermedades tropicales son enfermedades infecciosas transmitidas por vectores especialmente prevalentes en regiones tropicales y subtropicales, siendo menos frecuentes en climas templados.
Dentro de las transmitidas por insectos, se encuentran las enfermedades por picadura de mosquitos de los géneros Aedes (dengue, chikunguña, zika, fiebre amarilla), Culex (virus del Nilo Occidental y otras encefalitis víricas) y Anopheles (paludismo/malaria). Aedes y Culex transmiten virus conocidos como arbovirus (contracción del inglés de arthropod-borne viruses), mientras que Anopheles transmite un parásito protozoario, el Plasmodium.
Los factores que contribuyen a la propagación de estas enfermedades son fundamentalmente el aumento de viajes, movimientos migratorios y comercio internacional, la expansión demográfica con el aumento de la presencia de humanos en zonas geográficas donde tienen el hábitat estos vectores, y, sin duda, el cambio climático, que está provocando que algunos de estos vectores estén ampliando su hábitat hacia zonas templadas, o han ido recuperando su presencia en zonas donde en el pasado se habían encontrado hasta su erradicación, como por ejemplo en España, donde circularon de forma endémica provocando enfermedades como el paludismo, el dengue y la fiebre amarilla.
La historia natural de las enfermedades transmitidas por vectores es compleja. Para que la transmisión ocurra tienen que coincidir el agente infeccioso (muchas veces vinculado a un reservorio animal para su persistencia), el vector competente y un huésped susceptible, humano o animal, todo ello bajo unas condiciones ambientales adecuadas. Por ello, la OMS viene haciendo un llamamiento para preservar la salud aplicando un enfoque de «Una Sola Salud» (One Health) que abarque la interconexión de la salud humana, la salud animal y del medio ambiente en general (incluidos los ecosistemas).
Ahora, en el Manual de inmunizaciones en línea de la AEP se ha añadido un nuevo capítulo, el número 51, ubicado en la sección VII, titulado "Inmunizaciones frente a las enfermedades tropicales". El capítulo que hoy se presenta, ha sido realizado gracias a la colaboración entre la Sociedad Latinoamericana de Pediatría (SLIPE) y la Asociación Española de Pediatría a través de su Comité Asesor de Inmunizaciones (CAV-AEP). Por parte de la primera, han participado María Luisa Ávila Agüero (Costa Rica) y José Brea Del Castillo (República Dominicana), y por el CAV-AEP, Francisco J. Álvarez García, María Garcés Sánchez, Antonio Iofrío De Arce y Abián Montesdeoca Melián.
[volver al principio]
Inmunizaciones frente al dengue
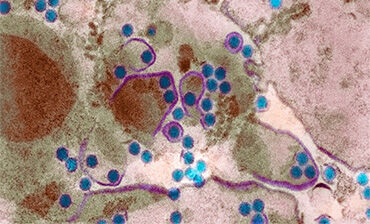 Existen dos inmunizaciones intramusculares comercializadas frente al dengue y autorizadas para su uso en varios países del mundo. En Europa ambas están aprobadas por la EMA, pero solo una de ellas está disponible en España.
Existen dos inmunizaciones intramusculares comercializadas frente al dengue y autorizadas para su uso en varios países del mundo. En Europa ambas están aprobadas por la EMA, pero solo una de ellas está disponible en España.
- Dengvaxia (Sanofi) es una inmunización tetravalente atenuada, elaborada con virus de la fiebre amarilla modificados mediante tecnología de ADN recombinante, para que expresen proteínas de los cuatro serotipos del DENV, aunque no induce respuesta frente a proteínas no estructurales. Entre los niños de 9 a 16 años con infección previa por el virus del dengue, tiene una eficacia global de alrededor del 80 %; contra el dengue sintomático confirmado virológicamente, la eficacia vacunal (EV) es del 82 % (IC95 %: 67 a 90), frente a hospitalización del 79 % (IC95 %: 69 a 86) y frente a dengue grave del 84 % (IC95 %: 63 a 93). En el año siguiente a la tercera dosis, la EV para las infecciones sintomáticas fue del 61,0 % (IC95 %: 29,6 a 86,5). Después de 6 años se redujo a una eficacia acumulada del 39,4 % (IC95 %: 0,2 a 63,0). Esto pone de relieve que la eficacia protectora se concentra en los primeros años tras de la inmunización. Solo debe utilizarse en personas de 6 a 45 años (aunque en varios países la indicación es partir de los 9 años) con infección previa demostrada por DENV mediante la detección de anticuerpos, ya que tras la inmunización en sujetos seronegativos aumenta el riesgo de dengue grave en las personas infectadas por segunda vez. No está disponible en España. La pauta consta de 3 dosis, con intervalos de 6 meses entre ellas.
- Qdenga (Takeda) es también una inmunización tetravalente atenuada compuesta por una cepa del DENV-2 y tres virus quiméricos (basados en el DENV-2) a los que se les inserta mediante tecnología de ADN recombinante el material genético que codifica la proteína M premembrana y las proteínas de la envuelta del DENV-1, DENV-3 y DENV-4. En cuanto a EV, a los 12 meses tras la pauta completa (2 dosis), la eficacia de la inmunización fue del 80,2 %. A los 18 meses, la eficacia de la inmunización contra todo el dengue en los receptores inmunes fue del 76,1 % y del 66,2 % en los receptores no inmunes al dengue; la eficacia frente a la hospitalización fue del 90,4 % y del 85,9 % contra el dengue hemorrágico; la eficacia específica del tipo fue del 69,8 % para DENV-1, del 95,1 % para DENV-2 y del 48,9 % para DENV-3, con intervalos de confianza variables. No hubo suficientes casos de DENV-4 para calcular la EV. La inmunización está autorizada para personas a partir de 4 años, hayan pasado o no la enfermedad anteriormente, no habiendo datos en individuos de más de 60 años, aunque la ficha técnica recoge que no es necesario ajustar la dosis en personas de ≥60 años. En España, está disponible en los Centros de vacunación Internacional. La pauta consta de 2 dosis con 3 meses de intervalo.
[volver al principio]
Nueva inmunización frente al dengue
El 1 de febrero de 2024 han sido publicados los resultados del ensayo doble ciego de fase 3 realizado en Brasil con otra inmunización atenuada tetravalente (Butantan-DV), en dosis única subcutánea. Está compuesto por virus atenuados para DENV-1, DENV-3 y DENV-4 y un virus quimérico que contiene los genes DENV-2 que codifican la premembrana y proteínas de la envoltura. En los participantes de 2 a 6 años, la EV fue del 80,1 % (IC95 %: 66,0 a 88,4), entre los de 7 a 17 años fue del 77,8 % (IC95 %: 55,6 a 89,6) y entre los de 18 a 59 años, del 90,0 % (IC95 %: 68,2 a 97,5). La eficacia global contra DENV-1 fue del 89,5% (IC95 %: 78,7 a 95,0), siendo del 96,8 % entre los participantes seropositivos y del 85,6 % entre los seronegativos. La EV global frente a DENV-2 fue del del 69,6 % (IC95 %: 50,8 a 81,5), siendo del 83,7 % entre los participantes seropositivos y del 57,9 % entre los seronegativos. No se detectaron casos por DENV-3 y DENV-4 durante el período de seguimiento. Como conclusión los autores destacan que una dosis única de esta inmunización previno el DENV-1 y el DENV-2 sintomáticos, independientemente del estado serológico del dengue al inicio del estudio, durante los 2 años de seguimiento.
[volver al principio]
Inmunizaciones frente al paludismo
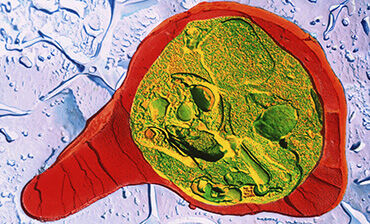 Actualmente se cuenta con dos inmunizaciones precalificadas por la OMS (Mosquirix el 8 de julio de 2022, y R21/Matrix-M1 el 21 de diciembre de 2023), ambas por vía intramuscular, para la prevención del paludismo en regiones con transmisión de moderada a alta por P. falciparum, especialmente en el África subsahariana.
Actualmente se cuenta con dos inmunizaciones precalificadas por la OMS (Mosquirix el 8 de julio de 2022, y R21/Matrix-M1 el 21 de diciembre de 2023), ambas por vía intramuscular, para la prevención del paludismo en regiones con transmisión de moderada a alta por P. falciparum, especialmente en el África subsahariana.
Son estas:
- RTS,S/AS01 (Mosquirix, GSK): aprobada por la EMA para niños entre 6 semanas y los 17 meses de edad para la primera dosis, y por la OMS para niños entre 5-17 meses para la primera dosis. La pauta consta de 3 dosis de primoinmunización con 4 semanas de intervalo entre ellas, y una dosis de refuerzo a los 12-18 meses. Entre 2009 y 2011 se llevó a cabo un estudio de fase 3 controlado con placebo en más de 15·000 lactantes de 7 países africanos, divididos en dos grupos: de 6 a 12 semanas de edad, entre 5 a 17 meses. En el grupo de 5 a 17 meses de edad, la inmunización previno aproximadamente 4 de cada 10 casos durante 4 años de seguimiento (EV del 36,3 %; IC95 %: 31,8 a 40,5) y aproximadamente 3 de cada 10 casos graves (EV del 32,2 %; IC95 %: 13,7 a 46,9), con reducciones significativas también de los ingresos hospitalarios. La eficacia fue menor en los lactantes de 6-12 semanas de edad. En 2015, los grupos asesores de la OMS recomendaron realizar en estudio piloto para completar la información sobre la efectividad de la inmunización. En enero de 2016, la OMS asumió la necesidad de completar los estudios antes de recomendar el despliegue de la inmunización en el continente africano, y así surgió el programa piloto con RTS,S/AS01 que se puso en marcha en 2019 en Ghana, Kenia y Malawi. El programa se cerró a finales de 2023, pero los tres países mantendrán a largo plazo sus programas de inmunización. Además, está prevista la introducción en 2024 en otros 9 países africanos: Benin, Burkina Faso, Burundi, Camerún, Liberia, Níger, República Democrática del Congo, Sierra Leona y Uganda. De hecho, el 22 de enero de 2024, Camerún ha sido el primer país en iniciar un programa de inmunización sistemática para niños en 42 de los distritos más afectados.
- R21/Matrix-M (Serum Institute de India y Universidad de Oxford): aprobada para niños de 5 a 36 meses para la primera dosis. La pauta consta de 3 dosis de primoinmunización con 4 semanas de intervalo entre ellas, y una dosis de refuerzo a los 12-18 meses. El ensayo fase 2b de esta inmunización se llevó a cabo en 2019, controlado y doble ciego, con 12 meses de seguimiento, en Nanoro, capital de Burkina Faso. La EV a los 12 meses tras la pauta de 3 dosis más la dosis de refuerzo fue del 75 %. El 1 de febrero de 2024 se ha publicado los resultados del estudio en fase 3 con la participación de 4800 niños de 5 a 36 meses de edad realizado en Burkina Faso, Kenia, Mali y Tanzania, con una EV a los 12 meses del 75% (IC95 %: 71 a 79; p<0,001) en los sitios con alta transmisión estacional de paludismo y del 68% (IC95 %: 61 a 74; p<0,001) en los sitios con más transmisión perenne. Hubo cierta disminución de la eficacia durante el primer año de seguimiento en los sitios de transmisión estacional y perenne, pero una dosis de refuerzo restauró la eficacia en los sitios estacionales con una eficacia de la inmunización durante 18 meses del 74 % (IC95 %: 70 a 77; p<0,001). Es la primera inmunización candidata que cumple con el objetivo del 75 % de eficacia planteado por la OMS.
[volver al principio]
Inmunizaciones frente al chikunguña
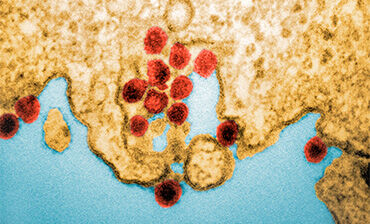 La FDA es la única agencia reguladora que ha autorizado, el 9 de noviembre de 2023, una inmunización atenuada intramuscular frente al CHIKV (Ixchiq, Valneva) en pauta de dosis única para personas a partir de 18 años con riesgo alto de exposición al CHIKV, bajo una aprobación acelerada basada en títulos de anticuerpos neutralizantes por encima de un umbral establecido (título de μPRNT50 ≥150) derivado de un modelo de primate no humano. A los 28 días tras la inmunización, esta indujo en los niveles seroprotectores en el 98,9 % (IC95 %: 96,7 a 99,8), sin diferencias según edad. El 96 % de los participantes mantuvieron la respuesta serológica seis meses después de la inmunización.
La FDA es la única agencia reguladora que ha autorizado, el 9 de noviembre de 2023, una inmunización atenuada intramuscular frente al CHIKV (Ixchiq, Valneva) en pauta de dosis única para personas a partir de 18 años con riesgo alto de exposición al CHIKV, bajo una aprobación acelerada basada en títulos de anticuerpos neutralizantes por encima de un umbral establecido (título de μPRNT50 ≥150) derivado de un modelo de primate no humano. A los 28 días tras la inmunización, esta indujo en los niveles seroprotectores en el 98,9 % (IC95 %: 96,7 a 99,8), sin diferencias según edad. El 96 % de los participantes mantuvieron la respuesta serológica seis meses después de la inmunización.
Actualmente, la Agencia Europea de Medicamentos (EMA), Health Canada y la Agencia Reguladora de Salud de Brasil (Anvisa) están revisando las solicitudes de comercialización con posibles aprobaciones en 2024. Para hacer más accesible esta inmunización para los países de medio y bajo índice de desarrollo humano, Valneva y el Instituto Butantan de Brasil firmaron un acuerdo en enero de 2021 para el desarrollo, fabricación y comercialización esta inmunización. El 28 de febrero de 2024, los CDC estadounidenses han aprobado la recomendación de uso en personas de 18 o más años de edad que van a viajar a zonas con transmisión conocida del virus del Chikunguña.
[volver al principio]
Nueva inmunización frente al ckikunguña
El 23 de febrero de 2024, el Comité de Medicamentos de Uso Humano (CHMP) de la Agencia Europea de Medicamentos (EMA) ha concedido una evaluación acelerada para la solicitud de autorización de comercialización para CHIKV VLP, inmunización de Bavarian Nordic compuesta por una partícula de tipo viral (VLP, por las siglas en inglés) construida con las proteínas de la cápside y la envoltura. La empresa tiene previsto presentar la documentación a la EMA en el primer semestre de 2024, y también a la FDA. Según la compañía, en 2023, se completaron dos estudios de fase 3 para esta inmunización. En ambos casos, se cumplieron con los criterios de valoración principales, demostrando la capacidad de CHIKV VLP para inducir altos niveles de anticuerpos neutralizantes contra chikunguña en individuos de 12 años o más. Uno de los estudios, incluyó a adolescentes y adultos sanos de 12 a 64 años (el otro fue en mayores de 64 años), y mostró que CHIKV VLP era altamente inmunogénica: el 98·% de los inmunizados desarrolló anticuerpos neutralizantes de chikunguña al día 22 tras la inmunización con una dosis intramuscular de 40 mcg. Estos anticuerpos se mantuvieron en niveles seroprotectores en el 86 % seis meses después de la inmunización.
[volver al principio]
Inmunizaciones frente a otras enfermedades tropicales
En el capítulo 52 de nuestro manual de inmunizaciones en línea (Inmunizaciones del futuro) pueden encontrar más información acerca de las investigaciones y productos en fase avanzada frente a otras enfermedades tropicales, como zika (apartado actualizado muy recientemente por Abián Montesdeoca Melián y Antonio Iofrío) o ébola. En dicho capítulo 52, aunque no se trata de una enfermedad tropical, también se ha actualizado muy recientemente el apartado sobre citomegalovirus (Lucía López Granados y Antonio Iofrío). En el capítulo 24 del Manual pueden encontrar todo lo referente a la inmunización frente a otra enfermedad transmitida por Aedes, la fiebre amarilla.
[volver al principio]
-oOo-
Más información en esta web
- CAV-AEP, 13 de noviembre de 2023. El dengue en Europa: nuevos casos en Cataluña.
- CAV-AEP, 6 de marzo de 2023. Casos de dengue con transmisión local en Ibiza.
- CAV-AEP. Otras noticias sobre el dengue y sus inmunizaciones.
- CAV-AEP, noviembre de 2023. Inmunización del dengue. En "las inmunizaciones, una a una", información para familias.
- CAV-AEP, noviembre de 2023. Dengue. En "enfermedades prevenibles", información para profesionales.
- CAV-AEP. 11 de diciembre de 2023. OMS: informe sobre el paludismo (malaria) en el mundo, 2023.
- CAV-AEP, 17 de mayo de 2023. Paludismo (malaria) 2: una nueva inmunización (R21/Matrix-M) ultima su desarrollo y puede ser la próxima.
- CAV-AEP, 14 de mayo de 2023. Paludismo (malaria) 1: la inmunización RTS,S/AS01e a punto para ser lanzada a gran escala.
- CAV-AEP, 2 de febrero de 2023. Inmunizaciones frente al paludismo (malaria).
- CAV-AEP. Otras noticias sobre el paludismo y sus inmunizaciones.
- CAV-AEP, 21 de junio de 2023. Primeros datos de nuevas inmunizaciones frente al chikunguña.
- CAV-AEP. Otras noticias sobre el virus chikunguña y sus inmunizaciones.
[volver al principio]
Referencias y enlaces recomendados
- ANDAVAC. Inmunización para viajeros internacionales.
- CDC. Travelers Health. Yellow Book 2024.
- Comité Asesor de Vacunas de la AEP. Enfermedades inmunoprevenibles.
- ECDC, European Centers for Disease Prevention and Control. Mosquito-borne diseases
- ECDC, European Centers for Disease Prevention and Control. Tick-borne diseases.
- Ministerio de Sanidad. Plan Nacional de Prevención, Vigilancia y Control de las Enfermedades Transmitidas por Vectores (abril 2023).
- Ministerio de Sanidad. Sanidad Exterior. Centros de Vacunación Internacional.
- National Travel Health Network and Centre (NaTHNac).
- OPS/PAHO. Cambio climático y salud.
- OPS/PAHO. Enfermedades desatendidas, tropicales y transmitidas por vectores.
- WHO. Fact sheets.
[volver al principio]
Dengue
- Deng SQ, et al. A Review on Dengue Vaccine Development. Vaccines (Basel). 2020;8:63.
- Halstead SB. Three Dengue Vaccines - What Now? N Engl J Med. 2024;390:464-5.
- Kallás EG, et al. Live, Attenuated, Tetravalent Butantan-Dengue Vaccine in Children and Adults. N Engl J Med. 2024;390:397-408.
- Kok BH, et al. Dengue virus infection - a review of pathogenesis, vaccines, diagnosis and therapy. Virus Res. 2023;324:199018.
- Paz-Bailey G, et al. Dengue Vaccine: Recommendations of the Advisory Committee on Immunization Practices, United States, 2021. MMWR Recomm Rep. 2021;70:1-16.
- Thomas SJ. Is new dengue vaccine efficacy data a relief or cause for concern? NPJ Vaccines. 2023;8:55.
- Torres-Flores JM, et al. Dengue Vaccines: An Update. BioDrugs. 2022;36:325-36.
- White LJ, et al. Defining levels of dengue virus serotype-specific neutralizing antibodies induced by a live attenuated tetravalent dengue vaccine (TAK-003). PLoS Negl Trop Dis. 2021;15:e0009258.
- WHO. The Global Advisory Committee on Vaccine Safety. Dengue vaccines.
[volver al principio]
Paludismo
- Aderinto N, et al. A perspective on Oxford's R21/Matrix-M™ malaria vaccine and the future of global eradication efforts. Malar J. 2024;23:16.
- Datoo MS, et al. Safety and efficacy of malaria vaccine candidate R21/Matrix-M in African children: a multicentre, double-blind, randomised, phase 3 trial. Lancet. 2024;403(10426);533-44.
- Duffy PE, et al. Malaria vaccines since 2000: progress, priorities, products. NPJ Vaccines. 2020;5:48.
- El-Moamly AA, et al. Malaria vaccines: the 60-year journey of hope and final success—lessons learned and future prospects. Trop Med Health. 2023;51:29.
- Laurens MB. RTS,S/AS01 vaccine (Mosquirix™): an overview. Hum Vaccin Immunother. 2020;16:480-9
- OMS. Vacunas antipalúdicas (RTS,S y R21). Preguntas y respuestas. 17 enero de 2024.
- Stanisic DI, et al. Malaria Vaccines: Progress to Date. BioDrugs. 2023;37:737-56.
- Willyard C. The slow roll-out of the world’s first malaria Vaccine. Nature. 2022;612:S48-9.
- WHO. Malaria vaccine: WHO position paper - March 2022. Weekly Epidemiological Record. 2022;97:60-78.
- WHO. Review of malaria vaccine clinical development. November 2022.
[volver al principio]
Chikunguña
- Bettis AA, et al. The global epidemiology of chikungunya from 1999 to 2020: A systematic literature review to inform the development and introduction of vaccines. PLoS Negl Trop Dis. 2022;16:e0010069.
- Cherian N, et al. Strategic considerations on developing a CHIKV vaccine and ensuring equitable access for countries in need. NPJ Vaccines. 2023;8:123.
- de Lima Cavalcanti TYV, et al. A Review on Chikungunya Virus Epidemiology, Pathogenesis and Current Vaccine Development. Viruses. 2022;14:969.
- Ly H. Ixchiq (VLA1553): The first FDA-approved vaccine to prevent disease caused by Chikungunya virus infection. Virulence. 2024;15:2301573.
- Richardson JS, et al. Safety and Immunogenicity of an Adjuvanted Chikungunya Virus (CHIKV) Virus-like Particle (VLP) Based Vaccine in Two Pivotal Phase 3 Trials, ≥12 Years of Age. Open Forum Infect Dis. 2023;10(Suppl 2):ofad500.2471.
- Roongaraya P, et al. Chikungunya vaccines: An update in 2023. Asian Pac J Allergy Immunol. 2023;41:1-11.
- Schneider M, et al. Safety and immunogenicity of a single-shot live-attenuated chikungunya vaccine: a double-blind, multicentre, randomised, placebo-controlled, phase 3 trial. Lancet. 2023;401:2138-47.
- Stephenson KE. Live-attenuated Chikungunya vaccine: a possible new era. Lancet. 2023;401:2090-1.
[volver al principio]
Otras referencias
Chikunguña
- Cerqueira-Silva G, et al. Risk of death following chikungunya virus disease in the 100 Million Brazilian Cohort, 2015–18: a matched cohort study and self-controlled case series. Lancet Infect Dis. 2024;24(5):504-13.
- Kang H, et al. Chikungunya seroprevalence, force of infection, and prevalence of chronic disability after infection in endemic and epidemic settings: a systematic review, meta-analysis, and modelling study. Lancet Infect Dis. 2024;24(5):488-503.
- Salje H, et al. The deadly potential of chikungunya virus. Lancet Infect Dis. 2024;24(5):442-4.
- Wilder-Smith AB, et al. Determining force of infection for chikungunya to support vaccine policy development. Lancet Infect Dis. 2024;24(5):441-2.
Dengue
- Flacco ML, et al. Immunogenicity, Safety and Efficacy of the Dengue Vaccine TAK-003: A Meta-Analysis. Vaccines. 2024;12(7):770.
- Medigeshi GR, et al. Quadrivalent dengue-virus vaccines: challenges and opportunities for India. Lancet Infect Dis. 2024;24(5):270-1.
Paludismo (malaria)
- Daily JP, et al. Malaria. N Engl J Med. 2025;392:1320-33.
- Ngou P, et al. R21/Matrix-M malaria vaccine: a vital tool in the arsenal against malaria, not a silver bullet. Lancet Infect Dis. 2024;24(5):438-9.
- Schmit N, et al. The public health impact and cost-effectiveness of the R21/Matrix-M malaria vaccine: a mathematical modelling study. Lancet Infect Dis. 2024;24(5):465-75.
[volver al principio]








