COVID-19
1. INTRODUCCIÓN
• En diciembre de 2019, China informó de un acúmulo de pacientes ingresados por brote de neumonías y síndrome respiratorio agudo grave (SARS) en Wuhan, provincia de Hubei, por un microorganismo desconocido que, posteriormente fue identificado como un nuevo coronavirus (SARS-CoV-2).
• La rápida expansión global del virus hizo que la Organización Mundial de la Salud (OMS) considerara la situación mundial debida a este virus como pandemia el 11 marzo de 2020. El 5 de mayo de 2023, más de tres años después, se declaró el fin de la emergencia de salud pública de interés internacional.
• La vía principal de contagio es la inhalación de las gotas y aerosoles respiratorios emitidos por una persona infectada, incluso si esta se encuentra asintomática.
• El cuadro clínico varía desde síntomas leves (o ausentes) como un cuadro de infección de vías respiratorias altas hasta cuadros más graves como neumonía con síndrome de distrés respiratorio, shock séptico y fallo multiorgánico.
• Los niños desarrollan formas de la enfermedad menos graves que los adultos y presentan en general mucho mejor pronóstico que estos.
• Se ha descrito un síndrome inflamatorio multisistémico pediátrico vinculado temporalmente a la infección por SARS-CoV-2 que podría ser una respuesta inflamatoria tardía a la infección, y que, aunque muy poco frecuente (especialmente con las variantes virales actualmente circulantes), comporta una mayor gravedad.
[volver al principio]
2. EL PATÓGENO
• Los coronavirus pertenecen a familia Coronaviridae, subfamilia Orthocoronavirinae. Su nombre deriva de la imagen del virus por microscopía electrónica, en la que pueden observarse unas espículas que sobresalen de la envoltura vírica y que le dan aspecto de corona solar.
• Pueden infectar los sistemas respiratorio, gastrointestinal, hepático y nervioso central de humanos, ganado, aves, murciélagos, ratones y otros animales salvajes. Antes de transmitirse fácilmente entre humanos han de dar el llamado “salto de especie”, acumulando las mutaciones necesarias que los hagan pasar de un hospedador animal al humano pasando por un hospedador intermediario. En el caso del síndrome respiratorio agudo grave (SARS) en 2003, producido por SARS-CoV, el hospedador del que se produjo el salto de especie fue la civeta, mientras que el dromedario lo fue para el síndrome respiratorio de Oriente Medio (MERS-CoV) en 2013. Los estudios filogenéticos del SARS-CoV-2 apuntan a que muy probablemente el virus provenga de murciélagos (88·% de similitud con dos coronavirus aislados de murciélagos en 2018) y que de allí haya pasado al ser humano a través de mutaciones o recombinaciones sufridas en un hospedador intermediario, probablemente algún animal vivo del mercado de Wuhan. La hipótesis de un origen accidental o intencionado asociado a la actividad de algún laboratorio es muy poco probable.
• Los coronavirus que afectan al ser humano pertenecen a dos géneros diferentes: Alphacoronavirus (HCoV-229E, CoV-NL63) y Betacoronavirus (HCoV-OC43, HCoV-HKU1, SARS-CoV-1, MERS-CoV y SARS-CoV-2). SARS-CoV-2 presenta una similitud genómica de un 79 % con SARS-CoV-1 y de un 50 % con MERS-CoV.
• Son los responsables de cuadros clínicos que van desde la neumonía o síndrome respiratorio agudo grave, causadas por los SARS-CoV-1 o por MERS-CoV, a cuadros leves como el resfriado común y conjuntivitis, causado por el resto de los coronavirus y que suponen el 15-30 % de todos los resfriados.
• Son virus esféricos de 100-160 nm de diámetro. Su estructura consiste en una nucleocápside y en una envoltura externa. La nucleocápside protege al material genético viral, que incluye una única molécula de ARN simple de sentido positivo de aproximadamente 30 000 pares de bases. Al ARN se encuentran unidas múltiples copias de la proteína de la nucleocápside (proteína N). En la envoltura externa se insertan proteínas estructurales denominadas E (envoltura), M (membrana) y S (del inglés spike, o espícula), además de otras proteínas accesorias como la hemaglutinina esterasa (HE). La proteína E juega un papel importante en el ensamblaje y liberación del virus, la proteína M ayuda a mantener la curvatura y conformación de la membrana y la unión con la nucleocápside, y la proteína S facilita la unión del virus al receptor de la célula huésped.
• La proteína S del SARS-CoV-2 posee dos subunidades (S1 y S2). La subunidad S1 es la que interacciona, a través del dominio de unión al receptor (RBD), con los receptores de la enzima convertidora de la angiotensina 2 (ACE2) ubicados en las membranas celulares del huésped, especialmente en las células epiteliales alveolares pulmonares y en enterocitos del intestino delgado, aunque también en otras localizaciones como en las células endoteliales y en las del músculo liso arterial de órganos como el corazón y el riñón. La subunidad S2 es la que determina la fusión de la membrana del virus con la de la célula huésped, tras la que los coronavirus pasan por endocitosis al citoplasma, donde la nucleocápside del virus se libera y permite la salida del ARN genómico viral, que será procesado por los ribosomas como si fuera ARNm propio, sintetizando por un lado nuevas copias de ARN viral (que se asociará de nuevo a la proteína N formando una nueva nucleocápside). En las membranas del retículo endoplasmático el ARN viral se traduce en la síntesis de nuevas proteínas estructurales, que serán transportadas al complejo de Golgi donde se ensamblarán a la nucleocápside formándose las nuevas partículas virales. Finalmente, las vesículas que contienen los nuevos viriones se fusionan con la membrana celular para liberar los virus al exterior de la célula mediante exocitosis.
[volver al principio]
3. EPIDEMIOLOGÍA Y TRANSMISIÓN
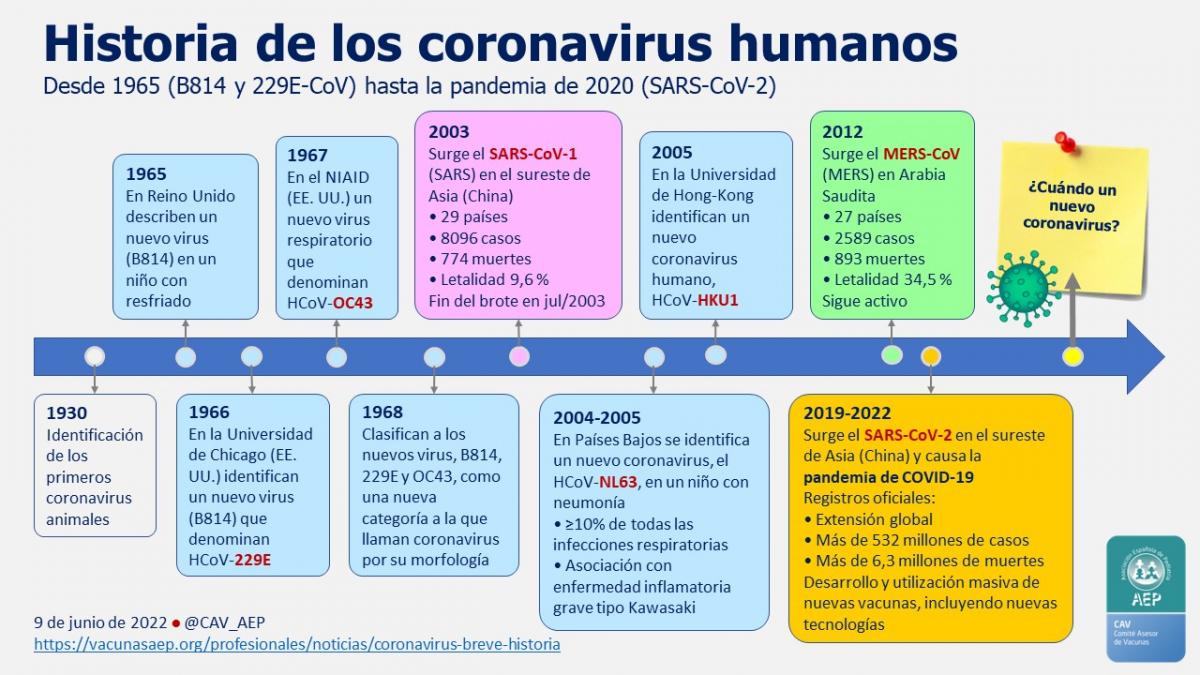
• En 2003 se describió un coronavirus (SARS-CoV-1) como el causante del brote del llamado síndrome respiratorio agudo severo (SARS) en la provincia de Guangdong (China), y que se distribuyó a los 5 continentes a través de rutas aéreas infectando a algo más de 8000 personas y causando 774 muertes. En 2012 emergió otro coronavirus en la península arábiga (MERS-CoV), exportado a 27 países, que ha causado aproximadamente 2500 infecciones con una letalidad del 30-40 %; este brote no está cerrado, pero los casos en los últimos años están confinados en la península arábiga. En diciembre de 2019, se alertó desde China por un brote de neumonía y SARS en Wuhan, provincia de Hubei. El 7 de enero de 2020, identificaron a un nuevo coronavirus (llamado inicialmente 2019-nCoV) como su causa, y 5 días más tarde China compartió el genoma del coronavirus con el resto del mundo. El 2 de marzo el International Committee on Taxonomy of Viruses (ICTV) denomina al nuevo coronavirus como SARS-CoV-2. A la infección producida por este se la denominó COVID-19.
• La OMS, el 30 enero de 2020, declaró la "emergencia de salud pública de interés internacional“ (ESPII) y el 11 marzo la consideró como pandemia. En mayo de 2023, la misma OMS dejó de considerar a la COVID-19 como una ESPII.
• El periodo de incubación es variable, pero generalmente dura de 2 a 7 días. Se estima que aproximadamente entre el 7 % y el 10 % de los casos progresan a enfermedad grave, y que la tasa de letalidad pueda estar entre 1·% y 3 %, aunque estas tasas varían dependiendo de la edad y las comorbilidades de los pacientes y de la ubicación geográfica.
• En personas con síntomas leves, más allá de la primera semana tras el inicio de síntomas, la probabilidad de transmisión de la infección a otros sería muy baja, incluso cuando el material viral aún es detectable mediante PCR. En personas con un curso clínico más grave la carga viral es de hasta 60 veces mayor que las que tienen un curso más leve y puede mantenerse detectable de forma más duradera. Se desconoce si la intensidad de la transmisión a partir de personas asintomáticas es igual que desde personas con síntomas, aunque la carga viral detectada en los casos asintomáticos es similar a la de otros casos sintomáticos.
• Los niños y adolescentes se infectan en una proporción similar a la de otras edades. La población pediátrica, en base a la evidencia actual disponible, parece presentar una menor capacidad de trasmisión respecto a los adultos, a pesar de haberse descrito una carga viral similar e incluso mayor en los menores de 5 años. El predominio de cuadros asintomáticos y formas leves de la enfermedad con menos tos y menor vehiculización de aerosoles parecen respaldar esta menor capacidad infectiva. La transmisión entre niños parece ser menos eficiente que para otras infecciones respiratorias como, por ejemplo, la gripe. La mayor probabilidad de contagio entre los niños ocurre en sus hogares, siendo menos probable en los centros educativos cuando se han mantenido medidas como la distancia interpersonal, higiénicas como lavado de manos y uso de mascarillas en interiores.
• Con la evidencia científica acumulada, se considera que el SARS-CoV-2 puede transmitirse de persona a persona por diferentes vías, siendo la principal la inhalación de las gotas y aerosoles respiratorios emitidos por un enfermo hasta las vías respiratorias superiores e inferiores de una persona susceptible. También se puede producir el contagio por contacto indirecto a través de las manos u objetos contaminados por las secreciones respiratorias del enfermo con las mucosas de las vías respiratorias y la conjuntiva del susceptible. La transmisión vertical a través de la placenta también podría ser posible, aunque prácticamente no se han descrito casos. En leche materna se ha encontrada ARN del virus, pero no virus viables. Otras vías de transmisión (heces, orina, semen, sangre y hemoderivados) son muy improbables.
• Respecto a la transmisión por gotas y aerosoles, recientemente se ha demostrado la viabilidad del virus en el aire, en condiciones experimentales, durante, al menos, 16 horas, en las que además se mantiene con la misma carga viral. Los virus contenidos en los aerosoles tienen capacidad de generar infección sobre todo si el tiempo de exposición ha sido mayor de 15 minutos, en espacios cerrados y mal ventilados, y sin el uso mascarilla o con una mascarilla no adecuada o mal utilizada, aunque el riesgo puede estar relacionado además con la carga viral de la persona infectada.
• Respecto a la transmisión por fómites, en entornos donde hay enfermos de covid, el virus SARS-CoV-2 se ha encontrado en las superficies inanimadas en la cercanía de los enfermos (cama, baños, pomos ...), tanto en entornos hospitalarios como en los domicilios de los pacientes, aunque no se ha logrado cultivar. Tras los procesos habituales de desinfección el material genético del virus se detecta en pocas ocasiones, y cuando se ha detectado no se ha logrado cultivar, lo que en principio apunta a una ausencia de viabilidad, lo que supone que, con los métodos de limpieza recomendados, la transmisión mediante fómites sería muy poco probable. Hasta el momento no se ha descrito ningún caso por transmisión exclusiva a través de fómites.
• La infección natural por SARS-CoV-2 da lugar a una respuesta inmune humoral, con anticuerpos neutralizantes, y celular. A día de hoy se desconoce con precisión cuánto tiempo se mantienen esos anticuerpos y cuál es el nivel que se considera protector. La reinfección es frecuente. La inmunidad celular, implicada en la protección frente a la enfermedad pulmonar grave, parece ser duradera, sin embargo, la irrupción de variantes virales nuevas puede reducir la efectividad de la inmunidad adquirida tras infecciones anteriores. La inmunidad adquirida por el sumatorio de la vacunación y la infección natural proporciona la mejor protección conocida, tanto humoral como celular. Dicha respuesta ha recibido el nombre de inmunidad híbrida.
[volver al principio]
4. CLÍNICA Y COMPLICACIONES
• Los niños desarrollan formas de la enfermedad menos graves que los adultos y presentan, en general, mucho mejor pronóstico que estos. Según datos de una revisión sistemática, solamente un 47,5 % presentaron fiebre y alrededor de la mitad fueron leves o asintomáticos. Entre los casos de mayor gravedad, con los datos publicados hasta la fecha, los menores de 1 año y los mayores de 10 años representan la población pediátrica con mayor riesgo de desarrollar una enfermedad moderada-grave. Se ha descrito un síndrome inflamatorio multisistémico pediátrico vinculado temporalmente a la infección por SARS-CoV-2 (conocido con las siglas SIMP, SIM-PedS o PIMS) que podría ser una respuesta inflamatoria tardía a la infección, qué, aunque poco frecuente, comporta una mayor gravedad y precisa en un alto porcentaje de ingreso en unidades de cuidados intensivos pediátricas (UCIP). La incidencia del SIMP es de alrededor de un 90 % menor con la variante ómicron que con las variantes anteriores. En la actualidad, la mayoría de los casos pediátricos que ingresan en cuidados intensivos o fallecen presentan algún factor de riesgo definido (cardiopatía, asma bronquial, obesidad, enfermedad hepática, neuromuscular, oncológica o inmunológica).
• Según datos del “Estudio epidemiológico de las infecciones pediátricas por el nuevo coronavirus SARS-CoV-2. EPICO-AEP” en el que han participado 92 hospitales pediátricos, a fecha de 22 de diciembre de 2021, se habían incluido 1443 niños hospitalizados con covid (mediana de edad: 5,1 años), y de ellos 521 (36 %) necesitaron cuidados intensivos. En un informe del 25 de mayo de 2021, se incluían 743 niños (sexo femenino 55,7 %, mediana de edad 5,9 años), y de ellos, 176 (23,7 %) presentaron clínica broncopulmonar, síntomas gastrointestinales 9,7 %, fiebre sin foco 15,4 %, SIMP 18,7 % y manifestaciones leves en el 32,4 %. El 32,2 % presentaba comorbilidades preexistentes.
• En otro estudio multicéntrico en el que incluyeron datos provenientes de 47 unidades de cuidados intensivos españolas se determinó que la principal causa de ingreso en críticos por covid se debía al padecimiento de SIMP (durante el primer año de circulación del virus en nuestro país) y que los pacientes que lo padecían eran mayoritariamente sanos previamente, con una edad media superior respecto a los que no padecían SIMP y además presentaban con frecuencia sintomatología cutáneo-mucosa, gastrointestinal y hemodinámica.
[volver al principio]
5. PREVENCIÓN
• Las medidas higiénicas recomendadas por el Ministerio de Sanidad y los servicios de Salud Pública de las comunidades autónomas para la prevención de contagios de la covid incluyen el lavado de manos (priorizando el lavado con agua y jabón sobre el uso de geles hidroalcohólicos), la limpieza y desinfección de superficies, la ventilación de espacios cerrados, el uso de mascarilla en determinados contextos, el aumento de la distancia física interpersonal y la reducción del tiempo de contacto entre personas.
• La Agencia Europea de Medicamentos ha autorizado el uso de algunas vacunas frente a la covid en los países europeos para su distribución mediante un procedimiento centralizado y hay cuatro autorizadas en menores de 18 años: Comirnaty (BioNTech & Pfizer) y Spikevax (Moderna), ambas de ARNm, y para la inmunización de niños desde los 6 meses de edad y mayores, Nuvaxovid (Novavax) para adolescentes a partir de los 12 años y Bimervax (Hipra) para adolescentes a partir de los 16 años.
• A partir de 2023 se ha redefinido la estrategia de vacunación contra la covid, pues tras la expansión poblacional de ómicron el foco ha de ponerse especialmente en proteger a la población más susceptible. En lo que se refiere a la vacunación en menores de 18 años, se recomienda para aquellos que tengan factores de riesgo (definidos en la estrategia ministerial) o sean convivientes de personas con riesgo incrementado. Pese a que la vacunación de niños sanos deja de ser actualmente una prioridad a nivel mundial, en la hoja de ruta del WHO-SAGE de 03/2023 se deja la puerta abierta a vacunarlos, según las prioridades del sistema de salud de cada país.
• Las vacunas se han ido adaptando a las variantes o linajes circulantes (actualmente predominan los sublinajes de ómicron JN.1: LP8.1. y KP.2) y así lo harán en cada temporada otoño-invierno, evitándose la vacunación de la población (especialmente la que no ha tenido nunca contacto con el virus) con preparados que contengan variantes del virus que no estén circulando en ese momento, siguiendo una política similar a la de la gripe. En la actualidad se recomienda la administración de una dosis única en mayores de 5 años independientemente de si han sido previamente vacunados o no o si han padecido la enfermedad o no. Los de edades comprendidas entre los 6 meses y los 5 años recibirán una pauta completa (de 2 o 3 dosis según el preparado utilizado) si nunca han sido vacunados ni han padecido la enfermedad y solo una dosis si ya han tenido contacto con el virus o han recibido alguna dosis de vacuna. Los pacientes de muy alto riesgo deberán recibir una dosis extra en su pauta vacunal contra la covid.
Ir al capítulo de la vacuna del SARS-CoV-2 en el Manual de Inmunizaciones en Línea de la AEP.
[volver al principio]
6. TRATAMIENTO
• En la actualidad, el único tratamiento antiviral autorizado en España para población pediátrica con covid grave es el remdesivir. Existe un antiviral de administración oral (nirmatrelvir/ritonavir) indicado en poblaciones especialmente susceptibles que, si bien la FDA lo ha autorizado por encima de los 12 años, la EMA fija la edad mínima para su uso en los 18. La administración en menores de esa edad requeriría de una solicitud de uso compasivo. Conforme ha ido avanzado la pandemia y los distintas variantes han ido circulando, se han desarrollado anticuerpos monoclonales específicos que, como consecuencia de la capacidad de mutar del SARS-CoV-2 se han ido quedando inutilizables.
• En este enlace, correspondiente a la AEMPS, se recogen las últimas novedades referidas a la prevención y tratamiento sujetos a condiciones especiales de acceso por motivos diversos (medicamento en investigación no comercializado, restricciones de suministro, etc.).
[volver al principio]
7. BIBLIOGRAFÍA
- AEMPS, Agencia Española de Medicamentos y Productos Sanitarios. Últimas noticias
- ANDAVAC, Plan Estratégico de Vacunaciones de la Consejería de Salud y Familias de la Junta de Andalucía. Vacunación COVID-19.
- Centers for Disease Control and Prevention. Healthcare Workers: Information on COVID-19
- Centers for Disease Control and Prevention. COVID-19 Vaccination Clinical & Professional Resources
- Centers for Disease Control and Prevention. Appendix: Vaccine Administration Errors and Deviations
- Centers for Disease Control and Prevention. ACIP Vaccine Recommendations and Guidelines
- Centro Nacional de Epidemiología (CNE), Instituto de Salud Carlos III. Informes Covid-19
- Comité Asesor de Vacunas e Inmunizaciones de la AEP (CAV-AEP). Fichas técnicas de las vacunas de la covid-19 disponibles en España
- Comité Asesor de Vacunas e Inmunizaciones de la AEP (CAV-AEP). Calendario de Vacunaciones e Inmunizaciones de la Asociación Española de Pediatría. Razones y bases de las recomendaciones 2026. [Internet]. Madrid: AEP; 2026.
- Comité Asesor de Vacunas e Inmunizaciones de la AEP (CAV-AEP). Noticias sobre el SARS-CoV-2 y sus vacunas
- Comité Asesor de Vacunas e Inmunizaciones de la AEP (CAV-AEP). Vacunación de las embarazadas contra la covid
- Comité Asesor de Vacunas e Inmunizaciones de la AEP (CAV-AEP). Vacunación frente a la covid en el embarazo y lactancia materna: recopilación de referencias bibliográficas (actualizado a julio de 2024)
- Comité Asesor de Vacunas e Inmunizaciones de la AEP (CAV-AEP). Preguntas frecuentes sobre la vacunación frente al coronavirus
- Comité Asesor de Vacunas e Inmunizaciones de la AEP (CAV-AEP). Enfermedades inmunoprevenibles. COVID-19
- Comité Asesor de Vacunas e Inmunizaciones de la AEP (CAV-AEP). Las vacunas una a una... y un anticuerpo. Información para familias. Vacuna de la COVID-19.
- Comité Asesor de Vacunas e Inmunizaciones de la AEP (CAV-AEP). Manual de inmunizaciones en línea. Virus SARS-CoV-2, actualizado en agosto de 2025.
- ECDC, European Centre for Disease Prevention and Control. COVID-19
- ECDC, European Centre for Disease Prevention and Control. COVID-19 Vaccine Tracker
- ISCIII, Instituto de Salud Carlos III. COVID-19 en España
- Johns Hopkins University. Coronavirus Resource Center. Covid-19 Dashboard
- LSHTM, London School of Hygiene & Tropical Medicine. COVID-19 vaccine tracker
- Ministerio de Sanidad. Vacunación COVID-19 - Profesionales sanitarios
- Ministerio de Sanidad. Vacunación frente a gripe y COVID-19 en la temporada 2025-2026. Preguntas y respuestas sobre vacunación frente a COVID-19. 23 de julio de 2025.
- Ministerio de Sanidad. Gobierno de España. Ponencia de Programa y Registro de Vacunaciones. Recomendaciones de vacunación frente a COVID-19 en la temporada 2025-2026 en España 3 de julio de 2025.
- PHE, Public Health England. Green Book. Cap. 14a. COVID-19.
- The New York Times. Coronavirus Vaccine Tracker
- World Health Organization. Coronavirus (COVID-19) Dashboard
- World Health Organization. Coronavirus disease (COVID-19) Weekly Epidemiological Updates and Monthly Operational Updates
- World Health Organization. Coronavirus disease (COVID-19) pandemic
- World Health Organization. COVID-19 vaccine tracker and landscape
- World Health Organization. COVID-19 vaccines
- World Health Organization. Enfermedad por el coronavirus (COVID-19): Vacunas y seguridad de las vacunas
- World Health Organization. Statement on the antigen composition of COVID-19 vaccines. 15 May 2025.
- World Health Organization. Statement on the fifteenth meeting of the IHR (2005) Emergency Committee on the COVID-19 pandemic. 5 May 2023.
- World Health Organization. WHO SAGE Roadmap for prioritizing uses of COVID-19 vaccines. November 2023.
[volver al principio]