Para evitar confusiones, le informamos de que ESTE NO ES el formulario para enviar PREGUNTAS SOBRE VACUNAS al comité. Si esa fuera su intención, diríjase a la sección de preguntas de profesionales o de preguntas de familias.
A través de este formulario, el responsable del mismo, la Asociación Española de Pediatría (AEP) y su Comité Asesor de Vacunas, recaba los datos necesarios para gestionar el envío de sus comentarios y sugerencias sobre el Manual de Inmunizaciones en línea de la AEP, que ponemos a su disposición en nuestra página web.
Los campos marcados con asterisco son obligatorios y, sin ellos, no se tramitará su comentario o sugerencia.
Este tratamiento de datos no puede realizarse sin su consentimiento, por lo que deberá validar la casilla de protección de datos antes de enviar la consulta.
Sus datos no serán cedidos a otras entidades, ni transmitidos a otros países. Tiene derecho a acceder, rectificar y suprimir los datos, así como otros derechos, como se explica en la información común a los tratamientos que efectúa la AEP.
Puede consultar la información detallada sobre protección de datos, así como la información común a los tratamientos que efectúa la AEP.
46. Aspectos legales de las inmunizaciones
CAPÍTULO 46 - Aspectos legales de las inmunizaciones
1.1. Las vacunas están catalogadas legalmente como medicamentos especiales
1.2. ¿Cuáles son los procedimientos de autorización de las vacunas en España?
1.3. ¿Cuáles son las vías rápidas aprobadas por la EMA para la autorización de las vacunas para prevenir la COVID-19?
1.4. ¿Cuál es el papel de la AEMPS en relación de las vacunas para prevenir la COVID-19?
2.1. ¿En qué casos se puede imponer la vacunación con carácter obligatorio?
2.1.1. Normativa de salud pública
2.1.2. Normativa básica en materia de información y consentimiento
2.1.3. El debate social sobre la obligatoriedad de las vacunas
2.2. ¿Cuál es el procedimiento administrativo y judicial para imponer la vacunación obligatoria?
2.3. ¿En qué supuestos vienen exigiendo nuestros juzgados y tribunales la vacunación obligatoria?
2.4. Si un profesional sanitario trabaja en unidades de riesgo, por ejemplo con inmunodeprimidos, ¿puede ser obligado a vacunarse? ¿En caso de no vacunarse, se le puede impedir al profesional sanitario el acceso a ese puesto de trabajo?
3.1. ¿Quién debe informar sobre las vacunas pediátricas a los padres? ¿Es válido el prospecto a estos efectos?
3.2. ¿Debe el equipo pediátrico exigir que los padres o representantes legales de un menor firmen un documento de consentimiento informado para la vacunación?
3.3. ¿La mera visita de los padres o representantes legales al centro de vacunación puede entenderse como que se presta el consentimiento?
3.4. ¿Es válida la autorización verbal de padres o representantes legales para la vacunación, o se precisa consentimiento informado por escrito?
3.5. ¿Hasta qué edad es preciso que los padres o representantes legales autoricen la vacunación de los hijos o representados? Catálogo de situaciones
3.5.1. ¿Los padres pueden negarse a vacunar a sus hijos?
3.5.2. Edad, madurez, consentimiento y representación en materia vacunal. ¿Todos los menores de edad están en la misma situación? (menores maduros y mayores de dieciséis años cumplidos)
3.5.3. El ejercicio de la representación en menores. El “interés superior del menor” como canon de constitucionalidad
3.6.1. Consentimiento por representación y patria potestad
3.6.2. La casuística entre los progenitores respecto a la vacunación de sus hijos menores
3.6.3. Breve referencia a las reglas de la patria potestad y consentimiento en el caso de menores con discapacidad tras la Ley 8/2021, de 2 de junio, por la que se reforma la legislación civil y procesal para el apoyo a las personas con discapacidad en el ejercicio de su capacidad jurídica.(BOE núm. 132, de 03/06/2021)
4.1. ¿Deben firmar algún documento los padres o tutores que se nieguen a vacunar a sus hijos?
4.2. ¿Puede un menor de edad negarse a la vacunación?
4.3. En el caso de personas que se niegan a vacunarse (o que rechazan la vacunación de sus hijos o representados), ¿pueden recaer en algún tipo de responsabilidad legal si enferman?
4.4. ¿Podrían los hijos reclamar a sus padres por la vida enferma derivada de la negativa de éstos a la vacunación?
5.1. ¿Quiénes pueden prescribir medicamentos sujetos a prescripción médica?
5.2. Régimen de prescripción de las vacunas como medicamento especial
5.3. La receta médica como instrumento de prescripción
5.4. Las vacunas deben prescribirse obligatoriamente por denominación comercial
5.5. ¿Es necesaria una receta para cada dosis o se pueden prescribir varias dosis en una misma receta?
6.1. Sustituibilidad de la prescripción médica por el farmacéutico
6.2. La prescripción médica de la vacuna no es sustituible por el farmacéutico
- Administración de vacunas por el personal de enfermería
- Responsabilidad patrimonial de la Administración
8.1. ¿Cuál es la responsabilidad de la Administración sanitaria en relación con las vacunas?
9.1. En el caso de que un pediatra del sistema público prescriba una vacuna no incluida en el calendario vacunal. ¿Está obligado el enfermero del sistema público a administrarla?
9.2. ¿Cuál es el riesgo legal del profesional si tras la administración de una vacuna no incluida en el calendario oficial aparece una reacción adversa?
9.3. ¿Cuál es la responsabilidad legal del pediatra si recomendó no vacunar frente a una determinada enfermedad y posteriormente el paciente la desarrolla?
9.4. ¿Qué responsabilidad asume el profesional sanitario que inyecta suero en lugar de la vacuna?
10.1. Tras la aprobación del calendario único por parte del Ministerio de Sanidad en 2013, con una última actualización en 2024 en el Calendario para toda la vida, ¿puede una Comunidad Autónoma modificarlo o debe respetarlo salvo que concurran razones epidemiológicas?
10.2. ¿Cuáles son los límites legales que tiene un pediatra para prescribir una vacuna fuera de calendario?
10.3. Libertad de prescripción en relación con la ficha técnica del medicamento
10.4. Libertad de prescripción en relación con el calendario común de vacunación
11.1. Si los padres consultan sobre la compra de vacunas no disponibles en nuestro país, ¿cuál debe ser la recomendación del profesional, desde un punto de vista legal?
11.2. La compra de vacunas por internet
11.3. La compra de vacunas en oficinas de farmacia de países limítrofes
- Bibliografía
- Enlaces de interés
- Historial de actualizaciones
- Tablas y figura incluidas en el capítulo:
Tabla 46.1. El Derecho como herramienta de seguridad en todas las etapas de la inmunización
Tabla 46.2. El consentimiento informado en función de la edad del menor
Tabla 46.3. Tabla de posibles situaciones en relación con el consentimiento de los menores de edad y sus padres
Tabla 46.4. Situación legal de la prescripción de vacunas
Tabla 46.5. Criterios de prescripción, validez de la receta y duración del tratamiento
Tabla 46.6. Asignación de tareas de vacunación a los profesionales sanitarios
Tabla 46.7. Medicamentos sujetos y no sujetos a prescripción médica. Tipología de prescripciones
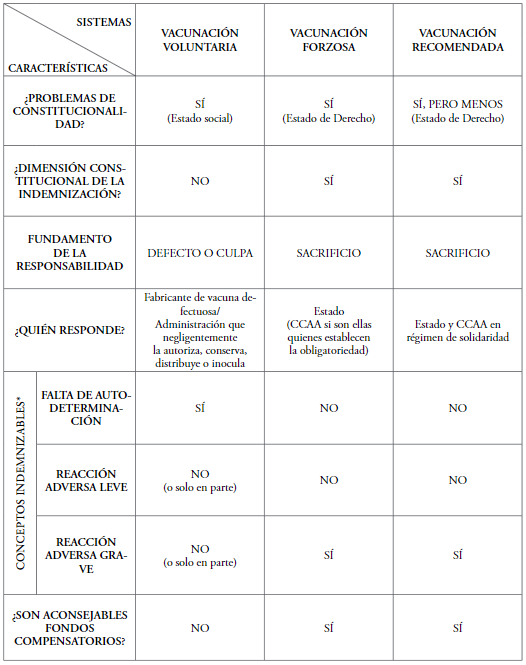
Figura 46.1. Resumen de la responsabilidad patrimonial por reacción adversa a la vacunación
Sugerencia para la citación: Comité Asesor de Vacunas e Inmunizaciones (CAV-AEP). Aspectos legales de las inmunizaciones. Manual de inmunizaciones en línea de la AEP [Internet]. Madrid: AEP; ene/2022. [consultado el dd/mmm/aaaa]. Disponible en: http://vacunasaep.org/documentos/manual/cap-46
0. A MODO DE INTRODUCCIÓN
Debates jurídicos de la vacunación, situación de la duda vacunal y la evolución de las potencialidades de las vacunas (de la vacunación a la inmunización: los nuevos anticuerpos monoclonales o las vacunas contra el cáncer)
El debate sobre la obligatoriedad de la vacunación y la duda vacunal a raíz de la pandemia
El fenómeno de la vacunación presenta, junto a los aspectos puramente médicos y científicos —cuyo análisis no nos corresponde en el presente capítulo—, otras cuestiones que son del máximo interés, tales como la consideración de las vacunas como uno de los instrumentos más eficaces de las políticas de salud pública, así como la permanente controversia sobre los riesgos de la vacunación y la voluntariedad u obligatoriedad de las vacunas.
En la situación de la pandemia por la COVID-191, la polémica se vio magnificada ante la extrema gravedad de la situación epidemiológica a nivel global, siendo las vacunas la principal herramienta para superar la crisis sanitaria y social en la que el coronavirus SARS-CoV-2 sumió a todo el planeta.
Aunque el debate social sobre la conveniencia o no de la vacunación tampoco es nuevo2, lo cierto es que se ha reavivado a nivel social, médico y jurídico. Primero con el procedimiento de aprobación de las primeras vacunas para prevenir la COVID-19, los problemas logísticos y las disfunciones en las fases iniciales de las campañas de inmunización de la población. Seguido de las posturas contrarias —o cuando menos escépticas— a la vacuna de la Covid, a cargo del Dr. Cavadas, Miguel Bosé, Victoria Abril o, a nivel colectivo, del llamado movimiento antivacunas. Después con las dudas sobre la seguridad de las vacunas covid y sus efectos adversos3. Lo cierto es que en determinados momentos ha existido cierta sobrecarga informativa y cierta infodemia e infoxicación sobre las vacunas, sus dosis, los momentos óptimos de administración según colectivo, otras medidas de salud pública, etc. llevando a la población a una especie de agotamiento pandémico.
El éxito de las vacunas y la práctica eliminación de las enfermedades infecciosas, que en otras épocas asolaron a la población infantil, determinan que los padres tengan una percepción de riesgo muy bajo si no vacunan a sus hijos (por la protección que dispensa la protección de grupo) y teman por los riesgos asociados a la vacunación (pese a que los mismos, tales como el autismo, se ha demostrado que carecen de base científica)4. Sin embargo, cuando sube la percepción del riesgo de la enfermedad, las tasas de vacunación se disparan, tal y como ocurrió en Cataluña, donde las tasas de vacunación de difteria, tras el contagio y posterior fallecimiento del niño en 2015, se elevaron un 23 %5.
Este fenómeno también se observa en la pandemia de la COVID-19, donde el grupo que afirmaba que no se pondría la vacuna bajó del 47 % (noviembre de 2020) a un 28 % (enero de 2021)6; Los datos actualizados a 1 de abril de 2023, reflejan que la campaña de vacunación, incluyendo las dosis de recuerdo y actualizaciones han sido un éxito, como refleja el Informe de actividad GIV-19 (Gestión Integral de la Vacunación)7: el 92,6 % de la población mayor de 12 años tiene la pauta completa de vacunación. Aunque es cierto que la cobertura de población pediátrica (de 5 a 12 años) desciende considerablemente (47,5 % con pauta completa); ello aun con las dudas generadas sobre los posibles efectos adversos de la vacuna de AstraZeneca y la publicación actualizada de las ratios de esta y el resto de vacunas, ejemplo de transparencia que ha logrado superar el desplome en la confianza surgido a raíz de aquel hecho8, así como de algún episodio que quedó en mera anécdota, como el de la combinación de vacunas9.
Esta controversia social tiene su proyección legal, fundamentalmente en términos de voluntariedad versus obligatoriedad, con la necesidad de proteger derechos fundamentales tales como el derecho a la salud, a la integridad física o la libertad personal, la renuncia a la vacunación, los problemas que surgen en el consentimiento por representación de los menores (especialmente conflictivo, como veremos en el análisis jurisprudencial); posibles responsabilidades derivadas de la vacunación; estas y otras cuestiones son objeto de análisis en el presente capítulo.
El Derecho como herramienta para mejorar la seguridad del paciente en todas las fases de la inmunización
| El Derecho debe adaptarse a los avances científicos en materia de inmunización; a corto plazo habría que simplificar el entorno regulatorio |
En este punto, frente a lo que se pudiera pensar por la mayoría de los profesionales sanitarios, el Derecho no se presenta como una normativa que suponga un obstáculo en todas las etapas de la inmunización, sino como una herramienta eficaz, que mejora la seguridad del proceso de inmunización en beneficio de todos: de los niños, de los profesionales, de las autoridades sanitarias y de la sociedad en su conjunto (tabla 46.1).
Tabla 46.1. El Derecho como herramienta de seguridad en todas las etapas de la inmunización.
| Información | Todos los profesionales sanitarios | Financiadas: consecuencias leves y riesgos típicos | Financiadas |
| No financiadas: riesgos graves e infrecuentes | No financiadas | ||
| Prescripción | Médico | Por denominación comercial | No financiadas |
| Enfermería | Orden de dispensación | Financiadas y campañas vacunales | |
| Dispensación | Faramaceútico | La vacuna indicada en la receta por denominación comercial | No fianciadas |
| Centro de vacunación | Orden de dispensación enfermera | Financiadas y campañas vacunales | |
| Administración | Enfermería | Conforme a las advertencias del prescriptor, velando porque se administra la vacuna prescrita, en centro autorizado | Financiadas/No financiadas |
Fuente: elaboración propia.
Por otro lado, se ha abierto una senda nueva en los tipos de inmunización, desde los nuevos modelos de vacunas ARN mensajero, a los anticuerpos monoclonales, que sugieren cambios también desde el punto de vista jurídico, tanto en el procedimiento regulatorio, como incluso en su consideración como vacuna o medicamento. En este proceso de evolución científica, habrá que discernir si los cambios en estos modelos de inmunización supondrían aplicar reglas distintas tanto para su autorización como para su evaluación y administración, estando por determinar si se atribuirán las funciones clásicas en materia de vacunación a la Ponencia de Vacunas, o si el procedimiento debería ser el de Informe de Posicionamiento Terapéutico, que es el común en medicamentos innovadores.
Por la información actual de la AEMPS, cuando la situación epidemiológica es menos compleja y existe disponibilidad de diferentes tratamientos frente a la COVID-19 que ya están comercializados y, en algunos casos, incluso se han adquirido a través de compras centralizadas europeas, parece haberse optado por un modelo mixto, teniendo en cuenta los criterios establecidos en la normativa sobre administración de medicamentos en situaciones especiales. En 2022 se estableció un esquema de intervención y priorización de tratamientos por parte de la AEMPS, que ya no es necesaria. Corresponde al médico, dentro de la práctica clínica habitual, decidir la opción más adecuada atendiendo a las características y especificidades de su paciente, de acuerdo con la ficha técnica o las instrucciones de los distintos comités sanitarios a nivel autonómico u hospitalario. Para el uso de los medicamentos para prevención mediante inmunización pasiva se deben seguir las recomendaciones emitidas por la Comisión de Salud Pública, a propuesta de la Ponencia de Programa y Registro de Vacunaciones10.
En cuanto a las primeras, las vacunas ARNm, aunque se están investigando y desarrollando desde hace décadas, se trata de un nuevo tipo de vacunas, principalmente porque no contienen virus vivos. En cambio, estas vacunas les enseñan a nuestras células a producir una porción inocua de la “proteína S” que está presente en la superficie del virus que causa la COVID-19. Después de producirla, las células muestran esta porción de proteína creada sobre su superficie. Nuestro sistema inmunitario reconoce que la proteína es un cuerpo extraño y comienza a generar una respuesta inmunitaria para deshacerse de ella. Cuando se comienza a generar la respuesta inmunitaria, se crean anticuerpos que desencadenan la misma respuesta producida por una infección natural.
A diferencia de las vacunas de ARNm, muchas otras vacunas utilizan una porción, o una versión atenuada, del microbio que la vacuna combate. Así funcionan las vacunas contra la gripe y el sarampión. Cuando se introduce una parte pequeña o debilitada del virus en nuestro organismo, se generan anticuerpos para ayudar a protegerlo de futuras infecciones11.
La expansión de vacunas covid utilizando esta u otras técnicas nos obliga a seguir refiriéndonos a ellas, en tanto pueden llevar a un modelo de vacunación avanzada, y también porque el listado de vacunas se va actualizando día a día, como veremos posteriormente, produciéndose distintos modelos de autorización y revirtiendo las anteriores autorizaciones condicionales al modelo regular de autorización.
Pero quizás la mayor novedad está en la evolución científica respecto al uso de anticuerpos monoclonoles, sin duda el futuro de la inmunización frente a determinadas patologías. Aunque esta tecnología no es propiamente una vacuna. Podemos decir, sencillamente, que la vacuna conlleva una inmunización activa, mientras que los monoclonales suponen una inmunización pasiva. Puede ser significativo que el calendario de la AEP ha cambiado su denominación clásica por el nuevo de “calendario de inmunización” por estos nuevos paradigmas de la protección y prevención.
Uno de estos usos ha tenido también que ver con el proceso de vacunación covid. El 8 de febrero de 2022, la Comisión de Salud Pública (CSP) aprobó la recomendación de uso de Evusheld en personas con alto grado de inmunosupresión y en otras personas que no se pueden vacunar frente a COVID-19. La administración de este fármaco, una combinación de anticuerpos monoclonales cilgavimab y tixagevimab, proporciona mediante una inmunización pasiva, protección frente a una posible infección por variantes del virus SARS-CoV-2 frente a las cuales es susceptible de neutralizar. Las recomendaciones han ido revisándose ante la aparición de las nuevas variantes del virus y la práctica de la inoculación. La última de ellas de 22 de febrero 2023, sobre cambio en las recomendaciones, ante la ausencia de actividad neutralizante in-vitro frente a variantes actuales circulantes12.
Manipular la respuesta inmunitaria con las nuevas plataformas ARN mensajero va a suponer un antes y un después en la lucha frente a algunas enfermedades, como el cáncer u otras patologías neurodegenerativas, al permitir el desarrollo de vacunas personalizadas frente a diversos tipos de tumores con una alta efectividad. Por ello, el potencial vacunal no solo se sitúa en la protección y prevención ante la infección causada por múltiples patógenos, sino también por las posibilidades que ha puesto de manifiesto el uso de nuevas tecnologías para la prevención, tratamiento y mejora de la calidad de vida de muchas enfermedades crónicas y degenerativas. Actualmente en Europa se contempla un potencial de más de 100 vacunas futuras, que usan diferentes tecnologías. En esta nueva era, las vacunas son más fáciles y rápidas de producir, más flexibles en condicionantes de distribución y con más opciones de personalización para la aplicación individual. Y, además, suman a su función preventiva, la terapéutica, esencial para el tratamiento de patologías relacionadas con los tumores y otras enfermedades. Ello también nos hará replantearnos la naturaleza jurídica atribuida actualmente a las vacunas en su sentido tradicional, repensar modelos regulatorios, administraciones competentes, actuación de los profesionales y formas de administración13.
En este nuevo escenario, hay que destacar la importancia de seguir avanzando en el conocimiento del papel de la Inteligencia Artificial en el ámbito sanitario, pues el descubrimiento y desarrollo de nuevos medicamentos en el marco de la Medicina Personalizada de Precisión requiere de un cambio de paradigma en la investigación con el objetivo de conseguir nuevos y mejores tratamientos para cada paciente de forma más eficiente y contribuyendo a la sostenibilidad del sistema sanitario. Ello va a plantear no pocos retos, como la accesibilidad a suficientes datos de calidad, la capacidad de explicación de los sistemas de Inteligencia Artificial y la regulación para garantizar la seguridad de los datos de los pacientes”. Por ello, la colaboración entre profesionales médicos y los sistemas de Inteligencia Artificial, así como la supervisión humana son esenciales para el éxito de esta herramienta en la Medicina del Futuro. E indudablemente, ello también deberá impactar en los organismos regulatorios y con capacidad decisoria en materia vacunal, todavía faltos, a nivel estatal al menos, de una composición multidisciplinar que lleva años reclamándose14. Lo que resulta evidente es que los avances en inmunología, la bioinformática, la biología de sistemas y las ciencias ómicas han favorecido el desarrollo de nuevos tipos de vacunas y el diseño, adaptación u optimización de estrategias de vacunación para mejorar el grado de respuesta inmune atendiendo a distintos factores, a través de nuevas formulaciones, vías de administración o el uso de adyuvantes. En este sentido, las vacunas de precisión buscan inducir una respuesta inmunológica más robusta y específicas que las vacunas clásicas considerando no solo la enfermedad o las características del patógeno, sino también la edad, las patologías asociadas con inmunodeficiencias o incluso las características genéticas individuales del receptor. Como decimos, las vacunas de precisión cambiarán el paradigma de la prevención y el abordaje de las enfermedades tanto infecciosas como no infecciosas15. Y ello puede suponer también cambios en las clásicas estrategias de vacunación. Se ha señalado que un reto a afrontar de forma prioritaria son las coberturas vacunales del adulto y de los grupos de riesgo. “Los esfuerzos de los Servicios de Medicina Preventiva y Salud Pública (SMPYSP), de Atención Primaria (AP) y las estrategias implementadas podrían no ser suficientes para alcanzar las coberturas de vacunación deseadas en los grupos de riesgo”. Y ello debe suponer que el modelo de gestión de la salud pública debería contemplar la importancia de la vacunación en grupos de riesgo a través de la incorporación activa de las indicaciones de vacunación en los Procesos Asistenciales Integrados (PAI). “Los PAI cumplen las características idóneas (abordaje multidisciplinar, estrategia preventiva e implicación de los gestores) para poder integrar la vacunación del paciente de riesgo y la revisión de su calendario de acuerdo con las recomendaciones vigentes, lo que podría mejorar considerablemente las coberturas de vacunación de los adultos y de los grupos de riesgo en particular"16.
En este sentido, la “vacunómica” podría ayudar a identificar qué factores genéticos contribuyen a las diferencias en la inmunización entre las personas, intentando desarrollar vacunas más efectivas y personalizadas. Por otro lado, uno de los avances más significativos en vacunómica es la identificación de biomarcadores genéticos que pueden predecir la respuesta a las vacunas, algo que el grupo GENVIP de Santiago de Compostela (Grupo de Genética, Vacunas, Infecciones y Pediatría) en colaboración con el grupo de Oxford mostraba recientemente en relación a la vacunación frente al neumococo, y cómo la regulación epigenética modula la intensidad de la respuesta humoral. Conocer estos genes podría permitir a los médicos predecir quiénes podrían necesitar estrategias de vacunación alternativas. Además, la tecnología de secuenciación de nueva generación ha hecho que sea más accesible y asequible analizar grandes conjuntos de datos genómicos, lo cual es esencial en la investigación de la vacunómica17.
De no menor impacto es el desarrollo del primer anticuerpo monoclonal para hacer frente al virus respiratorio sincitial (VRS) causante de las olas de bronquiolitis que fueron especialmente virulentas en el otoño de 2023. La Comisión Europea aprobó el 4 de noviembre 2022 un nuevo medicamento, Beyfortus (nirsevimab) con una alianza entre Sanofi y Astrazeneca, destinado a todos los niños de mayor riesgo (menores de 1 año y aquellos con patologías asociadas)18. No es una vacuna, pero en la práctica es bastante parecida. El anticuerpo es una proteína artificial creada en laboratorio que actúa frente al virus como si fuera un anticuerpo, requiere un solo pinchazo intramuscular, pero protege al bebé durante 5 meses. Su ventaja frente a la vacuna clásica es que es efectivo desde el momento de la inoculación. Estamos ante un cambio de paradigma. Hasta ahora solo teníamos un anticuerpo monoclonal, el palivizumab, pero indicado solo para grandes prematuros y bebés con dolencias congénitas. El nuevo Beyfortus es 100 veces más potente y evitará 3 de cada 4 infecciones que requieren atención médica19. En esta senda, son muchas ya las compañías que se han sumado al carro de esta nueva forma de inmunización, y ya hay ensayos en fase III que buscan proteger a los bebés inmunizándolos a través de la madre en el embarazo, cerca de 16 fármacos y vacunas en desarrollo.
Ante esta panorámica de progreso científico, las autoridades regulatorias, de evaluación y, esperemos que también las financiadoras a nivel estatal, reinventen los procedimientos, reduzcan los tiempos -porque se ha demostrado que se puede, sin comprometer la seguridad- y se decida si se requiere un nuevo modelo de autorización y seguimiento ante lo que está por venir20. Ante este futuro prometedor, parece evidente que a corto plazo habría que simplificar el entorno regulatorio, armonizando en todos los países los requisitos necesarios para las variaciones post-autorización y buscar alternativas al modelo animal para los test de liberación de lotes por repetitivos, variables y por coherencia con la Directiva de reducción, reemplazo y refinamiento21.
Además, debemos ser conscientes de que aún quedan retos pendientes a los que dar respuesta por parte de los colectivos médicos, investigadores científicos y gestores públicos. Un primer escenario de futuro se ha vislumbrado a raíz del consenso sobre el calendario de inmunización/vacunación a lo largo de toda la vida. Es indudable que el envejecimiento inmunitario asociado a la edad y otras comorbilidades médicas, influyen negativamente en las respuestas inmunitarias inducidas por la vacunación. No sólo eso: el acceso desigual a las vacunas, las barreras regulatorias, el reto logístico que plantean los problemas de abastecimiento y/o distribución, y la saturación de la Atención Primaria, donde se centralizan la mayoría de las campañas de vacunación, merecen un análisis más detenido y la búsqueda de alternativas, desde la educación en salud integral, mayor inversión, mejora de las estructuras y modelos de coordinación asistencial y, desde luego, seguir potenciando una cultura de credibilidad y confianza en torno a la vacunación, mediante campañas educativas y de formación ciudadana.
__________
1 https://www.sanidad.gob.es/areas/alertasEmergenciasSanitarias/alertasActuales/nCov/situacionActual.htm; https://elpais.com/sociedad/crisis-del-coronavirus/?rel=friso-portada
2 Algunos conflictos pueden verse ya como clásicos. Por citar algunos ejemplos: el brote de sarampión de Disneyland, en California, a principios de 2015, donde se vieron afectadas más de 100 personas en 14 estados de EE. UU; el fallecimiento de un niño en Olot por difteria, en junio de 2015; el médico italiano que fue expulsado de su colegio profesional por oponerse a las vacunas; las manifestaciones del periodista Javier Cárdenas vinculando el autismo y las vacunas; las dudas sobre la seguridad de las vacunas que el presidente Trump planteó en EE. UU; la reaparición de enfermedades que se consideraban eliminadas (sarampión o difteria); la inhabilitación de una pediatra por propagar que las vacunas causan el autismo en el Ilustre Colegio Oficial de Médicos de Madrid; o los casos de la pediatra que inyectó suero en vez de vacunas, además cobrando por ello y más recientemente la enfermera de Bizcaia denunciada por las familias de 80 menores afectados que fingía inocular vacunas, por presuntos delitos de falsificación de documentos, malversación de fondos y delito contra la salud pública. https://elpais.com/internacional/2015/02/04/actualidad/1423016244_553593.html; https://www.lavanguardia.com/vida/20150627/54433067058/muere-nino-olot-difteria.html; https://www.abc.es/sociedad/abci-medico-italiano-no-podra-ejercer-medicina-oponerse-vacunas-201704212222_noticia.html; https://elpais.com/elpais/2017/06/07/hechos/1496855559_006331.html; https://www.eldiario.es/sociedad/antivacunas-trump-salud_1_3647012.html; https://elpais.com/elpais/2018/08/21/ciencia/1534840912_770017.html; https://www.who.int/news-room/questions-and-answers/item/diphtheria; https://elpais.com/sociedad/2019/06/20/actualidad/1561034181_540468.html; https://www.levante-emv.com/comunitat-valenciana/2017/12/14/pediatra-inyecto-suero-vez-vacunas-12100936.html; https://www.eitb.eus/es/noticias/sociedad/detalle/9236616/declara-ante-juzgado-enfermera-de-santurtzi-acusada-de-no-vacunar-a-ninos-y-ninas/
3 https://elpais.com/noticias/vacunas/; https://www.economiadigital.es/politica/el-doctor-pedro-cavadas-cuestiona-la-vacuna-van-a-aparecer-sintomas-adversos_20108011_102.html; https://www.redaccionmedica.com/termometro/miguel-bose-miguel-bose-vuelve-a-cuestionar-las-vacuna-contra-el-covid-19-3163; https://www.lavanguardia.com/cultura/cine/20210225/6259629/victoria-abril-evita-mascarilla-comparecencia-feroz-honor.html; https://www.lavanguardia.com/vida/junior-report/20201120/49551491409/quienes-son-y-que-defienden-los-antivacunas.html
4 https://vacunasaep.org/profesionales/noticias/no-relacion-entre-vacunas-y-autismo
5 https://elpais.com/ccaa/2015/06/07/catalunya/1433694498_614087.html
6 https://www.elconfidencial.com/espana/2020-12-21/vacuna-covid-coronavirus-cis-encuesta_2880980/
7 https://www.sanidad.gob.es/profesionales/saludPublica/ccayes/alertasActual/nCov/documentos/Informe_GIV_comunicacion_20230210.pdf
8 https://www.elconfidencial.com/mundo/europa/2021-03-22/la-confianza-en-la-vacuna-de-astrazeneca-se-hunde-en-europa-tras-las-suspensiones_3000752/. La Agencia Europea de los Medicamentos (EMA) ha confirmado la seguridad global de la citada vacuna https://vacunasaep.org/profesionales/noticias/vacuna-covid-astrazeneca-EMA-confirma-balance-favorable
9 https://www.vacunacovid.gob.es/voces-expertas/mezclar-o-no-mezclar-vacunas-esa-es-la-cuestion
10 https://www.aemps.gob.es/medicamentos-de-uso-humano/acceso-a-medicamentos-en-situaciones-especiales/criterios-para-valorar-la-administracion-de-las-nuevas-alternativas-terapeuticas-antivirales-frente-a-la-infeccion-por-sars-cov-2/#collapse11
11 Más información sobre cómo funcionan las vacunas de ARNm contra el COVID-19
12 https://www.saludcastillayleon.es/es/covid-19/informacion-profesionales/vacunacion-gripe-covid-19/estrategia-vacunacion/evusheld.ficheros/2387025-Recomendaciones_uso_Evusheld_Cambios%2022022023.pdf Para consultar los datos actualizados a diario, https://opendata.ncats.nih.gov/covid19/variant/activity
13 Nos parece de imprescindible lectura el documento de consenso en el que se pone en valor el potencial preventivo de la vacunación, escanea las tendencias a futuro y propone medidas frente a los desafíos que se presentan en la era post covid-19, accesible en: https://diariofarma.com/2024/01/24/la-era-post-covid-abre-un-futuro-prometedor-para-el-desarrollo-de-las-nuevas-vacunas
14 Garrido Cuenca, N. Political and regulatory key factors of transparency and independence in terms of vaccination in Spain: information,participation and lobbies. Pharmaceuticals Policy and Law. 2017;19:103-20.
15 Interesante debate que puede verse en A debate, el papel de la Inteligencia Artificial, la Investigación Farmacológica y las Vacunas de Precisión en la Medicina del Futuro (institutoroche.es)
16 Fernández-Prada M, Campins-Martí M, Tamames-Gómez S. Redefiniendo el paradigma de la vacunación en inmunodeprimidos después de la pandemia. Enferm Infecc Microbiol Clin (Engl Ed). 2023;41:524-5.
17 Descubriendo la vacunómica: el futuro de las vacunas y la inmunización | Live-Med (livemed.in)
18 https://www.ema.europa.eu/en/medicines/human/EPAR/beyfortus#authorisation-details-section. La autorización es válida para todos los países UE, pero el procedimiento de autorización ha sido el previsto para los medicamentos.
19 https://elpais.com/sociedad/2022-11-23/hacia-el-fin-de-la-bronquiolitis-nuevos-farmacos-pueden-hacer-que-la-actual-ola-sea-la-ultima-que-golpea-a-los-bebes-espanoles.html
20 Garrido Cuenca, N., Predicaments during a period of health emergency: Waiving patent protections or innovative public procurement? Theexample of advance purchase agreements (APA) for COVID-19 vaccines. International Journal of Risk & Safety inMedicine. 2022;33:145-6.
21 Alsina Mier; P:; Las vacunas del futuro serán personalizadas | Noticias de en Heraldo.es
1. ¿Cuál es la consideración legal de las vacunas?
1.1. LAS VACUNAS ESTÁN CATALOGADAS LEGALMENTE COMO MEDICAMENTOS ESPECIALES
Las vacunas están catalogadas legalmente como medicamentos especiales.
Son medicamentos especiales los que, en cada caso, decida el legislador, por ser precisa una regulación determinada. A ellos se refiere el artículo 8.1.d) del Real Decreto Legislativo 1/2015, de 24 de julio, por el que se aprueba el texto refundido de la Ley de garantías y uso racional de los medicamentos y productos sanitarios (en adelante, Ley del Medicamento, abreviadamente LM).
El artículo 45 LM regula las garantías sanitarias concretas de las vacunas y demás medicamentos biológicos:
- Quedan sometidas a la regulación contenida en la propia ley y las que se determinan reglamentariamente (Real Decreto 1345/2007, de 11 de octubre, por el que se regula el procedimiento de autorización, registro y condiciones de dispensación de los medicamentos de uso humano fabricados industrialmente).
- Se exceptúan las preparaciones individualizadas de vacunas y alérgenos para un solo paciente.
- Por interés de la salud pública, la Agencia Española de Medicamentos y Productos Sanitarios (en adelante AEMPS) podrá someter a autorización previa cada lote y condicionar la comercialización a su conformidad.
El RD 1345/2007 define el medicamento inmunológico como todo medicamento consistente en vacunas, toxinas, sueros y alérgenos; también se definen las vacunas individualizadas y los alérgenos. Asimismo, se regulan las condiciones especiales de autorización previa de lotes de fabricación y tramitación de expedientes de registro, con previsión de modificaciones anuales para la vacuna de la gripe humana.
1.2. ¿CUÁLES SON LOS PROCEDIMIENTOS DE AUTORIZACIÓN DE LAS VACUNAS EN ESPAÑA?
| Las primeras vacunas contra el SARS-CoV-2 fueron autorizadas por la Comisión Europea con carácter condicional |
Existen 4 procedimientos de autorización de una vacuna en España, pero esto no implica que todas ellas posean código nacional y se encuentren comercializadas o disponibles, puesto que una vez autorizado un medicamento, el procedimiento para su puesta en circulación y decisión de financiación ya es competencia de cada Estado22.
- Procedimiento centralizado (Reglamento 726/2004): la Agencia Europea de los Medicamentos (EMA) es la responsable de la evaluación del medicamento para el mercado único europeo, coordinando las autorizaciones nacionales de los Estados miembros, más Islandia, Noruega y Liechtenstein. Sin embargo, aunque el valor de su trabajo en red y sus informes, es la Comisión Europea quien aprueba la autorización de una vacuna mediante este procedimiento.
- Procedimiento descentralizado (Directiva 2001/83; 2004/27): la compañía presenta la solicitud de autorización de comercialización al Estado Miembro de Referencia (EMR) y a los distintos Estado Miembros Concernidos (EMC) simultáneamente, los cuales elaboran y evalúan la autorización de comercialización
- Reconocimiento Mutuo (Directiva 2001/83; 2004/27): la compañía posee la autorización de comercialización nacional en un Estado (por lo general EMR) y presenta, posteriormente, la solicitud de autorización de comercialización a distintos EMC
- Nacional (Real Decreto 1345/2007), autorización por la AEMPS para la puesta en mercado de cualquier medicamento en España
Aunque estos sean los procedimientos previstos para la autorización de medicamentos, y también por tanto para las vacunas, a pesar de su naturaleza de medicamento especial, pueden darse circunstancias determinadas, excepcionales como la que hemos vivido en época de pandemia, que cambien las reglas generales por las que requiera la propia situación. Previstas también normativamente, y aunque la situación haya cambiado, pensamos que debemos seguir refiriéndonos a ellas, primero porque una de estas circunstancias puede volver a ocurrir, segundo porque la vacuna covid sigue inoculándose y parece haber venido para quedarse y, tercero y principal, porque este proceso ha supuesto una clara enseñanza sobre las posibilidades de mejorar los procedimientos ligados a la innovación, sin merma de las garantías, a flexibilizar la enorme carga burocrática que viene suponiendo una rémora para la industria, los profesionales, la Administración y los pacientes, a los problemas del desabastecimiento y la distribución, en fin, a la negociación, fijación de precios y financiación. También porque a estas alturas, estamos en disposición de corregir errores, muchos de ellos ligados a los problemas de transparencia que han empañado la inmunización masiva, pero que pueden y deben hacerse extensivos a este déficit todavía presente en nuestros sistemas de contratación pública en materia de medicamentos.
__________
22 https://www.aemps.gob.es/medicamentos-de-uso-humano/vacunas/autorizacion-de-vacunas/
⌂
1.3. ¿CUÁLES SON Las vías rápidas aprobadas por la EMA PARA LA AUTORIZACIÓN DE LAS VACUNAS PARA PREVENIR LA COVID-19?
| La directiva europea de medicamentos permite procedimientos nacionales de autorización en situaciones excepcionales |
Con carácter general, los medicamentos biológicos, y en particular las vacunas, tienen que autorizarse por la Comisión Europea, siguiendo las propuestas de la Agencia Europea de los Medicamentos (EMA), como se ha indicado en el apartado anterior; por tanto, debería haber sido aquella quien autorizase las vacunas, como ocurrió con la autorización de comercialización condicional para vacuna Comirnaty, desarrollada por BioNTech y Pfizer23, y posteriormente, la de Moderna24, la de AstraZeneca25 y la de Janssen26.
Sin embargo, la Directiva Europea de Medicamentos27 contempla la posibilidad de que, en situaciones excepcionales, como es sin duda la pandemia de la COVID-19, los países puedan utilizar sus procedimientos nacionales de autorización y tomar la delantera en situaciones excepcionales de riesgo28. Esto es lo que hizo Reino Unido, autorizando la primera vacuna con un procedimiento de autorización de emergencia la vacuna de Biontech-Pfizer29, a diferencia del resto de los países.
Éstos son, hasta la fecha, los procedimientos aprobados por la Agencia para agilizar los plazos regulatorios de aprobaciones covid sin mermar la solidez de los criterios científicos30.
| La situación de pandemia aceleró, sin merma de la seguridad, la etapa de I+D, autorización y posautorización |
- Apoyo acelerado en la etapa de I+D.
- Asesoramiento científico rápido. En el contexto de la COVID-19 no se cobran tasas por este asesoramiento, y el procedimiento se ha reducido a un máximo de 20 días, en comparación a la media habitual, establecida entre los 40 y los 70 días
- Planes de investigación pediátrica (PIP). El tiempo de revisión para un PIP se ha reducido a 20 días, en comparación al tiempo habitual, de hasta 120 días
- Evaluación acelerada en procedimientos de autorización y posautorización.
- Revisión continua. En circunstancias normales, todos los datos que respaldan una solicitud de autorización de comercialización deben presentarse al comienzo del procedimiento de evaluación. La revisión continua, empleada en emergencias de salud como la actual, permite a la EMA evaluar los datos de un medicamento prometedor a medida que están disponibles
- Evaluación acelerada. Este procedimiento ha permitido reducir el tiempo de revisión de productos de gran interés para la salud pública de 210 días a menos de 150
Para la aprobación plena es necesaria la presentación de resultados de vacunación pediátrica (que han avanzado con las pruebas clínicas del uso de vacunas frente al COVID-19 en niños31), datos sobre la duración de la inmunidad o que demuestren que la calidad de los lotes se mantiene en el escalado de la producción.
En todo caso, según los informes más recientes del Centro para el Control y prevención de Enfermedades, desde el 12 de septiembre del 2023, se recomienda que todas las personas de 5 años de edad o más‡ reciban 1 dosis de una vacuna actualizada contra el COVID-19 para protegerse de la forma grave de la covid; especialmente las vacunas actualizadas contra la covid para 2023-2024 de Pfizer-BioNTech, Moderna, o Novavax para evitar enfermarse gravemente a causa de esta enfermedad. Los niños de 6 meses a 4 años de edad necesitan varias dosis de vacunas contra la covid para estar al día, incluida al menos 1 dosis de una vacuna actualizada32. Las vacunas recomendadas, según la franja de edad, son las de Pfizer-BioNTech, Moderna o Novavax
| Es preciso seguir evaluando las condiciones de las vacunas frente al SARS-CoV-2, (lo que se ha denominado “Rolling review”) autorizadas condicionalmente, hasta su autorización plena |
El seguimiento regulatorio implica seguir evaluando las condiciones que tienen que cumplirse en el plazo que concede la autorización condicional -en el caso de estas vacunas, antes de un año- para después volver a presentar la solicitud al Committee for Medicinal Products for Human Use (EMA) y que éste pueda optar por conceder una autorización plena, renovar la condicional por un tiempo limitado o retirar la autorización de comercialización33.
En el momento actual, según los datos de la EMA, la Comisión ha concedido ocho autorizaciones condicionales de comercialización a las vacunas desarrolladas por BioNTech y Pfizer, Moderna, AstraZeneca, Janssen Pharmaceutica NV, Novavax, Valneva, Sanofi y GSK e HIPRA, respectivamente, a raíz de los resultados positivos de las evaluaciones de su seguridad y eficacia que ha efectuado la Agencia Europea de Medicamentos (EMA). Otras vacunas se encuentran en distintas fases de evaluación por la EMA. De las vacunas aprobadas, las de BioNTech & Pfizer, Moderna, AstraZeneca, Valneva y Sanofi Pasteur han recibido, en octubre y noviembre de 2022, una autorización de comercialización estándar, mientras que las de Janssen y Novavax aún mantienen el estatus de "autorización condicionada" con renovación anual34. El estado actual pormenorizado de la situación de autorización puede consultarse en la página de la EMA35.
__________
23 https://www.aemps.gob.es/la-aemps/ultima-informacion-de-la-aemps-acerca-del-covid%e2%80%9119/vacunas-contra-la-covid%e2%80%9119/comirnaty/
24 https://www.aemps.gob.es/la-aemps/ultima-informacion-de-la-aemps-acerca-del-covid%e2%80%9119/vacunas-contra-la-covid%e2%80%9119/covid-19-vaccine-moderna/
25 hhttps://www.aemps.gob.es/la-aemps/ultima-informacion-de-la-aemps-acerca-del-covid%e2%80%9119/vacunas-contra-la-covid%e2%80%9119/covid-19-vaccine-astrazeneca/
26 https://www.aemps.gob.es/la-aemps/ultima-informacion-de-la-aemps-acerca-del-covid%e2%80%9119/vacunas-contra-la-covid%e2%80%9119/covid-19-vaccine-janssen/
27 Directiva 2001/83 / CE del Parlamento Europeo y del Consejo, de 6 de noviembre de 2001, por la que se establece un código comunitario sobre medicamentos para uso humano (Versión consolidada actual: 26/07/2019).
28 https://www.fieldfisher.com/es-es/locations/espana2/actualidad/todas-las-claves-legales-que-respaldan-la-autoriza
29 https://diariofarma.com/2020/12/02/reino-unido-autoriza-la-vacuna-de-pfizer-biontech-contra-el-sars-cov2
30 https://elglobal.es/politica/la-ema-a-favor-de-exigir-a-las-companias-estudios-post-autorizacion-de-aprobaciones-covid/
31 https://www.redaccionmedica.com/secciones/industria/vacuna-covid-19-astrazeneca-primeros-ensayos-mundo-en-ninos-3205
32 CDC. La seguridad de las vacunas contra el COVID-19 en niños y adolescentes
33 https://www.diariomedico.com/medicina/politica/la-aemps-abarca-360o-en-el-proceso-previo-y-postcomercializacion-de-las-vacunas.html
34 Los datos del estudio regulatorio, con datos actualizados a 19 de marzo 2024 de la última vacuna autorizada HYPRA, en: https://www.ema.europa.eu/en/human-regulatory-overview/public-health-threats/coronavirus-disease-covid-19/covid-19-medicines
35 https://commission.europa.eu/strategy-and-policy/coronavirus-response/safe-covid-19-vaccines-europeans/questions-and-answers-covid-19-vaccination-eu_es#authorisation
⌂
1.4. ¿CUÁL ES EL PAPEL DE LA AEMPS EN RELACIÓN CON LAS VACUNAS PARA PREVENIR LA COVID-19?
| La AEMPS, una vez aprobadas condicionalmente las vacunas contra el SARS-CoV-2, tendrá una labor fundamental en su farmacovigilancia |
El papel de la AEMPS en el caso concreto de las vacunas frente al coronavirus es novedoso respecto a la evaluación de otras vacunas, ya que sus representantes no solo han hecho el trabajo tradicional de asesoría científica y evaluación de los ensayos clínicos y dosieres —directamente o a través de su participación en la EMA—, sino que la AEMPS también ha formado parte del proceso europeo de selección, negociación y adquisición de las vacunas, ha prestado soporte técnico a la elaboración de la estrategia de vacunación dirigida desde el Ministerio de Sanidad y empieza ahora su trabajo de farmacovigilancia. También asume un papel importante en la coordinación de la logística entre las CC. AA. y las compañías.
Una vez que por parte de la EMA se ha concedido la autorización condicional para todos los países del entorno, dentro de cada país las autoridades sanitarias son las que fijan las condiciones de precio y de financiación.
En la situación actual, parece previsible que haya cambios respecto a las formas clásicas de fijación de precio: precio de reembolso por envase (es lo habitual), acuerdos de techo máximo (el Estado fija el tope de lo que va a gastar), o de riesgo compartido (se paga si el medicamento funciona)36.
En el caso de las nuevas vacunas, una labor fundamental de la AEMPS será la de farmacovigilancia, especialmente por dos razones:
- Las vacunas frente al coronavirus se han utilizado de forma masiva, de manera que la posibilidad de que aparezcan efectos desconocidos es más alta que cuando un medicamento se va introduciendo paulatinamente. Si apareciera un acontecimiento inesperado o desconocido, hay que reaccionar inmediatamente para evitar que siga afectando a la población o suponga cualquier tipo de riesgo, y poner las condiciones para que no vuelva a ocurrir; un buen ejemplo de ello fue la suspensión de la vacuna de AstraZeneca durante dos semanas, hasta aclarar las dudas sobre su seguridad37
- Además, la AEMPS requirió que se le comuniquen todos los acontecimientos adversos, incluso un error en la dosificación o en la preparación del vial; habitualmente, solo se notifican las sospechas de reacciones adversas.
A este fin se orientó el plan Vigilancia de la Seguridad de las vacunas frente a la COVID-19 que la AEMPS anunció el 17 de diciembre de 2020, cuya última versión fue en enero de 202138. El pasado 19 de enero de 2023 la AEMPS publicó el 19.º Informe de Farmacovigilancia sobre Vacunas COVID-19, que será la última publicación de este tipo. Los nuevos riesgos que pudieran identificarse desde esa fecha para cada una de las vacunas autorizadas en España podrán consultarse en la ficha técnica y el prospecto disponibles en el Centro de Información Online de Medicamentos (CIMA).
__________
36 https://www.fieldfisher.com/es-es/locations/espana2/actualidad/todas-las-claves-legales-que-respaldan-la-autoriza.
37 https://www.aemps.gob.es/informa/notasinformativas/medicamentosusohumano-3/seguridad-1/2021-seguridad-1/el-ministerio-de-sanidad-suspende-a-partir-de-manana-y-durante-las-dos-proximas-semanas-la-vacunacion-con-la-vacuna-frente-a-la-covid-19-de-astrazeneca/
38 www.aemps.gob.es/medicamentosUsoHumano/vacunas/docs/vigilancia_seguridad_vacunas_COVID-19.pdf.
2. VOLUNTARIEDAD-OBLIGATORIEDAD DE LA VACUNACIÓN
2.1. ¿En qué casos se puede imponer la vacunación con carácter obligatorio?
2.1.1. Normativa de salud pública
2.1.2. Normativa básica en materia de información y consentimiento
2.1.3. El debate social sobre la obligatoriedad de las vacunas
2.2. ¿Cuál es el procedimiento administrativo y judicial para imponer la vacunación obligatoria?
2.3. ¿En qué supuestos vienen exigiendo nuestros juzgados y tribunales la vacunación obligatoria?
2.1. ¿En qué casos se puede imponer la vacunación con carácter obligatorio?
| Las crisis sanitarias, como las epidemias, permiten al gobierno declarar el estado de alarma |
La vacunación en España es voluntaria, ya que nuestro ordenamiento no incorpora explícitamente el deber de vacunación y nadie puede, en principio, ser obligado a vacunarse. Ahora bien, hay determinadas situaciones que permiten que los poderes públicos competentes impongan la vacunación forzosa, fundamentalmente en caso de epidemias.
La primera norma de carácter general, no propiamente sanitaria, que permitiría fundamentar en determinados casos la obligatoriedad de las vacunas es la Ley Orgánica 4/1981, de 1 de junio, de estados de alarma, excepción y sitio, cuyo art. 4 establece que:
“El Gobierno, en uso de las facultades que le otorga el artículo 116.2 de la Constitución, podrá declarar el estado de alarma, en todo o parte del territorio nacional, cuando se produzca alguna de las siguientes alteraciones graves de la normalidad: b) “crisis sanitarias, tales como las epidemias”.
Una vez que se produzca esta situación, el art. 12 establece que:
“La autoridad competente podrá adoptar por sí, según los casos, además de las medidas previstas en los artículos anteriores, las establecidas en las normas para la lucha contra las enfermedades infecciosas”.
Esta norma, por su carácter marcadamente excepcional, sólo se había aplicado una vez en la historia de nuestro Derecho39, antes del Real Decreto 463/2020, de 14 de marzo, por el que se declara el estado de alarma para la gestión de la situación de crisis sanitaria ocasionada por la COVID-1940 y del posterior Real Decreto 926/2020, de 25 de octubre, por el que se declara el estado de alarma para contener la propagación de infecciones causadas por el SARS-CoV-241.
| Una norma de 1944 permite declarar obligatorias algunas vacunas, aunque hay dudas sobre si es aplicable |
Por lo que se refiere a la normativa sanitaria, hemos de comenzar haciendo referencia a la Ley 22/1980, de 24 de abril, de modificación de la Base IV de la Ley de Bases de la Sanidad Nacional de 25 de noviembre de 194442, en cuyo artículo único dispone que:
“Las vacunaciones contra la viruela y la difteria y contra las infecciones tíficas y paratíficas, podrán ser declaradas obligatorias por el Gobierno cuando, por la existencia de casos repetidos de estas enfermedades o por el estado epidémico del momento o previsible, se juzgue conveniente. En todas las demás infecciones en que existan medios de vacunación de reconocida eficacia total o parcial y en que ésta no constituya peligro alguno, podrán ser recomendados y, en su caso, impuestos por las autoridades sanitarias.”
Si bien es cierto que se trata de una norma en vigor, es de dudosa aplicabilidad, al no haberse cumplido el mandato de la Disposición Final 5.ª de la Ley General de Sanidad de refundición, regularización, aclaración y armonización de dicho artículo en el plazo de 18 meses y no tener la citada Ley el necesario rango de Ley Orgánica, por afectar a derechos fundamentales, en concreto, a la integridad física del artículo 15 de la Constitución.
Nos referiremos a continuación a la normativa en materia de salud pública y posteriormente a la normativa en materia de información y consentimiento informado.
__________
39 Solo se ha aplicado una vez en la historia de nuestro Derecho, en concreto con la aprobación del Real Decreto 1673/2010, de 4 de diciembre, por el que se declara el estado de alarma para la normalización del servicio público esencial del transporte aéreo, con ocasión de la huelga de controladores aéreos de diciembre de 2010 que colapsó nuestro espacio aéreo.
40 https://boe.es/buscar/act.php?id=BOE-A-2020-3692
41 https://www.boe.es/buscar/act.php?id=BOE-A-2020-12898.
42 Ley 22/1980, de 24 de abril, de modificación de la Base IV de la Ley de Bases de la Sanidad Nacional de 25 de noviembre de 1944.
2.1.1. Normativa de salud pública
| El Tribunal Europeo de Derechos Humanos avala la vacunación infantil obligatoria, como medida necesaria y proporcional |
Por lo que se refiere al Derecho Comunitario, el artículo 168 del Tratado de Funcionamiento de la Unión Europea dispone que:
“Al definirse y ejecutarse todas las políticas y acciones de la Unión se garantizará un alto nivel de protección de la salud humana”.
Añadiendo, a continuación, que:
“La acción de la Unión, que complementará las políticas nacionales, se encaminará a mejorar la salud pública, prevenir las enfermedades humanas y evitar las fuentes de peligro para la salud física y psíquica”.
En similares términos, la Carta de los Derechos Fundamentales de la Unión Europea dispone en su artículo 35 que:
“Toda persona tiene derecho a la prevención sanitaria y a beneficiarse de la atención sanitaria conforme a las condiciones establecidas en las disposiciones nacionales. Al definirse y ejecutarse todas las políticas y acciones de la Unión se garantizará un alto nivel de protección de la salud humana”.
A nivel europeo, la reciente Sentencia del Tribunal Europeo de Derechos Humanos, de 8 de abril de 202143, avala la vacunación infantil obligatoria, entendiendo que es "necesaria en una sociedad democrática", en una sentencia pronunciada después de ser solicitado por padres de niños rechazados por guarderías en República Checa por no estar vacunados.
La política sanitaria checa, que obliga a vacunar a los niños contra nueve enfermedades, entre ellas la difteria, el tétanos, la hepatitis B y el sarampión, "no viola la convención europea de los derechos humanos ni el derecho al respeto de la vida privada".
"El objetivo tiene que ser que cada niño esté protegido contra enfermedades graves, mediante la vacunación o gracias a la inmunidad de grupo“
El tribunal apoya un "principio de solidaridad social que puede justificar que se imponga la vacunación a todos, incluso a aquellos que se sienten menos amenazados por la enfermedad, cuando se trata de proteger a las personas más vulnerables".
En conclusión, el Tribunal declaró la proporcionalidad de las medidas del gobierno checo, justificando la obligatoriedad de la vacunación, desde el principio de justicia social. Asimismo, consideró ajustadas a Derecho las multas coercitivas que pudieran imponerse ante un eventual incumplimiento, planteando más dudas el ejercicio de la fuerza coercitiva para llegar a un modelo de vacunación forzosa44.
Como veremos, este supuesto de vacunación condicional ha sido también planteado en nuestro país, solucionándose jurídicamente en el mismo sentido, en aplicación del principio del interés superior del menor.
En esta línea, también ha sido relevante la doctrina sentada por el mismo Tribunal en el caso Abgrall et 671 autres c.France. El TEDH en Decisión de 24 de agosto de 2021 denegó la petición de medidas cautelares solicitadas por un importante colectivo de bomberos franceses frente a la Ley núm. 2021-1040, de 5 de agosto 2021 relativa a la gestión de la crisis sanitaria45. Se solicitaba la suspensión de la obligación vacunal para los colectivos profesionales que trabajan en el ámbito hospitalario prevista en el art. 12 de la ley francesa, así como de las disposiciones que prohibían el ejercicio de su actividad y la suspensión de empleo y sueldo en caso de negativa a la vacunación. Los funcionarios entendían comprometidos sus derechos a la vida (art. 2 CEDH) y a la integridad física o moral (art. 8 CEDH). El TEDH rechazará la medida cautelar de urgencia solicitada en virtud del artículo 39 de su Reglamento, al no apreciar la existencia de un riesgo inminente de daño irreparable, confirmando la decisión administrativa de vacunación obligatoria.
Las vacunas constituyen, sin duda, una de las herramientas más eficaces en materia de salud pública, en lo que a la prevención de enfermedades se refiere, sin embargo, por lo que se refiere ya al Derecho interno español, se parte de un principio de voluntariedad en las medidas de salud pública.
| En España las vacunas son voluntarias, salvo situaciones especiales en materia de salud pública |
Por una parte, el artículo 28 de la Ley 14/1986, de 25 de abril, General de Sanidad, establece que:
“Todas las medidas preventivas contenidas en el presente capítulo deben atender a los siguientes principios:
- Preferencia de la colaboración voluntaria con las autoridades sanitarias
- No se podrán ordenar medidas obligatorias que conlleven riesgo para la vida
- Las limitaciones sanitarias deberán ser proporcionadas a los fines que en cada caso se persigan
- Se deberán utilizar las medidas que menos perjudiquen al principio de libre circulación de las personas y de los bienes, la libertad de Empresa y cualesquiera otros derechos afectados
Por otra parte, resulta sorprendente que apenas se haga mención a las vacunas en la Ley 33/2011, 4 de octubre, General de Salud Pública; en dicha ley, lejos de imponer la obligatoriedad de la vacunación, se parte de un principio general de voluntariedad en las actuaciones de salud pública, así el art. 5.2 establece que:
“Sin perjuicio del deber de colaboración, la participación en las actuaciones de salud pública será voluntaria, salvo lo previsto en la Ley Orgánica 3/1986, de 14 de abril, de Medidas especiales en materia de salud pública”.
La regla general es, así pues, la voluntariedad, salvo lo dispuesto en la Ley Orgánica 3/198646. El art.1 de esta norma establece:
“Al objeto de proteger la salud pública y prevenir su pérdida o deterioro, las autoridades sanitarias de las distintas Administraciones Públicas podrán, dentro del ámbito de sus competencias, adoptar las medidas previstas en la presente Ley cuando así lo exijan razones sanitarias de urgencia o necesidad”.
| Las medidas especiales de salud pública fuera del estado de alarma deben ser convalidadas por la autoridad judicial |
Por su parte, el art. 2 señala que:
“Las autoridades sanitarias competentes podrán adoptar medidas de reconocimiento, tratamiento, hospitalización o control cuando se aprecien indicios racionales que permitan suponer la existencia de peligro para la salud de la población debido a la situación sanitaria concreta de una persona o grupo de personas o por las condiciones sanitarias en que se desarrolle una actividad”.
Finalmente, el art. 3 dispone que:
“Con el fin de controlar las enfermedades transmisibles, la autoridad sanitaria, además de realizar las acciones preventivas generales, podrá adoptar las medidas oportunas para el control de los enfermos, de las personas que estén o hayan estado en contacto con los mismos y del medio ambiente inmediato, así como las que se consideren necesarias en caso de riesgo de carácter transmisible”.
Aunque estas previsiones legales están plagadas de conceptos jurídicos indeterminados, podemos concluir que es legalmente posible imponer la vacunación en caso de epidemia, cuando exista un riesgo colectivo para la salud pública, desplazando en dichos supuestos el principio general de voluntariedad en la vacunación que impera en nuestro Derecho.
| La ley gallega, que imponía multas al que se negara injustificadamente a la vacunación, ha quedado en suspenso, al haberse admitido recurso de insconstitucionalidad contra dicha medida |
A nivel autonómico, es de destacar la nueva Ley de Salud de Galicia y su previsión de sancionar a los que se nieguen injustificadamente a la vacunación.
La Ley 8/2021, de 25 de febrero, de modificación de la Ley 8/2008, de 10 de julio, de salud de Galicia47, pretende concretar en su art. 38 las medidas que, teniendo en cuenta lo dispuesto en la legislación estatal, de rango orgánico y ordinario, pueden adoptarse por las autoridades sanitarias gallegas para la protección de la salud pública y los requisitos que se han de cumplir para su correcta adopción.
Se distinguen, por un lado, medidas preventivas de obligado cumplimiento (art. 38.1) y, por otro, medidas especiales en materia de salud pública (art. 38.2) y, entre ellas, las del apartado b. 5.ª), dirigidas al control de las enfermedades transmisibles: 5.ª) Sometimiento a medidas profilácticas de prevención de la enfermedad, incluida la vacunación o inmunización, con información, en todo caso, de los posibles riesgos relacionados con la adopción o no adopción de estas medidas.
Y se establece el siguiente régimen sancionador en los artículos 39 y siguientes:
- Infracciones leves, según el art. 41 bis d) La negativa injustificada al sometimiento a medidas de prevención consistentes en la vacunación o inmunización prescritas por las autoridades sanitarias, de acuerdo con lo establecido en la presente ley, con la finalidad de prevención y control de una enfermedad infectocontagiosa transmisible, si las repercusiones producidas han tenido una incidencia escasa o sin trascendencia directa en la salud de la población. Se prevén sanciones de 1000 a 3000 € (art. 44 bis).
- Infracciones graves, según el art. 42 bis, cuando esa negativa injustificada a la vacunación pudiera producir un riesgo o un daño grave para la salud de la población, siempre que no sean constitutivas de infracción muy grave. Se prevén sanciones de 3001 a 60 000 € (art. 44 bis).
- Infracciones muy graves, según el art. 43, cuando esa negativa injustificada a la vacunación produjese un riesgo o un daño muy grave para la salud de la población. Se prevén sanciones de 60 001 a 600 000 € (art. 44 bis).
Dejando al margen las dudas acerca de si esta ley afecta a derechos fundamentales y si el legislador autonómico tiene competencia para ello —en cuyo caso, lo más adecuado sería que se aprobase por una ley estatal con rango de ley orgánica—, la existencia de un régimen sancionador no hace sino poner de manifiesto la previa existencia de un deber cuyo incumplimiento conlleva consecuencias punitivas.
Es cierto que si bien no se puede afirmar propiamente que en dicha ley se obliga a la vacunación, en la medida en que no se lleva a cabo ninguna medida ablativa para los que no quieren ser vacunados, la libertad del individuo se ve claramente coartada, al tener que soportar una sanción por la decisión de no vacunarse.
Además, la propia ley en su art. 38 ter 6. prevé incluso la adopción de medidas ablativas, al afirmar que: “La ejecución de las medidas podrá incluir, cuando resultase necesario y proporcionado, la intervención directa sobre las cosas y la compulsión directa sobre las personas, con independencia de las sanciones que, en su caso, pudieran imponerse. A estos efectos, se recabará la colaboración de las fuerzas y cuerpos de seguridad que sea necesaria para la ejecución de las medidas”.
Sin embargo, el Tribunal Constitucional admitió a trámite el recurso de inconstitucionalidad a petición del Gobierno español contra la Ley de Salud de Galicia. Además, mientras resuelve sobre el fondo, deja en suspenso la vigencia de los apartados recurridos, donde se incluyen, entre otros aspectos, la vacunación obligatoria de la población. Así, el TC ha decidido finalmente tramitar este recurso que el Gobierno presentó el 30 de marzo de 2021 al entender que ciertos puntos de esta norma deberían formar parte de una ley estatal y no autonómica, después del dictamen solicitado al Consejo de Estado48. El auto de suspensión “razonó que la vacunación obligatoria no era una medida preventiva que apareciera expresamente contemplada en la Ley Orgánica 3/1986, de medidas especiales en materia de Salud Pública, y suponía una intervención corporal coactiva y practicada al margen de la voluntad del ciudadano, que ha de someterse a la vacunación si se adopta esta medida, so pena de poder ser sancionado, en caso de negativa injustificada a vacunarse”. El Gobierno retiró el recurso a la ley de Galicia tras alcanzar un acuerdo con la comunidad para que se dejara claro el carácter “voluntario” de inmunizarse, incluyendo una disposición adicional que señalará explícitamente que ponerse una vacuna no es obligatorio en ninguna circunstancia. Este precedente puso de manifiesto "el complicado encaje constitucional", porque se basó en el desarrollo legislativo y ejecución de la legislación básica que corresponde al Estado en materia de sanidad interior.
En idéntica situación se encuentran más de una docena de artículos de la Ley 2/2021, de 24 de junio, de medidas para la gestión de la pandemia de COVID-19 aprobada por el Parlamento vasco, que fue admitida a trámite por el Pleno del TC en febrero de 2022. Particularmente polémicas han sido los preceptos que contemplan "sin intervención judicial" cuestiones como la vacunación obligatoria, prestaciones personales obligatorias, la prohibición de trabajar si te niegas a vacunarte o a hacer prueba diagnóstica49. En el sentido del Auto sobre la Ley gallega, también fue suspendido en concreto el precepto sobre la vacunación obligatoria.
| La nueva Ley vasca de Salud Pública permite la vacunación selectiva de determinados grupos de población o profesionales, en situaciones de emergencia o pandemia |
La nueva Ley 13/2023, de 30 de noviembre, de Salud Pública de Euskadi50 vuelve a recoger la obligatoriedad de vacunarse en situaciones de “emergencia sanitaria” o “pandemia”. En concreto recoge un paquete de “medidas de intervención sobre las personas”, contemplando el art. 111 la vacunación selectiva de determinados grupos de población o profesionales sanitarios en caso de pandemia o catástrofe sanitaria. En este sentido, la ley sostiene que “Conforme a la normativa vigente y a las garantías establecidas por esta, cuando exista o se sospeche razonablemente la existencia de un riesgo urgente para la salud de la población debido a la situación sanitaria concreta de una persona o grupos de personas, o a situaciones de emergencia de salud pública o pandemias, la autoridad sanitaria podrá ordenar la adopción de medidas preventivas generales y de intervención. Entre dichas medidas se incluyen: el establecimiento de restricciones en la libertad de movilidad y en el ejercicio profesional; la práctica de exámenes y reconocimientos médicos; la vacunación selectiva de determinados grupos de población o profesionales; prescripción de tratamiento médico y hospitalización; el control individual sobre la persona o grupos de personas, así como el aislamiento domiciliario, mediante decisión motivada, por el tiempo necesario para la desaparición del riesgo.”
Frente a dicha Ley, al margen de los problemas constitucionales expuestos, se han planteado diversos recursos, entre otros, el del Consejo de Colegios de Médicos del País Vasco recurre la Ley de Salud Pública de Euskadi51.
Lo cierto es que todos estos conflictos están reclamando una regulación de ámbito nacional a través de una ley orgánica, como aconsejó, en el caso de Galicia, el propio Consejo de Estado a través de su informe preceptivo, que regule con la precisión que algunas cuestiones requieren lo vacíos normativos que todavía quedan en nuestro derecho, de excepción o no. Y que se aclaren las diferencias entre vacunación forzosa y obligatoria, despejando las dudas que sobre el control previo judicial pueden suscitar uno y otro tipo de vacunación. Lo cual es más necesario desde el momento en que el TC anuló por inconstitucionales los preceptos de la LOPJ que, en plena pandemia, apoderaron a los jueces de esta facultad de fiscalización previa (STC 70/2022, de 2 de junio).
__________
43 STEDH Vavricka and others v. The Czech Republic, de 8 de abril, en Vavřička and Others v. the Czech Republic [GC] (coe.int)
44 Comentario a propósito del debate generado por esta jurisprudencia, con la bibliografía de referencia, en DELGADO GARRIDO, C. El debate sobre la voluntariedad o la obligatoriedad de la vacunación en tiempos de pandemia. RVAP 2021;121:17..
45 Caso Abgrall. Les demandes de mesures provisoires de 672 sapeurs-pompiers concernant la loi relative à la gestion de la crise sanitaire n’entrent pas dans le champ d’application de l’article 39 du règlement de la Cour. Comunicado del TEDH 243/2021. 25 de agosto de 2021.
46 Recordemos que, en relación con la vacuna frente a la COVID-19, la actualización 1 de la Estrategia de vacunación frente a COVID-19 en España (18 de diciembre de 2020), como las que la han sucedido, siguen este mismo criterio: “sin perjuicio del deber de colaboración que recae sobre los individuos, la vacunación frente a COVID-19 será voluntaria, y ello, a salvo de lo previsto en la Ley Orgánica 3/1986, de 14 de abril, de Medidas especiales en materia de salud pública. Estrategia de vacunación frente a COVID-19 en España, Actualización 1, 18 de diciembre de 2020 .Las actualizaciones posteriores en Ministerio de Sanidad - Áreas - Estrategia de vacunación COVID-19 en España
47 LEY 8/2021, de 25 de febrero, de modificación de la Ley 8/2008, de 10 de julio, de salud de Galicia
48 El Consejo de Ministros cursa solicitud urgente de dictamen al Consejo de Estado para valorar si procede presentar recurso de inconstitucionalidad frente a la Ley 8/2021.
49 https://www.europapress.es/nacional/noticia-constitucional-admite-tramite-recurso-vox-contra-ley-antipandemias-pais-vasco-20220201110844.html
50 Ley 13/2023, de 30 de noviembre, de Salud Pública de Euskadi.
51 El Consejo de Colegios de Médicos del País Vasco recurre la Ley de Salud Pública de Euskadi
2.1.2. Normativa básica en materia de información y consentimiento
| La ley de autonomía del paciente, si hay riesgo para la salud pública, permite intervenciones clínicas indispensables sin consentimiento, que deben ser convalidadas por los jueces |
Finalmente, hemos de tener en cuenta la Ley 41/2002, de 14 de noviembre, básica reguladora de la autonomía del paciente y de derechos y obligaciones en materia de información y documentación clínica, que establece en su art. 9.2 que:
“Los facultativos podrán llevar a cabo las intervenciones clínicas indispensables en favor de la salud del paciente, sin necesidad de contar con su consentimiento, en los siguientes casos: a) Cuando existe riesgo para la salud pública a causa de razones sanitarias establecidas por la Ley. En todo caso, una vez adoptadas las medidas pertinentes, de conformidad con lo establecido en la Ley Orgánica 3/1986, se comunicarán a la autoridad judicial en el plazo máximo de 24 horas siempre que dispongan el internamiento obligatorio de personas".
El principio general de autonomía de la voluntad que establece la Ley 41/2002, cede en determinadas situaciones, donde es posible realizar intervenciones de salud sin consentimiento de los interesados; una de esas situaciones es el riesgo para la salud pública, remitiendo nuevamente el legislador la cuestión a la Ley Orgánica 3/1986 vista y con la preceptiva intervención de un juez que ejerza la función de control de este tipo de decisiones52.
En análogo sentido se manifiesta la normativa autonómica reguladora de los derechos de información y documentación clínica.
Así pues, a modo de conclusión, la regla general en nuestro Derecho es la no obligatoriedad de la vacunación, tanto de la vacunación sistemática, entendida como medida de salud pública para prevenir la aparición de enfermedades (meramente recomendada a través del calendario vacunal), como en los casos en los que el riesgo es exclusivamente individual, en ambas situaciones es preciso el consentimiento del interesado o de sus representantes legales.
Excepcionalmente, la Ley Orgánica 3/1986 permite plantear la vacunación con carácter obligatorio en casos de epidemias y crisis sanitarias y riesgo efectivo para la salud pública; en el resto de los casos, en los que el riesgo es exclusivamente individual, solo sería posible obligar a la vacunación siguiendo el art. 9.2 b) Ley 41/2002:
“Cuando existe riesgo inmediato grave para la integridad física o psíquica del enfermo y no es posible conseguir su autorización, consultando, cuando las circunstancias lo permitan, a sus familiares o a las personas vinculadas de hecho a él, sin que resulte de aplicación a estos supuestos de riesgo individual la Ley Orgánica 3/1986".
__________
52 La cuestión dista de estar clara tras la STC 70/2022, de 2 de junio, en Pleno (BOE núm. 159, de 04 de julio de 2022; ECLI:ES:TC:2022:70) que estima la cuestión de inconstitucionalidad promovida respecto de la norma introducida por la ley 3/2020 que sometió a autorización judicial la entrada en vigor y aplicación de las disposiciones sanitarias de alcance general que implicasen privación o restricción de derechos fundamentales, aprobadas por las distintas administraciones para la protección de la salud pública en el marco de las medidas frente al covid-19. El art. 10.8 de la Ley de la jurisdicción contencioso-administrativa, redactado por la disposición final segunda de la Ley 3/2020, de 18 de septiembre, de medidas procesales y organizativas para hacer frente al covid-19 en el ámbito de la Administración de Justicia, fue declarado nulo. El precepto cuestionado atribuía a las Salas de lo Contencioso-administrativo de los Tribunales Superiores de Justicia competencia para la autorización o ratificación judicial de las medidas adoptadas con arreglo a la legislación sanitaria que las autoridades sanitarias autonómicas (o en su caso, locales) considerasen urgentes y necesarias para la protección de la salud pública y que implicasen la limitación o restricción de derechos fundamentales, cuando sus destinatarios no estén identificados individualmente. Con ello, el legislador optaba por la solución de que todas las medidas sanitarias generales que pudieran suponer una injerencia en un derecho fundamental debían contar con la intervención de la voluntad de dos poderes, el ejecutivo y el judicial, para su entrada en vigor y aplicación, de suerte que la autorización judicial se erigía en condición necesaria para otorgar eficacia a esas disposiciones generales en materia de salud pública. La STC aprecia que el precepto cuestionado quebranta el principio constitucional de separación de poderes, al atribuir a los órganos judiciales del orden contencioso-administrativo funciones ajenas a su cometido constitucional (arts. 106.1 y 117 CE), con menoscabo de la potestad reglamentaria que la Constitución atribuye al poder ejecutivo (art. 97 CE), sin condicionarla al complemento o autorización de los jueces o tribunales para entrar en vigor y desplegar eficacia. Añade la sentencia que ese conmixtión de potestades quebranta también el principio de eficacia de la actuación administrativa (art. 103.1 CE) y limita o dificulta igualmente la exigencia de responsabilidades políticas y jurídicas al poder ejecutivo en relación con sus disposiciones sanitarias generales para la protección de la salud pública, en detrimento del principio de responsabilidad de los poderes públicos, consagrado en el art. 9.3 CE. Quiebra, asimismo -concluye la sentencia- los principios constitucionales de publicidad de las normas y de seguridad jurídica (art. 9.3 CE), dado que las resoluciones judiciales que autorizan esas disposiciones generales en materia sanitaria no son publicadas en el diario oficial correspondiente, lo que dificulta el conocimiento por parte de los destinarios de las medidas restrictivas o limitativas de derechos fundamentales a las que quedan sujetos como consecuencia de la autorización judicial de esos reglamentos sanitarios de necesidad.
2.1.3. El debate social sobre la obligatoriedad de las vacunas
| Para imponer la vacunación obligatoria es precisa una ley orgánica, al afectar a derechos fundamentales |
En los apartados anteriores ha quedado expuesto el marco legal que regula la voluntariedad de la vacunación en nuestro país; sin embargo, en los últimos tiempos ya había surgido un intenso debate social sobre si procede introducir cambios normativos que favorezcan la imposición obligatoria de la vacunación en determinados supuestos, tales como enfermedades altamente contagiosas y serias y cuando la erradicación es posible con la adopción de tal medida coercitiva.
Este debate se ha llevado al extremo en la crisis sanitaria provocada por la COVID-19, donde los poderes públicos vienen llevando a cabo intervenciones urgentes que afectan derechos fundamentales y libertades públicas, tales como la libre circulación o la integridad física; se hace preciso, por tanto, ponderar las medidas que se pueden acordar, bajo qué cobertura legal, qué Administración es competente para ello, su extensión en el tiempo, etc.
La falta de una normativa adecuada previa a la pandemia de la COVID-19 impide, en no pocas ocasiones, la adopción de medidas eficaces para dar respuesta a la situación sanitaria, como se ha puesto de manifiesto en el control judicial que de dichas medidas tienen encomendado nuestros Juzgados y Tribunales.
La eventual imposición de la vacunación obligatoria, en la medida en que afecta al derecho fundamental a la integridad física, debería aprobarse mediante una norma con rango de Ley Orgánica. Si bien se puede considerar que la Ley Orgánica 3/1986 y la Ley 41/2002 permitirían imponer una vacunación obligatoria, en función de las excepcionales circunstancias que concurre y de cómo evolucione la enfermedad, sometida al control judicial de proporcionalidad de la medida, al que nos referimos en el apartado 2.1.2.
La Ley 8/2021, de 25 de febrero, de modificación de la Ley 8/2008, de 10 de julio, de salud de Galicia, al imponer sanciones al que se niegue de forma injustificada a vacunarse, ha venido a establecer un sistema que, en opinión de algunos, impone de facto una vacunación obligatoria, con previsión incluso de medidas de compulsión directa sobre las personas, asistidos por fuerzas y cuerpos de seguridad que fuera necesaria para la ejecución de la medida. Dichas medidas han quedado en suspenso, al haberse admitido a trámite recurso de inconstitucionalidad contra las mismas. Para más información, véase el apartado 2.1.1.
| Las coberturas de vacunación en España no justifican la vacunación obligatoria |
En este debate conviene destacar los siguientes documentos:
- Cuestiones ético-legales del rechazo a las vacunas y propuestas para un debate necesario, emitido el 19 de enero de 2016 por el Comité de Bioética de España
- Declaración de la Comisión Central de Deontología de la Organización Médica Colegial (OMC) sobre la vacunación pediátrica, de 8 de febrero de 2016
- Posicionamiento 03/2016 de la Sociedad Española de Salud Pública y Administración Sanitaria (SESPAS), sobre Responsabilidades individuales y colectivas de las instituciones, los profesionales y la población en relación a las vacunas, de 19 de septiembre de 2016
- Estrategia de vacunación frente a COVID19 en España, Grupo de Trabajo Técnico de Vacunación COVID-19, de la Ponencia de Programa y Registro de Vacunaciones, 2 de diciembre 2020 y sucesivas actualizaciones.
- Hasta la fecha se han producido 11 actualizaciones de la Estrategia, la última en febrero de 2022. Cuadro Resumen en el siguiente enlace: https://www.sanidad.gob.es/areas/promocionPrevencion/vacunaciones/covid19/Actualizaciones_Estrategia_Vacunacion/docs/COVID-19_ActualizacionesTablaResumen_EstrategiaVacunacion.pdf
El debate sobre la obligatoriedad de la vacunación se había visto favorecido por las medidas de salud pública adoptadas en Italia (donde se han impuesto 10 vacunas obligatorias y 4 fuertemente recomendadas)53 y Francia (donde se ha establecido la vacunación obligatoria de 11 enfermedades inmunoprevenibles)54. Ambas decisiones se justifican en el alarmante descenso de las tasas de vacunación que se había producido en sus respectivos territorios.
La situación en España, era bien distinta y todos los informes precovid reconocían que las tasas de vacunación en nuestro país eran elevadas hasta 201955, sin embargo la declaración de la pandemia de la COVID-19 por la Organización Mundial de la Salud el 11 de marzo de 2020 y la declaración del estado de alarma en España el 14 de marzo de 2020 supuso una interrupción de la normal prestación de los servicios sanitarios, con el resultado de descensos muy significativos en las tasas de vacunación pediátrica56.
|
Los descensos de las coberturas de vacunación durante la primera etapa de la pandemia se recuperaron durante el verano de 2020 gracias a las administraciones, las sociedades científicas y los profesionales sanitarios |
Con el fin de recuperar las tasas de vacunación, el Ministerio de Sanidad57, las CC. AA.58, las sociedades científicas dictaron diversas recomendaciones para recuperar las tasas de vacunación, pero conviene destacar que esta tarea también es responsabilidad de los profesionales sanitarios, a título individual, así resulta del artículo 4.4. de la Ley 44/2003, de 21 de noviembre, de ordenación de profesiones sanitarias:
“Corresponde a todas las profesiones sanitarias participar activamente en proyectos que puedan beneficiar la salud y el bienestar de las personas en situaciones de salud y enfermedad, especialmente en el campo de la prevención de enfermedades, de la educación sanitaria, de la investigación y del intercambio de información con otros profesionales y con las autoridades sanitarias, para mejor garantía de dichas finalidades”.
| La vacunación frente a la COVID-19 en España es voluntaria, solo sería obligatoria si no se alcanzara la inmunidad de grupo con voluntarios |
Fruto de este esfuerzo conjunto, durante el verano de 2020 se pudo recuperar, en gran medida, la vacunación perdida durante el confinamiento59, y la estrategia de rescate planteada por la AEP sigue dando sus frutos, siendo destacable en adolescentes frente a los meningococos ACWY, que se recomienda en el calendario vacunal oficial y que se interrumpió durante la pandemia60.
De igual modo la percepción de la población sobre la vacuna frente a la COVID-19 es cada vez más favorable donde el grupo que afirmaba que no se pondría la vacuna bajó del 47 % (noviembre de 2020) a un 28 % (enero de 2021)61. Los datos en enero de 2023, reflejan que la campaña de vacunación, incluyendo las dosis de recuerdo y actualizaciones han sido un éxito, como refleja el Informe de actividad GIV-19 (Gestión Integral de la Vacunación)62: el 92,6 % de la población mayor de 12 años tiene la pauta completa de vacunación. Aunque es cierto que la cobertura de población pediátrica (de 5 a 12 años) desciende considerablemente (del 47,5 % con pauta completa, bajaron al 18,4%). El seguimiento durante la campaña 23/24, refleja como datos: 46 % vacunas en mayores de 60 años, que llegan al 64,3 % en mayores de 80 años63.
Tampoco debe olvidarse que las dudas generadas sobre los posibles efectos adversos de la vacuna de AstraZeneca provocó un desplome en la confianza de los ciudadanos64, como ha ocurrido después con otras vacunas. En los últimos meses se han difundido -sobre todo en redes sociales- numerosos comentarios alusivos a un supuesto aumento de los casos de muertes repentinas por eventos cardiacos o cerebrales. Sin embargo, la Agencia Europea de los Medicamentos (EMA) ha confirmado la seguridad global de las vacunas covid65, y son numerosos ya los estudios científicos que confirman que los efectos adversos son siempre mucho menores que los beneficios de la vacunación66.
__________
53 https://vacunasaep.org/profesionales/noticias/italia-hace-obligatorias-10-vacunas.
54 https://vacunasaep.org/profesionales/noticias/francia-tambien-hara-obligatorias-las-vacunas-infantiles.
55 https://vacunasaep.org/profesionales/noticias/cobertura-espana-2018-parte1; https://vacunasaep.org/profesionales/noticias/cobertura-espana-2018-parte2; https://vacunasaep.org/profesionales/noticias/cobertura-espana-2018-parte3;.https://vacunasaep.org/profesionales/noticias/cobertura-espana-2018-parte4 y https://vacunasaep.org/profesionales/noticias/cobertura-espana-2018-parte5.
56 https://vacunasaep.org/sites/vacunasaep.org/files/covid-19-caida-de-las-vacunaciones-sei-seip-aep_24abr2020b.pdf.
57 https://vacunasaep.org/profesionales/noticias/vacunaciones-demoradas-COVID-19-recuperacion.
58 Prioridades del Programa de Vacunaciones durante las fases de transición de la pandemia de Covid-19 https://www.sanidad.gob.es/areas/promocionPrevencion/vacunaciones/covid19/docs/COVID-19_Vacunacionprioritaria2.pdf y https://www.sanidad.gob.es/areas/promocionPrevencion/vacunaciones/covid19/docs/COVID-19_Preguntas_Respuestas_Vacunaciones_MadresPadres.pdf.
59 Andalucía (18 de mayo de 2020): Instrucciones para recuperar las vacunaciones perdidas; Comunidad Valenciana: instrucciones, 27 de mayo de 2020; Castilla y León: nota informativa, 27 de mayo de 2020; Cataluña: nota informativa, 27 de mayo de 2020; cartas (una y dos) dirigidas a las familias, 3 de junio de 2020; Madrid: nota informativa, 28 de mayo de 2020; La Rioja: nota informativa, 7 de junio de 2020.
60 https://www.infosalus.com/asistencia/noticia-asociacion-espanola-pediatria-insta-cumplir-calendario-vacunacion-prevenir-meningitis-20220422105306.html; http://www.medicosypacientes.com/articulo/los-pediatras-destacan-el-esfuerzo-realizado-en-verano-para-recuperar-la-vacunacion-perdida.
61 https://www.elconfidencial.com/espana/2020-12-21/vacuna-covid-coronavirus-cis-encuesta_2880980/. Resultan interesantes los últimos datos del Barómetro Sanitario, febrero 2023, Informe CIS, (pregunta 15 y 15.a), pp.16/17, donde los porcentajes que recogen percepciones sobre falta de seguridad de la vacuna o miedo a los efectos adversos no son elevados.
62 https://www.sanidad.gob.es/profesionales/saludPublica/ccayes/alertasActual/nCov/documentos/Informe_GIV_comunicacion_20230331.pdf.
63 https://web.mscbs.gob.es/areas/alertasEmergenciasSanitarias/alertasActuales/nCov/documentos/Informe_GIV_Comunicacion_25012024.pdf.
64 https://www.elconfidencial.com/mundo/europa/2021-03-22/la-confianza-en-la-vacuna-de-astrazeneca-se-hunde-en-europa-tras-las-suspensiones_3000752/.
65 https://vacunasaep.org/profesionales/noticias/vacuna-covid-astrazeneca-EMA-confirma-balance-favorable#:~:text=La%20EMA%20asegura%20que%20la,%2C%2018%2Fmar%20de%202021.
66 https://cuidateplus.marca.com/bienestar/2023/01/15/hay-mas-infartos-e-ictus-son-evidencias-supuestas-repentinitis-180285.html.
2.2. ¿Cuál es el procedimiento administrativo y judicial para imponer la vacunación obligatoria?
| La administración solo puede imponer vacunación obligatoria previa autorización judicial, en la vía contencioso-administrativa |
La Administración solo puede imponer la vacunación obligatoria, previa autorización judicial. Según nuestro Tribunal Constitucional, la adopción de medidas coercitivas que puedan comprometer la integridad física exige:
- Que se persiga un fin constitucionalmente legítimo, en este caso, el derecho a la protección integral de la salud que se consagra en el art. 43 de la Constitución.
- Que su decisión venga amparada por una norma con rango de ley (principio de legalidad), en este sentido el art. 3 de la Ley Orgánica 3/1986 permite adoptar “cualquier medida apropiada”.
- Respeto al principio de proporcionalidad: idoneidad, necesidad y proporcionada en sentido estricto.
- Que sea acordada por la autoridad judicial. En la situación precovid eran muy escasos los supuestos en que los Juzgados y Tribunales hacían uso de esta potestad por motivos de salud pública siendo, en cambio, más frecuentes los supuestos de internamientos forzosos por razones psiquiátricas. Sin embargo, la frecuencia e intensidad de intervenciones en materia de salud pública que llevaron a cabo las distintas administraciones competentes con ocasión de la pandemia, han cambiado la práctica de nuestros Juzgados y Tribunales en la materia, obligando a introducir reformas legales de calado.
Si la obligación de vacunación viene impuesta por una administración pública, la jurisdicción competente en la materia es la contencioso-administrativa, regulada en la Ley 29/1998, de 13 de julio, Reguladora de la Jurisdicción Contencioso-Administrativa (en adelante, LJCA)67.
En base al art. 8.6 párrafo segundo LJCA:
“Asimismo, corresponderá a los Juzgados de lo Contencioso-administrativo la autorización o ratificación judicial de las medidas adoptadas con arreglo a la legislación sanitaria que las autoridades sanitarias consideren urgentes y necesarias para la salud pública e impliquen limitación o restricción de derechos fundamentales cuando dichas medidas estén plasmadas en actos administrativos singulares que afecten únicamente a uno o varios particulares concretos e identificados de manera individualizada”.
No se concreta en la norma cuál es el procedimiento judicial que debe seguirse para acordar la medida coactiva de vacunación obligatoria, si bien se viene aplicando con carácter analógico el procedimiento previsto en el art. 763 de la Ley de Enjuiciamiento Civil, relativo al internamiento no voluntario por razón de trastorno psiquiátrico, que exige la autorización judicial previa a la adopción de la medida, salvo razones de urgencia que exijan la inmediatez de la medida y posterior ratificación del juez68.
A estos condicionantes se añade, según el Tribunal Constitucional, una última limitación “La ejecución de tales intervenciones corporales se habrá de efectuar por personal sanitario que deberá ser personal médico especializado en el supuesto de intervenciones graves que lo requieran por sus características” y “la práctica de la intervención se ha de llevar a cabo con respeto de la dignidad de la persona, sin que en ningún caso pueda constituir, en sí misma o por la forma de realizarla, un trato inhumano o degradante, aspectos éstos sobre los que pesa una prohibición absoluta (arts. 10.1 y 15 CE)”.
__________
67 En plena pandemia de Covid, la LJCA fue modificada por la Ley 3/2020, de 18 de septiembre, de medidas procesales y organizativas para hacer frente a la COVID-19 en el ámbito de la Administración de Justicia.
La reforma pretendía ajustar la competencia de los órganos jurisdiccionales en atención a la naturaleza del acto administrativo, el ámbito de la autoridad administrativa del que emana y la identificación de los afectados, con la finalidad de que las Salas de lo Contencioso-Administrativo establecieran criterios uniformes en relación con las medidas de salud pública que dictaban las autoridades sanitarias competentes en la pandemia de covid, lo cual no impidió pronunciamientos judiciales dispares sobre la legalidad de dichas medidas, con gran incertidumbre entre la ciudadanía.
Sin embargo, dicha modificación se vio afectada por la Sentencia del Tribunal Constitucional 70/2022, de 2 de junio, Pleno, cuestión de inconstitucionalidad núm. 6283/2020, BOE 4 julio 2022, en la que se declara la inconstitucionalidad y consiguiente nulidad de los artículos 10.8 y 11.1 i) y del inciso «10.8 y 11.1 i)» del art. 122 quater, todos ellos de la LJCA, en la redacción dada por la DF segunda de la Ley 3/2020, de 18 de septiembre, de medidas procesales y organizativas para hacer frente a la COVID-19 en el ámbito de la administración de justicia, al entender el Tribunal Constitucional que dichos preceptos son contrarios a la división de poderes.
La potestad reglamentaria se atribuye por la Constitución (y por los estatutos de autonomía, en su caso) al Poder Ejecutivo de forma exclusiva y excluyente, por lo que no cabe que el legislador la convierta en una potestad compartida con el Poder Judicial, lo que sucede si se sujeta la aplicación de las normas reglamentarias al requisito previo de la autorización judicial.
Se quebranta también el principio de eficacia de la actuación administrativa y limita o dificulta igualmente la exigencia de responsabilidades políticas y jurídicas al Poder Ejecutivo en relación con sus disposiciones sanitarias generales para la protección de la salud pública, en detrimento del principio de responsabilidad de los poderes públicos. Quiebra, asimismo, los principios constitucionales de publicidad de las normas y de seguridad jurídica, dado que las resoluciones judiciales que autorizan, en todo o en parte, esas disposiciones generales en materia sanitaria no son publicadas en el diario oficial correspondiente, lo que dificulta el conocimiento por parte de los destinarios de las medidas restrictivas o limitativas de derechos fundamentales a las que quedan sujetos como consecuencia de la autorización judicial de esos reglamentos sanitarios de necesidad.
68 Se declara la inconstitucionalidad de los incisos destacados del apartado 1 por SSTC 131/2010 y 132/2010, de 2 de diciembre (Ref. BOE-A-2011-274), por razones formales, al no estar regulada la materia por Ley Orgánica, si bien no se declara la nulidad de los referidos incisos para evitar un vacío indeseable en el Ordenamiento jurídico, máxime no habiéndose cuestionado su contenido material, hasta que el Legislador, proceda a regular la medida de internamiento no voluntario por razón de trastorno psíquico mediante ley orgánica, tarea aún pendiente de llevar a cabo, como reitera la STC 141/2012, de 2 de julio. Sobre la STC 141/2012, de 2 de julio, en la que el TC analiza sistemáticamente las garantías de los ingresos psiquiátricos urgentes, véase El ingreso psiquiátrico involuntario de carácter urgente: una revisión tras la STC 141/2012, de 2 de julio.
2.3. ¿En qué supuestos vienen exigiendo nuestros juzgados y tribunales la vacunación obligatoria?
Tal y como se ha expuesto en el apartado anterior, la Administración sólo puede imponer la vacunación con carácter obligatorio previa autorización judicial. ¿En qué casos han obligado nuestros juzgados y tribunales a vacunar?
| En 2010 un juzgado de Granada obligó a vacunar a un colectivo de niños en un brote de sarampión |
Aludiremos, en primer lugar a la Sentencia de la Sala de lo Contencioso-Administrativo de la Audiencia Nacional de 29 de octubre de 2010 cuando afirma que “fuera de estos casos (se refiere la Sentencia a la vacunación obligatoria respecto de sujetos en los que concurre una relación de especial sujeción militares, profesionales sanitarios- o en supuestos muy concretos como son los viajes al extranjero a la entrada en España), sólo cabría justificarla en una situación extraordinaria, amparado en la LO 3/1986, que excepcione el principio general de autonomía deducible del artículo 10.9 LGS y de la Ley 41/2002, de 14 de noviembre, no tanto del paciente, como del ciudadano a la hora someterse a tratamientos preventivos y que en este caso sería una vacuna69.
El supuesto más conocido es el Auto del Juzgado de lo Contencioso-Administrativo número 5 de Granada, de 24 de diciembre de 2010, en el que se abordaba un brote de sarampión en un Colegio Público del Barrio del Albaicín en Granada, donde se detectaron 36 casos confirmados a 18 de noviembre de 2010, pese a lo cual algunos padres se negaban a vacunar a sus hijos, lo que hacía imposible proteger a niños menores de 12/15 meses (no pueden ser vacunados por edad) y a los adultos susceptibles de contagiarse.
Ante esta situación la Consejería de Salud de la Junta de Andalucía solicitó al Juzgado la vacunación forzosa de los 35 niños cuyos padres se negaban a autorizar la vacunación. El Auto judicial procedió a autorizar la vacunación obligatoria con la siguiente argumentación: “Entendemos que no suscita debate que la medida solicitada por la Consejería de Salud de la Junta de Andalucía persigue un fin constitucionalmente legítimo; que su adopción se encuentra amparada por una norma de rango legal; y que existe proporcionalidad de la medida de manera que es idónea y necesaria a los fines constitucionalmente legítimos que se pretenden, sin implicar un sacrificio desmedido…“, debiendo llevarse a cabo la vacunación en el Colegio Público, en el Centro de Salud o en el domicilio de los menores, por personal sanitario especializado, sin que pueda en ningún caso constituir, por la forma de realizarla, un trato inhumano o degradante, pudiendo la Autoridad Sanitaria requerir el auxilio de las Fuerzas y Cuerpos de Seguridad del Estado, si fuere necesario.
| Los juzgados avalan la negativa a admitir en guarderías infantiles a niños que no están vacunados, pero no se les obliga a que se vacunen |
Otros pronunciamientos judiciales a destacar son aquellos en las que se analizan las consecuencias de la decisión de no vacunar en relación con la admisión en centros educativos:
- Sentencia del Tribunal Superior de Justicia de Cataluña, Sala de lo Contencioso-Administrativo, de 28 de marzo de 2000, en la que se impugnaba la resolución de la Universidad Autónoma de Barcelona (UAB) dejando sin efecto la matrícula de una menor en una Escola Bressol vinculada a la UAB por la negativa de los padres a que se le inoculara cualquier tipo de vacuna, entendiendo la Sala que la anulación de la matrícula no vulnera el derecho a la educación: "Así pues, no estamos aquí ante una vulneración del derecho a la educación, de lo que es buena prueba la admisión de la menor en la escuela, sino ante el incumplimiento de unas obligaciones que tienen como finalidad la prevención de enfermedades, y que se traducen en la práctica en la exigencia de acreditar las vacunaciones sistemáticas que le corresponden por su edad, que responden a la idea de obtener una inmunidad del grupo que, además de proteger del contagio a los individuos no vacunados por contraindicaciones individuales, permite la eliminación de la enfermedad de un área geográfica determinada, e incluso a nivel mundial”.
- Sentencia del Tribunal Superior de Justicia de la Rioja, Sala Contencioso Administrativo, 2 de abril de 2002, en la que se impugnaba la Resolución de la Comunidad Autónoma dejando sin efecto la concesión de una plaza en una guardería infantil a una menor al incumplir los requisitos de vacunación necesarios para su admisión “nada impide tal opción alternativa y nada obliga a una vacunación que decididamente se rechaza. No puede desconocerse la potestad de la Administración para imponer tal exigencia a quien pretenda acogerse a los servicios de Guardería, negando la admisión a los niños que no la cumplan, dado que la medida profiláctica aplicada resulta sanitariamente recomendable para la salud de todos los componentes del grupo. … resultó conforme a Derecho denegar la admisión de éste a la guardería infantil si se incumplió el requisito del sometimiento a la vacunación oficial normativamente impuesta a tal fin”.
En ambos supuestos, si bien no se puede imponer la vacunación al menor cuyos padres no prestan su autorización, se declara ajustado a Derecho no permitir la incorporación del menor no vacunado a la actividad educativa.
Más recientemente, la Sentencia del Juzgado de lo Contencioso Administrativo-Barcelona, Sección 16, Rec. 241/2018, de 28 de Diciembre de 2018, en un Procedimiento especial de derechos fundamentales70, en el que se impugna la resolución del Ayuntamiento de Barcelona por la que se deniega la solicitud de tramitación de la inscripción en la escuela cuna del hijo menor de la recurrente, entiende que con la citada resolución no se vulnera la libertad ideológica (art. 16 CE), pues nadie ha obligado a vacunar al niño, ni atenta contra la dignidad de la persona (art. 10 CE), ni contra la integridad física y moral (art. 15), ni la prohibición de discriminación (art. 14 CE).
En síntesis, entiende la sentencia, la actora no pretende que su opción minoritaria sea respetada, que ya lo es por cuanto de lege data no resulta obligatoria la vacunación, sino que el resto de familias y niños pequeños asuman las consecuencias y riesgos de su decisión unilateral, riesgo para la salud y la vida. En definitiva, como expone la demandada, la actora pretende que el conjunto de los niños y familias usuarias de aquella escuela cuna, asuman el riesgo de ir en contra de aquello que el conocimiento científico ha expuesto sobre el estado fisiológico de la enfermedad o la muerte, por una creencia subjetiva de la recurrente, que se le respeta, si bien el resto de los niños no han de asumir la carga negativa de dicha decisión.
Finalmente, se considera que la resolución recurrida no incurre en arbitrariedad, entendiendo que no se cumplimenta el requisito de aportar la cartilla de vacunación si la que se aporta no está completada, tal y como pretende el recurrente.
En esta línea se enmarca la propuesta aprobada en el Ayuntamiento de Barcelona para estudiar la obligatoriedad de estar al día de vacunas para acceder a las guarderías públicas71. Castilla y León, Extremadura y Galicia ya exigen que los niños estén vacunados para acceder a sus escuelas infantiles públicas72.
Ya hay países de nuestro entorno donde se está condicionando el acceso a las guarderías a que los niños estén vacunados73, o en Italia, donde los niños de hasta los 6 años de edad, nacidos a partir de 2017, deberán acreditar estar vacunados (o una condición eximente aceptada) para acceder a los centros escolares públicos y privados. La falta de cumplimiento de este requisito puede conllevar sanciones económicas74.
Esas intervenciones judiciales es cierto que se venían produciendo de forma esporádica y muy excepcional, sin embargo con la pandemia de la COVID-19 es frecuente que se someta a la decisión judicial medidas de salud pública adoptadas por las autoridades, en sus respectivos ámbitos de competencia, sin que nos corresponda a nosotros analizar las relativas a limitaciones de movilidad, confinamientos, toques de queda, actividades permitidas, etc., por exceder del objeto del presente capítulo.
__________
69 https://dialnet.unirioja.es/servlet/articulo?codigo=6295147.
70 https://www.iberley.es/jurisprudencia/sentencia-administrativo-jca-barcelona-sec-16-rec-241-2018-28-12-2018-47983816.
71 https://www.redaccionmedica.com/autonomias/cataluna/barcelona-estudiara-obligar-a-vacunarese-a-los-ninos-que-vayan-a-guarderias-6373.
72 https://elpais.com/sociedad/2019/02/27/actualidad/1551287158_737804.html.
73 https://www.elconfidencial.com/mundo/2018-08-27/holanda-medidas-antivacunas-guarderias_1608255/.
74 https://vacunasaep.org/profesionales/noticias/italia-hace-obligatorias-10-vacunas.
2.4. Si un profesional sanitario trabaja en unidades de riesgo, por ejemplo con inmunodeprimidos, ¿puede ser obligado a vacunarse? ¿En caso de no vacunarse, se le puede impedir al profesional sanitario el acceso a ese puesto de trabajo?
| No hay vacunación obligatoria de los sanitarios en España, salvo casos de epidemia y grave riesgo para la salud pública |
La profesiones sanitarias constituyen un grupo de riesgo, motivo por el que forman un grupo diana en materia de vacunación, tanto por razones de salud pública (protegerlos del riesgo de contraer determinadas enfermedades, evitar que puedan ser fuente de contagio para terceros y, por último, colaborar en la aplicación del calendario vacunal) como de salud laboral (protegerlos del riesgo de la exposición al contagio o complicaciones de la adquisición de enfermedades infecciosas en el lugar de trabajo y evitar el absentismo por adquisición de enfermedades infecciosas en el desempeño de sus funciones).
Sin embargo, las tasas de vacunación de los profesionales son muy bajas, fundamentalmente por razones culturales, la baja percepción del riesgo de la enfermedad, las dudas sobre la efectividad de las vacunas de algunos profesionales y, finalmente, porque no hay ninguna norma que imponga la vacunación, siendo sólo obligatoria cuando sea preciso para proteger la salud pública en caso de necesidad y cuando haya grave riesgo para la salud de la población.
La cuestión es si los empleados públicos se encuentran en una situación diferente a la del resto de ciudadanos, por su especial función de servicio a los intereses generales75. Y, en concreto, si esa mayor vinculación con el bien común o colectivo les afecta solo en el ejercicio de sus funciones o puede extenderse a otras facetas de su vida personal. Esto es, si conlleva obligaciones particulares de forma que sus derechos fundamentales puedan verse limitados o modulados de forma más intensa que el resto de ciudadanos, fruto de la relación de sujeción especial (que define la situación jurídica de los funcionarios como un estatus de libertad limitada o dependencia acentuada). Aunque esta tesis es aceptada doctrinalmente e incluso la jurisprudencia acude a ella en ocasiones para justificar límites al ejercicio de los derechos fundamentales, la vis expansiva de estos debe primar sobre cualquier restricción del «status libertatis» común aplicada a los servidores públicos .
De manera que los derechos de los empleados públicos solo pueden ceder de manera proporcionada en la medida que lo exigieran las necesidades del servicio o la realización de concretas actividades públicas, en su deber de actuar con eficacia, velar por la consecución del interés general y por «el cumplimiento de los objetivos de la organización» (art. 53.8 del Real Decreto Legislativo 5/2005 por el que se aprueba el Texto Refundido del Estatuto Básico del Empleado Público, en adelante, TREBEP).
De modo específico, el art. 54.9 impone la observancia de las normas sobre seguridad y salud laboral, recogidas en la Ley 31/1995, de 8 de noviembre en materia de salud en el trabajo y prevención de riesgos laborales, aplicable también en el ámbito de la función pública (art. 3), cuyo art. 29.l establece:
«corresponde a cada trabajador velar, según sus posibilidades y mediante el cumplimiento de las medidas de prevención que en cada caso sean adoptadas, por su propia seguridad y salud en el trabajo y por la de aquellas otras personas a las que pueda afectar su actividad profesional, a causa de sus actos y omisiones en el trabajo». El art. 29.3 de esta misma Ley señala las posibles sanciones por el incumplimiento de este deber general «a los efectos previstos en el art. 58.1 del Estatuto de los Trabajadores o de falta, en su caso, conforme a lo establecido en la correspondiente normativa sobre régimen disciplinario de los funcionarios públicos o del personal estatutario al servicio de las Administraciones Públicas».
Existen, pues, unos deberes de protección de la salud que también el empleado público debe cumplir, no solo por su interés, sino también por las personas a las que pueda afectar su actividad en el servicio, sean compañeros o usuarios de servicios públicos, fundamentalmente en la sanidad, donde se pueden ver afectados, sin posibilidad de elección, por la actitud del funcionario respecto a su salud.
__________
75 El art. 53.2 del Estatuto Básico del Empleado Público señala como principio ético del «código de conducta» sancionado legalmente: «su actuación perseguirá la satisfacción de los intereses generales de los ciudadanos…al margen de cualquier otro factor que exprese posiciones personales, familiares, corporativas, clientelares o cualesquiera otras que puedan colisionar con este principio»
| No procede actualmente sanción alguna al sanitario que, en ejercicio de su autonomía, decide no vacunarse, ni siquiera en unidades de alto riesgo, aunque en situaciones excepcionales cabría la aplicación del régimen disciplinario de los empleados públicos, e incluso medidas relacionadas con el traslado de puesto de trabajo |
La vacunación es, como para cualquier ciudadano, un derecho también para el profesional sanitario, en este sentido la Ley 33/2011, 4 de octubre, General de Salud Pública establece que la participación en las actuaciones de salud pública será voluntaria salvo lo previsto en la Ley Orgánica 3/1986 de Medidas Especiales en Materia de Salud Pública. Sin embargo, aunque no exista un deber legal específico de vacunación de los empleados públicos, las leyes citadas permitirían exigirla si fuera necesario para reducir el riesgo de transmisión de enfermedades infecciosas. Ahora bien, tratándose de una medida que puede colisionar con derechos fundamentales individuales, habría que respetar las reglas de necesidad, idoneidad y proporcionalidad que la jurisprudencia exige (por todas, STC 172/2020, de 22 de diciembre76).
Ello no obstante hay que tener en cuenta que:
- La Ley 55/2003 de 16 de diciembre del Estatuto Marco del Personal Estatutario de Servicios de Salud, incluye como deber «cumplir las normas relativas a la seguridad y salud en el trabajo, así como las disposiciones adoptadas en el centro sanitario en relación con esta materia» (art. 19.m).
Por tanto, no existe tampoco para los profesionales sanitarios un deber de vacunación pero, con arreglo a las disposiciones generales y esta específica, la Administración podría llegar a imponerlo. En favor del deber de vacunación opera, desde una perspectiva ética y deontológica, el principio general de no maleficencia que rige las profesiones sanitarias («primum non nocere»), reflejado en deberes básicos cuyo incumplimiento puede acarrear algún tipo de responsabilidad. Así, el deber de colaboración en situaciones de urgencia o necesidad (art. 19.f EMPS). O por oponerse a las medidas de vigilancia de la salud (art. 22 LGSP).
- Ley 33/2011 General de Salud Pública impone en su art. 8 a todos los ciudadanos un deber de colaboración en salud pública, absteniéndose de realizar conductas que dificulten, impidan o falseen su ejecución; con mayor motivo deben colaborar los profesionales sanitarios. También la oposición a las medidas de vigilancia de la salud podría suponer responsabilidades (art.22 LGSP).
Como expresamente sancionan las normas relativas a la seguridad y salud en el trabajo:
- La Ley 31/1995, de 8 de noviembre, de prevención de Riesgos Laborales, establece las obligaciones de la empresa para garantizar la salud y seguridad de los trabajadores en relación con los riesgos derivados del trabajo, en concreto, el art. 22 “Vigilancia de la salud”, establece que:
- El empresario garantizará a los trabajadores la vigilancia periódica de su estado de salud en función de los riesgos inherentes al trabajo
- Esta vigilancia sólo podrá llevarse a cabo cuando el trabajador preste su consentimiento. De este carácter voluntario sólo se exceptuarán, previo informe de los representantes de los trabajadores, los supuestos en los que la realización de los reconocimientos sea imprescindible para evaluar los efectos de las condiciones de trabajo sobre la salud de los trabajadores o para verificar si el estado de salud del trabajador puede constituir un peligro para el mismo, para los demás trabajadores o para otras personas relacionadas con la empresa o cuando así esté establecido en una disposición legal en relación con la protección de riesgos específicos y actividades de especial peligrosidad
- Los riesgos biológicos inherentes a la actividad sanitaria permiten sostener que estamos ante uno de los supuestos de excepción a la voluntariedad del reconocimiento médico de salud para los profesionales sanitarios
- Por otra parte, el Real Decreto 664/1997, de 12 de mayo sobre la protección de los trabajadores contra los riesgos relacionados con la exposición a agentes biológicos durante el trabajo, establece en su art. 8.3, relativo a la vigilancia de la salud de los trabajadores, que:
- Cuando exista riesgo por exposición a agentes biológicos para los que haya vacunas eficaces, éstas deberán ponerse a disposición de los trabajadores, informándoles de las ventajas e inconvenientes de la vacunación.
- Cuando los empresarios ofrezcan las vacunas deberán tener en cuenta las recomendaciones prácticas contenidas en el anexo VI de este Real Decreto77.
Lo dispuesto en el párrafo anterior será también de aplicación en relación con otras medidas de preexposición eficaz que permitan realizar una adecuada prevención primaria. El ofrecimiento al trabajador de la medida correspondiente, y su aceptación de la misma, deberán constar por escrito.
Se establece pues en el citado Real Decreto, la información y puesta a disposición de las vacunas existentes, sin que de dicha norma pueda deducirse obligatoriedad alguna de vacunación de los profesionales sanitarios.
- También el Real Decreto 592/2014, de 11 de julio, por el que se regulan las prácticas académicas externas de los estudiantes universitarios, que se acogerán a las leyes de los trabajadores sanitarios durante la realización de las prácticas en centro sanitarios. El art. 9.f) establece el derecho de los estudiantes en prácticas académicas externas: a recibir, por parte de la entidad colaboradora, información de la normativa de seguridad y prevención de riesgos laborales.
- Real Decreto 39/1997, de 17 de enero, por el que se aprueba el Reglamento de los Servicios de Prevención, en cuanto encargados de la captación, indicación, vacunación y registro de las vacunas administradas a los profesionales sanitarios.
- En fin, la Orden ESS/1451/2013, de 29 de julio, por la que se establecen disposiciones para la prevención de lesiones causadas por instrumentos cortantes y punzantes en el sector sanitario y hospitalario, dispone en su artículo 6: 3. Si la evaluación mencionada en el artículo 5 revela que existe un riesgo para la salud y la seguridad de los trabajadores debido a la exposición a agentes biológicos para los que existen vacunas eficaces, la vacunación debe ser ofrecida a dichos trabajadores. 4. La vacunación y, si fuera necesario, su recordatorio se debe realizar conforme a la legislación y a las recomendaciones de las autoridades sanitarias, incluyendo la determinación del tipo de vacunas. a) Se debe informar a los trabajadores de los beneficios y desventajas de la vacunación y de la no vacunación, incluyendo el posible impacto en su salud y en la de su entorno. b) La vacunación debe ofrecerse de manera gratuita a todos los trabajadores y a los estudiantes que realicen actividades sanitarias y afines en el lugar de trabajo. En el caso de no aceptación de la vacunación ofertada deberá quedar constancia escrita de esta decisión.
La Orden plantea, una vez más, el ofrecimiento de la vacunación a los trabajadores sanitarios, con información de riesgos y beneficios, de forma gratuita y dejar constancia escrita, en su caso, de la negativa del profesional sanitario a la vacunación. En este sentido, la Comisión de Salud Pública del Consejo Interterritorial del Sistema Nacional de Salud, publicó en 2001 un Protocolo de Vigilancia Sanitaria para Agentes Biológicos en el que, tras recomendar las vacunas que, como norma general, se han de administrar al personal sanitario, establece que: Los trabajadores que rechacen la vacunación deben dejar constancia escrita de la negativa en su ficha personal, en cuyo cayo se valorará el NO APTO. Sin embargo, dichos protocolos carecen de carácter vinculante y son meras recomendaciones; de modo que una eventual calificación de no apto de un trabajador sanitario para prestar servicios en una determinada unidad debería ser sometida a autorización judicial.
Llegados a este punto, hay que preguntarse qué tipo de medidas podría adoptar la Administración si un empleado público se niega a vacunarse, si esta fuera impuesta obligatoriamente. Como propone SÁNCHEZ MORÓN78, cabría el traslado forzoso del empleado siempre que se justificara la incompatibilidad con la garantía efectiva de protección de la salud en un puesto de trabajo especialmente sensible (pensemos en una unidad de cuidados intensivos o una estancia de enfermos Covid), siempre respetando sus retribuciones y condiciones esenciales de trabajo (art. 81.2 EBEP).
Pero, ¿sería posible tomar alguna medida disciplinaria, en situaciones de urgencia o necesidad, contra quienes se nieguen alegando únicamente su libertad de decisión?
Dado su deber de colaboración en materia de salud pública y en salud laboral, podría abrirse un expediente disciplinario por falta prevista en el art. 72 del EMPS79. Finalmente, aunque la LGSP no incluyó el deber del profesional no vacunado de informar al paciente, pensamos que una correcta información al respecto y la aceptación de los riesgos, o la negativa del paciente a ser tratado por ese profesional, mitigaría o eliminaría la posible responsabilidad80.
Aunque no se trate propiamente de un profesional sanitario, es importante la Sentencia de la Sala de lo Social, Sección 1.ª del TSJ de País Vasco, núm.. 897/2022 de 10 mayo (ECLI:ES:TSJPV:2022:1915), donde se considera nulo el despido de una trabajadora de un centro residencial de ancianos y personas dependientes por su negativa a ser vacunada de la covid. La sentencia entiende violentado el derecho fundamental a la integridad física (art.15 CE), insistiendo además en la inexistencia de una normativa expresa que imponga la vacunación:
“ Aunque el recurso, ciertamente, no incide sobre la repercusión de la quiebra del derecho a la integridad de la trabajadora, pues exclusivamente cuestiona el que exista un panorama indiciario, es lo cierto que el trabajador, en términos generales y aproximativos, no puede ser obligado a vacunarse, pues el art. 15 CE ha tenido una interpretación por el TC que señala que el derecho a la integridad física y moral no consiente el que se imponga a alguien una asistencia médica en contra de su voluntad, cualesquiera que fueren los motivos de la negativa a ello de la persona. La negativa y oposición a un tratamiento es admisible y violentar la expresión contraria a la aplicación del mismo supone una agresión de tal envergadura que no es justificable ni se ampara en un posible efecto curativo porque la decisión a someterse siempre es libre y personalísima, formando parte inescindible de la protección de la salud…
… Si la causa del despido ha sido la no vacunación de la trabajadora, su negativa a recibir el tratamiento de vacunación, la imposición obligatoria de la vacunación y la censura a la actuación persistente de la actora de negarse a su recepción, con el resultado ante esta posición de la actora de la articulación del despido disciplinario, con ello lo que acontece es que se está afectando a la esfera de un derecho fundamental, como es la integridad física.
Hoy por hoy, y careciéndose de una normativa expresa que imponga la vacunación, se mantiene el derecho de toda persona a negarse a la misma”.
También resulta importante recordar que, respecto al derecho a la vacunación de los profesionales sanitarios resulta discriminatorio primar a los que trabajan en centros públicos y privados, como nos ha recordado la Sentencia TSJ de C. Valenciana, (Sala de lo Contencioso-Administrativo, Sección 4.ª) Sentencia num. 293/2022 de 1 septiembre. Se entiende vulnerado el derecho a la salud, incluso a la vida e integridad física derivada de la inactividad administrativa por no vacunar al personal sanitario que ejercía su actividad en la medicina privada en la provincia de Alicante: aun cuando existiera insuficiencia de vacunas para poder vacunar a todos los sanitarios que se pudieran contagiar por el virus, para la Sala no tiene ninguna justificación ni admite paliativos ni excusas la prioridad que se estableció en este caso en el tratamiento inmunizatorio en favor de los sanitarios públicos con perjuicio y detrimento de los privados: la insuficiencia de vacunas era una circunstancia totalmente prevista e insuperable, existiendo un desabastecimiento de ese tipo de medicinas en el mercado ante una demanda abrumadora de vacunas a nivel mundial imposible de atender, pero esta escasez no puede servir de coartada para desatender a los sanitarios privados sometidos a los mismos riesgos que los sanitarios públicos.
Para terminar, recordemos que la obligatoriedad de vacunación para los profesionales sanitarios tanto en la red sanitaria como en centros o residencias de ancianos, se puso en marcha en Grecia y Francia ante el incremento de contagios por la variante Delta a mediados del año 202181, y que el TEDH avaló la constitucionalidad de esta medida para el colectivo de bomberos franceses.
__________
76 Esta importante sentencia aplicó estos estándares al valorar la constitucionalidad de diversos preceptos de la Ley Orgánica de Protección de la Seguridad Ciudadana que permitían adoptar medidas coercitivas de libertad individual, señalando que en todo caso debían sujetarse al principio de proporcionalidad para ser legítimas.
77 ANEXO VI Recomendaciones prácticas para la vacunación:
- Cuando la evaluación a que se refiere el artículo 4 demuestre la existencia de un riesgo para la seguridad y la salud de los trabajadores por exposición a agentes biológicos contra los que existan vacunas eficaces, el empresario deberá ofrecer dicha vacunación
- Deberá informarse a los trabajadores sobre las ventajas e inconvenientes tanto de la vacunación como de la no vacunación
- La vacunación ofrecida a los trabajadores no acarreará a éstos gasto alguno
- Podrá elaborarse un certificado de vacunación que se expedirá al trabajador referido y, cuando así se solicite, a las autoridades sanitarias
- Lo dispuesto en los apartados anteriores será de aplicación a las medidas a las que se refiere el segundo párrafo del apartado 3 del artículo 8
78 SÁNCHEZ MORÓN, M., «Sobre la exigibilidad de vacunación para los empleados públicos», en Revista El Cronista del Estado Social y democrático de Derecho, núm. 93-94, abril-mayo 2021, págs. 33 y 34.
79 La clasificación es la siguiente:
- Muy graves: «i) La negativa a participar activamente en las medidas especiales adoptadas por las Administraciones públicas o servicios de salud cuando así lo exijan razones sanitarias de urgencia o necesidad. u) La negativa expresa a hacer uso de los medios de protección disponibles y seguir las recomendaciones establecidas para la prevención de riesgos laborales, así como la negligencia en el cumplimiento de las disposiciones sobre seguridad y salud en el trabajo por parte de quien tuviera la responsabilidad de hacerlas cumplir o de establecer los medios adecuados de protección»;
- Graves: «m) La negligencia en la utilización de los medios disponibles y en el seguimiento de las normas para la prevención de riesgos laborales, cuando haya información y formación adecuadas y los medios técnicos indicados, así como el descuido en el cumplimiento de las disposiciones sobre seguridad y salud en el trabajo por parte de quien no tuviera la responsabilidad de hacerlas cumplir o de establecer los medios adecuados de protección»;
- Leves: «f) El incumplimiento de sus deberes u obligaciones, cuando no constituya falta grave o muy grave»El Anteproyecto de LGSP establecía al respecto (art. 69.6) que: “Los profesionales sanitarios tienen absoluta libertad en decidir si se vacunan o no frente a enfermedades que pueden transmitir a los pacientes e incluso de aquellas que transmitidas a ciertos pacientes pueden acarrearles consecuencias graves. Esta libertad acarrea la necesidad ineludible de que estos profesionales informen de su situación de no vacunación y adopten medidas de prevención adecuadas durante los periodos en que la enfermedad objeto de vacunación es prevalente. Una vez informados, los pacientes pueden decidir que ese personal sanitario no les atienda".
80 El Anteproyecto de LGSP establecía al respecto (art. 69.6) que: “Los profesionales sanitarios tienen absoluta libertad en decidir si se vacunan o no frente a enfermedades que pueden transmitir a los pacientes e incluso de aquellas que transmitidas a ciertos pacientes pueden acarrearles consecuencias graves. Esta libertad acarrea la necesidad ineludible de que estos profesionales informen de su situación de no vacunación y adopten medidas de prevención adecuadas durante los periodos en que la enfermedad objeto de vacunación es prevalente. Una vez informados, los pacientes pueden decidir que ese personal sanitario no les atienda".
81 https://www.redaccionmedica.com/secciones/sanidad-hoy/francia-y-grecia-imponen-la-vacuna-obligatoria-de-covid-a-todos-sus-medicos-2199. Con estas decisiones, de junio de 2021, se sigue el ejemplo de Italia o Gran Bretaña que ya tomaron esta decisión para algunos de sus colectivos sanitarios, entre mayo y junio. https://www.elperiodico.com/es/sociedad/20210712/paises-obligatoria-vacuna-covid-19-11903169.
3. Información y consentimiento informado en vacunas
3.5.1. ¿Los padres pueden negarse a vacunar a sus hijos?
3.6.1. Consentimiento por representación y patria potestad
3.6.2. La casuística entre los progenitores respecto a la vacunación de sus hijos menores
3.1. ¿Quién debe informar sobre las vacunas pediátricas a los padres? ¿Es válido el prospecto a estos efectos?
La Ley 41/2002 dispone en su art. 2.6 que:
“Todo profesional que interviene en la actividad asistencial está obligado no sólo a la correcta prestación de sus técnicas, sino al cumplimiento de los deberes de información y de documentación clínica, y al respeto de las decisiones adoptadas libre y voluntariamente por el paciente”.
Se impone así para los profesionales el deber de cumplir no sólo la lex artis material, concretada en la correcta prestación de las técnicas médicas propias de cada especialidad, sino también la lex artis formal, integrada por el cumplimiento de los deberes de información y documentación clínicas y el respeto a la autonomía de la voluntad del paciente; ambas manifestaciones de la lex artis se colocan en un plano de igualdad y vinculan por igual a los profesionales.
Tal y como establece el Tribunal Constitucional (Sentencia 37/2011, de 28 de marzo) información y consentimiento son dos derechos íntimamente relacionados, pues sólo si se dispone de la información adecuada se podrá prestar libremente el consentimiento.
La información se configura en el art. 4.2 Ley 41/2002 como un elemento esencial, entendida como proceso gradual, continuado en el tiempo, esencialmente verbal, dejando constancia en la historia clínica, adecuada, verdadera, comprensible, sobre la finalidad y naturaleza de cada intervención, riesgos y consecuencias para la toma de decisiones.
En materia de vacunación se plantean dudas sobre cuál es el medio idóneo para proveer de esa información adecuada a los padres o representantes legales, si basta con el prospecto de la vacuna o si es precisa una información detallada sobre la finalidad, naturaleza, riesgos y consecuencias de cada vacuna que se administra.
En lo relativo al prospecto, el mismo se configura como una garantía de información al paciente en el art. 15.3 del Real Decreto Legislativo 1/2015, de 24 de julio, por el que se aprueba el texto refundido de la Ley de garantías y uso racional de los medicamentos y productos sanitarios:
"El prospecto, que se elaborará de acuerdo con el contenido de la ficha técnica, proporcionará a los pacientes información suficiente sobre la denominación del principio activo, identificación del medicamento y su titular e instrucciones para su administración, empleo y conservación, así como sobre los efectos adversos, interacciones, contraindicaciones, en especial los efectos sobre la conducción de vehículos a motor, y otros datos que se determinen reglamentariamente con el fin de promover su más correcto uso y la observancia del tratamiento prescrito, así como las medidas a adoptar en caso de intoxicación. El prospecto deberá ser legible, claro, asegurando su comprensión por el paciente y reduciendo al mínimo los términos de naturaleza técnica”.
De acuerdo con ello, la Sentencia de la Audiencia Nacional, Secc. 4.ª, de 4 de abril de 2012, entiende que el prospecto se considera válido a efectos de información al estar el mismo singularmente dirigido al paciente. Así pues, con carácter general, el prospecto de los medicamentos se considera válido para información, al estar el mismo singularmente dirigido al paciente.
| La información sobre las vacunas es responsabilidad de todo el equipo pediátrico |
Sin embargo, esta previsión legal se aleja de la práctica diaria en materia de vacunación, pues lo cierto es que en la mayoría de los casos no hay un acceso previo de los padres al prospecto para decidir si vacuna o no a sus hijos. La realidad de nuestros centros nos demuestra que son los profesionales sanitarios, pediatras y enfermería, los que informan a los padres sobre los riesgos y beneficios de las vacunas. Con el fin de alcanzar las máximas coberturas vacunales, los equipos pediátricos deben colaborar en garantizar una información adecuada, con especial atención a los padres que puedan tener recelos a las vacunas.
El equipo pediátrico debe suministrar a los padres información completa y entendible (verbal/escrita –opcional-) sobre las vacunas que pueden recibir sus hijos, incluyendo a todas las vacunas autorizadas e indicadas, estén o no financiadas por el SNS.
| Hay que informar de todas las vacunas disponibles, estén o no financiadas |
El equipo pediátrico debe anotar en la historia clínica que se informa a los padres de todas las vacunas recomendadas para la prevención de enfermedades, estén o no financiadas; si no consta en la historia clínica anotación sobre información suministrada a los padres en relación a una vacuna no financiada y hay enfermedad prevenible, pueden ser útiles las hojas informativas que están disponibles en muchos Centros de Salud o consultas pediátricas. Es preciso alertar que estas hojas son muy útiles a los efectos meramente informativos, pero en ningún caso son válidas como prescripción de las vacunas a efectos de su posterior dispensación en oficina de farmacia, ni con ellas se debe entender cumplido el derecho a la información.
El deber de informar sobre todas las vacunas, estén o no financiadas, resulta de la Ley 41/2002:
- Artículo 2. Principios básicos: …“3) El paciente o usuario tiene derecho a decidir libremente, después de recibir la información adecuada, entre las opciones clínicas disponibles” y 6) “Todo profesional que interviene en la actividad asistencial está obligado no sólo a la correcta prestación de sus técnicas, sino al cumplimiento de los deberes de información y de documentación clínica, y al respeto de las decisiones adoptadas libre y voluntariamente por el paciente”
- Artículo 4. Derecho a la información asistencial: “1) Los pacientes tienen derecho a conocer, con motivo de cualquier actuación en el ámbito de su salud, TODA la información disponible sobre la misma, salvando los supuestos exceptuados por la Ley.” … “2) La información clínica forma parte de todas las actuaciones asistenciales, será verdadera, se comunicará al paciente de forma comprensible y adecuada a sus necesidades y le ayudará a tomar decisiones de acuerdo con su propia y libre voluntad. 3) El médico responsable del paciente le garantiza el cumplimiento de su derecho a la información. Los profesionales que le atiendan durante el proceso asistencial o le apliquen una técnica o un procedimiento concreto también serán responsables de informarle.”
De los preceptos citados resulta que la obligación del profesional sanitario de informar integra su lex artis, en el mismo plano que los deberes de documentación y los relativos a la correcta prestación de sus técnicas, y que dicho deber se extiende a todas las opciones clínicas disponibles, estén o no incluidas en el catálogo de prestaciones del SNS.
3.2. ¿Debe el equipo pediátrico exigir que los padres o representantes legales de un menor firmen un documento de consentimiento informado para la vacunación?
| Con carácter general, no es preciso un consentimiento informado por escrito para la vacunación pediátrica |
En lo referente al consentimiento informado por escrito, no forma parte de la práctica habitual su exigencia en relación con las vacunas, considerando que los padres o representantes legales están prestando dicho consentimiento de forma tácita por el mero hecho de acudir a un centro médico a solicitar una determinada vacuna, o que basta con el mero consentimiento verbal de los padres o representantes legales.
El Consentimiento informado se regula en el art.8.2 de la Ley 41/2002:
“El consentimiento será verbal por regla general. Sin embargo, se prestará por escrito en los casos siguientes: intervención quirúrgica, procedimientos diagnósticos y terapéuticos invasores y, en general, aplicación de procedimientos que suponen riesgos o inconvenientes de notoria y previsible repercusión negativa sobre la salud del paciente”.
Se configura así el consentimiento como la principal manifestación de la autonomía voluntad en la relación médico-paciente, es esencialmente verbal, sólo debe constar por escrito en casos excepcionales tasados por la Ley 41/2002, si bien es cierto que se utilizan al efecto conceptos jurídicos indeterminados. Así pues, la exigencia del consentimiento por escrito vendrá determinada por el hecho de que la vacunación se considere un procedimiento invasor que suponga riesgos o inconvenientes de notoria y previsible repercusión negativa sobre la salud.
Tal y como establece el Tribunal Constitucional (Sentencia 37/2011, de 28 de marzo), la ausencia del consentimiento informado puede suponer una vulneración del derecho fundamental a la integridad física consagrada en el artículo 15.1 de la Constitución española si bien aclara que la mera falta del consentimiento no supone violación del derecho fundamental a la integridad física, siendo preciso atender a las circunstancias del caso, pues no se trata de un derecho absoluto e ilimitado, pudiendo ceder ante intereses constitucionalmente relevantes. La regulación del consentimiento supone una doble garantía: para el paciente, que le permite hacer efectivo el derecho fundamental a la integridad física respecto a las actuaciones médicas que se le efectúen; y para el médico, una garantía de la legitimidad del acto médico.
| En vacunas financiadas y campañas vacunales basta con informar de las consecuencias leves y medidas paliativas |
| En vacunas no financiadas hay que informar de los riesgos graves e infrecuentes |
El Tribunal Supremo ha sentado una doctrina casuística al respecto, flexibilizando el uso del consentimiento informado en relación con las vacunas:
- Sentencia del Tribunal Supremo, de 9 de octubre de 2012, en relación a un cuadro de Guillain-Barré tras la inoculación a un varón sano de 37 años de edad de la vacuna de la gripe correspondiente a la campaña 2002-3, afirma que: “En cuanto al primero, es decir, el referido al consentimiento informado al que también se refiere el segundo, ya que en supuestos como el presente, vacunación en todo caso voluntaria si bien aconsejada y promovida por la Administración por los beneficios sociales que de la misma derivan, es bastante con que en el acto de la inoculación del virus se advierta verbalmente a la persona que lo recibe de aquellas consecuencias leves que pueden presentarse y que desaparecerán en breve tiempo y se indique los medios para paliar sus efectos".
- Sentencia del Tribunal Supremo, de 12 de septiembre de 2012, es mucho más restrictiva sobre los riesgos que se deben informar, por entender que: "y, en fin, porque la administración de la vacuna contra la varicela no integra un acto de medicina satisfactiva sino curativa en la que el consentimiento informado no alcanza a aquellos riesgos que no tienen un carácter típico, por no producirse con frecuencia ni ser específicos del tratamiento aplicado, siempre que tengan carácter excepcional, como es aquí el caso, en que la prueba practicada resulta que la cerebelitis posvacunal es rarísima". Esta tesis es más favorable a fomentar el uso de las vacunas, pues una información detallada sobre los riesgos de la vacunación podría provocar un descenso significativo de las tasas de cobertura vacunal, con el riesgo de la inmunización, tanto individual como de grupo.
Ello no obstante, hay situaciones en las que se condena por no haber informado sobre riesgos excepcionales en relación con las vacunas, tal y como veremos en el siguiente apartado.
3.3. ¿La mera visita de los padres o representantes legales al centro de vacunación puede entenderse como que se presta el consentimiento?
| Hay que dejar constancia en la historia clínica de la información suministrada a los padres |
La cuestión hace referencia a la validez del consentimiento tácito que supone la voluntariedad de los padres que llevan al menor al centro de vacunación y que ha sido una justificación muy extendida para legitimar la vacunación.
Esta era la argumentación del SACYL en la Sentencia del Tribunal Superior de Justicia de Castilla y León de 2 de enero de 2012:
“El simple hecho de que los demandantes acudieran al centro de salud para la administración a su hijo de la vacuna triple vírica supone un consentimiento para la misma”.
Sin embargo, dicha argumentación no fue tenida en cuenta:
“Esta Sala no alberga duda de que si bien los padres consintieron la inoculación de la vacuna de la triple viral - imposible de realizar sin su personal y directa colaboración dada la edad del niño-, sin embargo, no fueron informados ni advertidos del que, aunque muy excepcional, posible riesgo de encefalitis secuente a su administración: no consta ningún consentimiento informado por escrito en tal sentido, ni obra referencia alguna en la historia clínica…”
Condenando al SACYL por no dar consentimiento informado de la vacuna triple vírica, causante de encefalitis y tetraparesia espástica, que provocó un 92 % de minusvalía a un menor de 15 meses de edad. Lo que se indemniza es “el daño moral derivado de haber privado al paciente de la información necesaria sobre los posibles riesgos y complicaciones, a fin de que adoptase la decisión que reputaba más conveniente”. La Sala concluye afirmando que “Sin perjuicio de reconocer que probablemente no exista en el campo de la prevención ninguna medida con mejor relación beneficio/coste y beneficio/riesgos que la de las vacunaciones, sí hubo violación del derecho de los recurrentes a poder optar por rechazar sin más la vacunación de su hijo tras la información que la Administración sanitaria pudo y debió suministrarles”.
3.4. ¿Es válida la autorización verbal de padres o representantes legales para la vacunación, o se precisa consentimiento informado por escrito?
| El representante siempre debe consentir en interés del representado |
Tal y como se expuso anteriormente, si bien el consentimiento informado es esencialmente verbal, el mismo debe prestarse por escrito en cirugías, procedimientos diagnósticos y terapéuticos invasivos y en, general en procedimientos que supongan riesgos o inconvenientes de notoria y previsible repercusión negativa para la salud.
Sobre esta cuestión se pronuncia el documento “Criterios de Evaluación para Fundamentar Modificaciones en el Programa de Vacunación en España”: también en la vacunación es necesario el consentimiento informado, habiendo consenso de que sea verbal, excepto en determinadas circunstancias en que se realice por escrito, como por ejemplo ante la administración de vacunaciones en el ámbito escolar donde los padres o tutores no están presentes. En este caso, será necesario contar con la autorización de los padres o tutores para poder administrar cualquier vacuna a los menores de edad.
| Los jueces están imponiendo vacunación obligatoria cuando los representantes se niegan a la vacunación de sus representados |
Con carácter general, esta recomendación de autorización verbal es aplicable a la situación de vacunación frente a la COVID-19. En la particularidad de la vacunación de personas que tengan limitada la capacidad para tomar decisiones es conveniente la información y autorización por escrito por parte del representante legal o personas vinculadas a él o ella por razones familiares o de hecho. En los casos de personas con discapacidad cognitiva o psicosocial, pero con un grado de discapacidad que no les impide tomar una decisión, se informará mediante los formatos adecuados y contando con los apoyos necesarios para que la persona pueda tomar una decisión libre, en condiciones análogas a las demás (lo que además es exigible de manera reforzada desde las aprobación de la Ley 8/2021, de 2 de junio, por la que se reforma la legislación civil y procesal para el apoyo a las personas con discapacidad en el ejercicio de su capacidad jurídica, donde se fomenta el ejercicio de la propia autonomía y se propicia un sistema basado en el respeto a la voluntad y preferencias de las personas con discapacidad muy exigente).
En el anexo 1 se propone un texto para elaborar una hoja informativa y un modelo de consentimiento informado por representación legal63.
En la situación de pandemia por la COVID-19 fueron frecuentes los conflictos derivados de la negativa del representante legal del discapacitado (normalmente, ingresado en residencia de ancianos) a que su representado fuera vacunado. Esta cuestión se analiza en el apartado correspondiente al consentimiento prestado por el representante legal (apartado 3.6). No menos relevantes han sido los casos en los que los tribunales han tenido que resolver sobre la inoculación ante las discrepancias entre los padres de menores. Estas cuestiones han llegado al Tribunal Constitucional que, como se analizará seguidamente, ha sentado una doctrina que ha avalado la autorización judicial de la administración de la vacuna para personas que no son capaces de decidir por sí mismas, y en particular de los menores (la STC 38/2023, de 20 de abril, inaugura una saga de sentencias que consolidan esta doctrina).
Pese a la seguridad de las vacunas, es cierto que, ocasionalmente, se producen eventos adversos de extrema gravedad y que se trata de un procedimiento -mínimamente- invasivo, por lo que pese a alguna jurisprudencia más exigente, el TC ha dado por válido en la reciente jurisprudencia el consentimiento verbal y entendido como información suficiente la de los riesgos o efectos adversos más frecuentes (STC 148/23, de 6-11). La jurisprudencia menor (por todas, STSJCL 114/2024, de 8 de febrero) sigue también esta regla general.
Como quiera que la práctica —no se informa de los riesgos más graves de las vacunas y no se exige el consentimiento escrito— está muy alejada de las exigencias jurídicas —muchos Tribunales empiezan a hacer una aplicación excesivamente rigurosa de la obligación de informar, incluso en casos en los que consta un consentimiento específico— y que las reacciones adversas a las vacunas pueden ser excepcionalmente graves, convendría tener en cuenta que el consentimiento es un medio de prueba de la realidad de la información, por lo que el riesgo legal podría reducirse de forma considerable si se mejoran los instrumentos de información y se deja constancia de ello en la historia clínica. En último término, en relación con la cuestión planteada, téngase en cuenta lo expuesto en los apartados 3.1 y 3.2, a los que nos remitimos para evitar reiteraciones innecesarias.
Por tanto, siguiendo la doctrina jurisprudencial, aun no siendo imprescindible disponer de un consentimiento informado explícito para administrar las vacunas incluidas en los calendarios oficiales de vacunación, debe tenerse en cuenta que sigue habiendo resoluciones judiciales muy exigentes en materia de información y consentimiento. Por ello resulta recomendable, como mínimo, anotar en la historia clínica del paciente que el acto de la vacunación ha sido realizado de acuerdo con los padres (o con consentimiento verbal informado de los padres o tutores) y que los mismos han sido informados de las consecuencias leves que pueden presentarse, de los medios para paliar sus efectos, así como de la duración prevista de las mismas.
__________
3.5. ¿Hasta qué edad es preciso que los padres o representantes legales autoricen la vacunación de los hijos o representados? Catálogo de situaciones
Para mejor comprensión de esta cuestión, que se vio afectada por importantes cambios legislativos en el año 2015, se podrían distinguir tres etapas en el desarrollo y en las capacidades del menor: de 0 a 12 años, de 12 a 16 dependiendo de su madurez y de 16 a 18 años, donde se alcanza la mayoría de edad en el ámbito sanitario.
El régimen jurídico del consentimiento en materia sanitaria parte fundamentalmente un criterio objetivo, de manera que el factor que determina que se atribuya o no capacidad de obrar al menor es la edad. Los menores de 12 o más años tienen el “derecho a ser escuchados” a la hora de adoptar una decisión médica que los afecte, mientras que los de 16 o más años son ya, en principio, titulares del derecho a aceptar o rechazar el tratamiento médico.
Sin embargo, a partir de la reforma de 2015 puede admitirse, aunque de forma algo confusa, que la Ley incorpora ya un criterio mixto (objetivo y subjetivo) basado tanto en una edad de referencia como en la madurez suficiente real del menor. Este régimen general se matiza con una serie de excepciones en las que se seguirá el criterio general de mayoría de edad (18 años) y que atienden a la naturaleza y/o gravedad del acto médico. Y como aún quedan zonas grises, surge la doctrina de la escala móvil de capacidad, que incluya la valoración de la edad y de la gravedad de las consecuencias de la decisión y el impacto de éstas a corto, medio y largo plazo.
Como correlato del criterio del “interés superior del menor”, la capacidad de los menores debe entenderse modulada cuando se trate de intervenciones “de grave riesgo” (art.9.3, modificado en 2015). Ello implica, para una autorización de tratamiento, que se haya pasado de la mera “información a los padres/representantes”, cuya opinión será tenida en cuenta, a “la decisión por sus representantes” en salvaguarda de la vida o salud del menor. Y respecto al rechazo al tratamiento (para menor o representante), el art.9.6 modificado establece una regla general: “la decisión debe adoptarse siempre al mayor beneficio para la vida o salud”. Las decisiones contrarias se deben poner en conocimiento de la autoridad judicial (directamente o a través del Ministerio Fiscal), que adoptará la resolución correspondiente. Con una excepción: “Salvo que, por razones de urgencia, no fuera posible recabar la autorización judicial, en cuyo caso los profesionales sanitarios adoptarán las medidas necesarias, amparados por las causas de justificación de cumplimiento de un deber y de estado de necesidad”.
Para ayudar a la mejor comprensión de la materia, analizaremos las situaciones que pueden plantearse en las diferentes etapas según que el menor tenga más de 16 años o menos83.
__________
83 En esta sistematización se ha seguido a GONZÁLEZ CARRASCO C. y MORENO ALEMÁN J. “Vacunación contra la Covid-19 en menores. La capacidad decisoria en distintos escenarios”, CESCO, Noticias, diciembre 2021.
3.5.1. ¿Los padres pueden negarse a vacunar a sus hijos?
Como en cualquier supuesto de decisión vacunal, es necesario diferenciar entre una diversidad de conceptos que van más allá del binomio obligatoriedad-voluntariedad. No es correcto hablar de obligatoriedad como vacunación forzosa, como nos ha demostrado la casuística, sobre todo en época de la covid. Las vacunas pueden ser meramente voluntarias no financiadas, recomendadas (financiadas o no), pero también condicionantes para entradas en lugares o realización de actividades. Si su carácter es impuesto, pueden ser obligatorias – que, como obligación personalísima, no permite compulsión física, pero sí sanción administrativa- y finalmente, coactivas o forzosas en sentido estricto. Estas últimas solo podrían imponerse con autorización judicial puntual regulada en la LJCA (arts. 8 y ss.), en supuestos muy excepcionales. La Ley 22/1980, de 24 de abril, así como la Ley Orgánica 3/1986, de 14 de abril, de Medidas Especiales en Materia de Salud Pública, avalan la obligatoriedad en todas sus modalidades descritas, siempre que se cumpla con el principio de proporcionalidad en relación con el riesgo para la salud pública.
Comenzando por el supuesto más extremo, el de unos padres negacionistas frente a las vacunas, la situación varía en función de la franja de edad del menor.
En el caso de que los progenitores sean contrarios a la vacuna y nieguen la prestación de dicho consentimiento, hemos de preguntarnos de qué forma podrá ser autorizado dicho acto médico.
Tras la modificación operada en la Ley 41/2002 por la Ley 26/2015, de modificación del sistema de protección de la infancia y la adolescencia, el apartado 6 del art. 9 exige que la decisión del representante legal del menor o de la persona con discapacidad, en cualquiera de los supuestos descritos en los apartados 3 a 5 del mismo artículo, sea adoptada atendiendo siempre al mayor beneficio para la vida o la salud del paciente. Aquellas decisiones que sean contrarias a dichos intereses “deberán ponerse en conocimiento de la autoridad judicial, directamente o a través del Ministerio Fiscal, para que adopte la resolución correspondiente, salvo que, por razones de urgencia, no fuera posible recabar la autorización judicial, en cuyo caso los profesionales sanitarios adoptarán las medidas necesarias en salvaguarda de la vida o salud del paciente, amparados por las causas de justificación de cumplimiento de un deber y de estado de necesidad”. Parece evidente que en materia de vacunación no concurren las razones de urgencia que permiten a los profesionales sanitarios actuar sin el consentimiento de los representantes legales del menor, por lo que la autorización judicial sustitutoria será necesaria.
La vía procesal para obtener una autorización judicial sustitutoria de la negada por los titulares de la patria potestad será la del expediente de jurisdicción voluntaria previsto en el art. 87.1 Ley de Jurisdicción Voluntaria (ejercicio inadecuado de la patria potestad), instado de oficio, por el Ministerio Fiscal, cualquier pariente o el propio menor (o, en caso de que se trate de una persona con discapacidad, el propio profesional sanitario responsable del protocolo de vacunación o cualquier interesado) para que el juez adopte las medidas del apartado 6º del art 158 CC. En dicho expediente, el Juez puede “acordar la suspensión cautelar en el ejercicio de la patria potestad y/o en el ejercicio de la guarda y custodia, la suspensión cautelar del régimen de visitas y comunicaciones establecidos en resolución judicial o convenio judicialmente aprobado y, en general, las demás disposiciones que considere oportunas, a fin de apartar al menor de un peligro o de evitarle perjuicios en su entorno familiar o frente a terceras personas”. Veremos que, en caso de conflicto sobre la decisión de vacunar entre los progenitores, esta ha sido la vía procesal escogida en la práctica totalidad de los supuestos, llevando a la autorización judicial para confirmar la autorización a uno de los padres.
Y es que entendemos que la resolución a adoptar en esta vía no puede extenderse a la suspensión de la patria potestad o guarda y custodia que prevé esta norma, pues esta medida sólo procede en los casos de riesgo para el menor. Y ello porque, si bien el apartado 2 del artículo 17 de la LO 1/1996 (modificados por LO 8/2021, de 4 de junio, de protección integral a la infancia y la adolescencia frente a la violencia), consideran indicador de la situación de riesgo del menor “b) La negligencia en el cuidado de las personas menores de edad y la falta de seguimiento médico por parte de los progenitores, o por las personas que ejerzan la tutela, guarda o acogimiento”. No parece que la negativa a consentir la vacunación de un menor de edad sano comprendido entre los cinco y los 16 años de edad sea equiparable a la negligencia y falta de seguimiento médico, e incluso aunque la vacuna estuviera en calendario vacunal, que es meramente recomendado, sería desproporcionado aplicar esta medida.
Sin embargo, como cabe la posibilidad de que, por razones de salud pública, se haya avalado una vacunación condicionante en virtud de los arts. 8 y ss. de la LJCA, la declaración de riesgo del menor podrá proceder, desde el momento en que la ausencia de la vacunación le impida acceder a actividades que conforman su interés superior, como la educación, el ocio o incluso la socialización con sus iguales.
3.5.2. Edad, madurez, consentimiento y representación en materia vacunal. ¿Todos los menores de edad están en la misma situación? (menores maduros y mayores de dieciséis años cumplidos)
| Hasta los 12 años: consienten los padres o tutores |
| A partir de los 12 años: los menores pueden consentir por sí mismos, teniendo en cuenta su grado de madurez (menores maduros), pero los padres deben codecidir, en ejercicio de la patria potestad |
| Con 16 años: se alcanza la mayoría de edad sanitaria y pueden consentir por sí mismo |
- Menores, a partir de 12 años de edad, en función de su grado de madurez
Según establece el art. 9.3 c) de la Ley 41/2002 (en su redacción por la Ley 26/2015, de 28 de julio, de modificación del sistema de protección a la infancia y adolescencia: “Se otorgará el consentimiento por representación c) Cuando el paciente menor de edad no sea capaz intelectual ni emocionalmente de comprender el alcance de la intervención. En este caso, el consentimiento lo dará el representante legal del menor, después de haber escuchado su opinión, conforme a lo dispuesto en el artículo 9 de la Ley Orgánica 1/1996, de 15 de enero, de Protección Jurídica del Menor".
Para comprender el alcance del derecho que tiene el menor a ser oído y escuchado, la Ley 41/2002 en su redacción actual remite la cuestión al artículo 9 de la Ley Orgánica 1/1996 de 15 de enero, de Protección Jurídica del menor, de modificación parcial del Código Civil y de la Ley de Enjuiciamiento Civil (en su redacción por la Ley Orgánica 8/2015, de 22 de julio, de modificación sistema de protección a la infancia y adolescencia), establece que en su Artículo 9 el derecho a ser oído y escuchado: el menor tiene derecho a ser oído y escuchado sin discriminación alguna por edad, discapacidad o cualquier otra circunstancia, tanto en el ámbito familiar como en cualquier procedimiento administrativo, judicial o de mediación en que esté afectado y que conduzca a una decisión que incida en su esfera personal, familiar o social, teniéndose debidamente en cuenta sus opiniones, en función de su edad y madurez. Para ello, el menor deberá recibir la información que le permita el ejercicio de este derecho en un lenguaje comprensible, en formatos accesibles y adaptados a sus circunstancias.
En los procedimientos judiciales o administrativos, las comparecencias o audiencias del menor tendrán carácter preferente, y se realizarán de forma adecuada a su situación y desarrollo evolutivo, con la asistencia, si fuera necesario, de profesionales cualificados o expertos, cuidando preservar su intimidad y utilizando un lenguaje que sea comprensible para él, en formatos accesibles y adaptados a sus circunstancias informándole tanto de lo que se le pregunta como de las consecuencias de su opinión, con pleno respeto a todas las garantías del procedimiento.
Se garantizará que el menor, cuando tenga suficiente madurez, pueda ejercitar este derecho por sí mismo o a través de la persona que designe para que le represente. La madurez habrá de valorarse por personal especializado, teniendo en cuenta tanto el desarrollo evolutivo del menor como su capacidad para comprender y evaluar el asunto concreto a tratar en cada caso. Se considera, en todo caso, que tiene suficiente madurez cuando tenga doce años cumplidos.
Para garantizar que el menor pueda ejercitar este derecho por sí mismo será asistido, en su caso, por intérpretes. El menor podrá expresar su opinión verbalmente o a través de formas no verbales de comunicación.
No obstante, cuando ello no sea posible o no convenga al interés del menor se podrá conocer la opinión del menor por medio de sus representantes legales, siempre que no tengan intereses contrapuestos a los suyos, o a través de otras personas que, por su profesión o relación de especial confianza con él, puedan transmitirla objetivamente.
Además, siempre que en vía administrativa o judicial se deniegue la comparecencia o audiencia de los menores directamente o por medio de persona que le represente, la resolución será motivada en el interés superior del menor y comunicada al Ministerio Fiscal, al menor y, en su caso, a su representante, indicando explícitamente los recursos existentes contra tal decisión. En las resoluciones sobre el fondo habrá de hacerse constar, en su caso, el resultado de la audiencia al menor, así como su valoración.
Un análisis sistemático de estas normas conducen a que, si el menor tiene la madurez suficiente para comprender el alcance de la intervención a criterio del facultativo, aunque no tenga cumplidos los dieciséis años, no sería necesario acudir al consentimiento “por representación”. Esta interpretación sería posible teniendo en cuenta que el dato decisivo es la capacidad real del menor –«sus condiciones de madurez», en la terminología del art. 162 del Código Civil– para comprender la trascendencia de la intervención; y que, todo menor mayor de doce años no afectado por una discapacidad intelectual o un trastorno cognitivo puede tener la madurez suficiente para comprender el alcance de la vacunación al efecto de ser escuchado y que su opinión se tenga en cuenta (art. 9.2 LO 1/1996, modificado por LO 8/2015). No es solo la propia literalidad del precepto, y la remisión a la LO 1/1996 la que conduce a esta interpretación, sino también la interpretación que del mismo realiza la Circular de la Fiscalía General del Estado 1/20124, que fue la precursora de la reforma operada por la Ley 26/2015 en el art. 9 de la Ley 41/200284.
La duda que se plantea entonces es la de si en tal caso -menores de dieciséis que a juicio del profesional responsable gozan de capacidad y madurez suficiente para comprender el alcance de la intervención y que desean ser vacunados- se puede prescindir del consentimiento de los padres y contar sólo con el del propio menor.
La doctrina más autorizada en materia de capacidad ya entendió en la fecha de la entrada en vigor de la ley 41/2002 que “la exigencia del cumplimiento de los deberes de guarda y protección impide una contraposición radical entre, de una parte, la representación de los padres o tutor y, de otra, la actuación del menor por sí mismo”. En efecto, eliminar la necesidad de consentimiento parental no parece razonable, y resulta preferible conciliar el criterio “mixto” del art. 9.3.c) con lo previsto en el ámbito del ejercicio del deber de guarda de los padres (y tutores, «representante legal»: arts. 154 y 215 - 216 - 267 y 269 del Código Civil). Es decir: si a juicio del profesional responsable, el menor (de más de doce años, por remisión a la LO 1/1996) está plenamente capacitado intelectual y emocionalmente para comprender el alcance de la intervención a pesar de no tener dieciséis años cumplidos, se excluye la representación en sentido técnico (es decir, no cabe que otro tome la decisión por el menor, y debe recabar su consentimiento); pero no la intervención de los obligados a su guarda y custodia, que deben prestar también su consentimiento, junto al del menor, (esto es, codecidir) como manifestación del deber de velar por él..
| A partir de los 16 años consienten los menores maduros, salvo casos de grave riesgo |
- Menores, de 16 a 18 años de edad
Según establece el art. 9.4 de la Ley 41/2002 (en su redacción por la Ley 26/2015, de 28 de julio): “Cuando se trate de menores emancipados o mayores de 16 años que no se encuentren en los supuestos b) y c) del apartado anterior, no cabe prestar el consentimiento por representación”.
No obstante lo dispuesto en el párrafo anterior, cuando se trate de una actuación de grave riesgo para la vida o salud del menor, según el criterio del facultativo, el consentimiento lo prestará el representante legal del menor, una vez oída y tenida en cuenta la opinión del mismo. Es más, cabría plantear que la referencia al apartado c) del art. 9.3 transcrito es definitiva para entender que, en la actualidad, siguiendo el criterio mixto impulsado por la Circular, se requerirá el consentimiento de los representantes legales del menor mayor de dieciséis años o del defensor judicial del emancipado cuando, a juicio del facultativo, el paciente menor de edad (aun mayor de dieciséis años o emancipado) “no sea capaz, intelectual ni emocionalmente, de comprender el alcance de la concreta intervención”.
En definitiva, por un lado, con carácter general, mantiene su capacidad para prestar el consentimiento a partir de los 16 años de edad, alcanzando así la denominada mayoría de edad sanitaria.
En cambio, en los casos de grave riesgo para la vida o salud del menor, a criterio del facultativo, el menor pierde la capacidad de prestar el consentimiento a favor de su representante legal, después de haber oído y tenido en cuenta la capacidad del menor (a diferencia de lo que ocurría antes de la reforma de 2015, donde el menor a partir de los 16 años de edad conservaba la capacidad de consentir incluso en los casos de grave riesgo, siendo los padres informados y tomando en consideración su opinión al respecto).
A pesar de que la doctrina no se ha hecho eco de que la redacción actual haya supuesto cambio de criterio alguno, la referencia al apartado c) del art. 9.3 transcrito es definitiva para entender que, en la actualidad, siguiendo el criterio mixto impulsado por la Circular, se requerirá el consentimiento de los representantes legales del menor mayor de dieciséis años o del defensor judicial del emancipado cuando, a juicio del facultativo, el paciente menor de edad (aun mayor de dieciséis años o emancipado) “no sea capaz, intelectual ni emocionalmente, de comprender el alcance de la concreta intervención”. Y si éstos la niegan, será aplicable la misma solución anteriormente expuesta.
En la medida en que la vacunación es de carácter voluntario y su aplicación no entraría en el supuesto de grave riesgo para la vida o la salud del menor, entendemos que procede aplicar, en lo que a las vacunas se refiere, el criterio de la mayoría de edad sanitaria a partir de los 16 años, pudiendo el menor consentir o rechazar la vacunación.
El resumen del consentimiento informado en función de la edad del menor se puede consultar en la tabla 46.2.
Tabla 46.2. El consentimiento informado en función de la edad del menor.
| Edad del niño o adolescente | Consentimiento | Audiencia | |
| De 0 a 12 años | Representante legal | No procede legalmente audiencia al menor, salvo que concurran condiciones de madurez a criterio de personal especializado | |
| De 12 a 16 años | El menor, atendidas sus condiciones de madurez, a criterio del facultativo (menor maduro) Si bien los padres deben codecidir, en ejercicio de la patria potestad |
Después de haber oído y escuchado al menor y según la valoración de la escala móvil de capacidad en cuanto a su madurez | |
| De 16 a 18 años | Con carácter general: el menor (alcanza la mayoría de edad sanitaria) | — | |
| En caso de grave riesgo para la vida o la salud del menor: el representante legal | En caso de grave riesgo, a criterio del facultativo, el menor será oído y su opinión será tenida en cuenta |
__________
84 La Fiscalía considera que el legislador no opta en la redacción original de la Ley de autonomía del paciente por un criterio únicamente objetivo, basado en la mera edad, sino que de su tenor se deduce la operatividad también de una regla subjetiva basada en la madurez real del menor para entender y aceptar o rechazar el tratamiento. No obstante, la propia Fiscalía admite en la justificación de la propia Circular que resulta tan correcto una interpretación que postule como criterio único el objetivo, como la que postule un criterio mixto objetivo y subjetivo
3.5.3. El ejercicio de la representación en menores. El “interés superior del menor” como canon de constitucionalidad
En todo caso, cuando el consentimiento haya de otorgarlo el representante legal o las personas vinculadas por razones familiares o de hecho en cualquiera de los supuestos descritos en el art.9, apartados 3 a 5 de la Ley 41/2002 descritos, la decisión deberá adoptarse atendiendo siempre al mayor beneficio para la vida o salud del paciente. Aquellas decisiones que sean contrarias a dichos intereses deberán ponerse en conocimiento de la autoridad judicial, directamente o a través del Ministerio Fiscal, para que adopte la resolución correspondiente, salvo que, por razones de urgencia, no fuera posible recabar la autorización judicial, en cuyo caso los profesionales sanitarios adoptarán las medidas necesarias en salvaguarda de la vida o salud del paciente, amparados por las causas de justificación de cumplimiento de un deber y de estado de necesidad.
Además, la prestación del consentimiento por representación será adecuada a las circunstancias y proporcionada a las necesidades que haya que atender, siempre en favor del paciente y con respeto a su dignidad personal. El paciente participará en la medida de lo posible en la toma de decisiones a lo largo del proceso sanitario.
Hay que tener en cuenta que los padres o representantes legales siempre deben actuar en interés de sus representados, y que, en caso de conflicto entre los padres, debe primar el interés superior del menor. Si no se llega a un acuerdo, debe darse cuenta del mismo a la autoridad judicial (directamente, o a través del Ministerio Fiscal), quien decidirá siempre en beneficio del menor, salvo que por razones de urgencia los facultativos se vieran obligados a actuar sin autorización judicial en cumplimiento del deber y debido al estado de necesidad.
El criterio del interés superior del menor, que es un principio general del derecho, de carácter transversal —en la medida en que se aplica a cualquier regulación normativa que pueda afectar el interés del menor—, ha pasado de una mera formulación general en nuestro Derecho a tener una desarrollo normativo destacado en el artículo 2 de la Ley Orgánica 1/1996, de 15 de enero, de Protección Jurídica del Menor (en su redacción por la Ley Orgánica 8/2015, de 22 de julio, de modificación del sistema de protección a la infancia y a la adolescencia), desplegando sus efectos en tres vertientes: 1) el derecho sustantivo que tiene el menor a que cuando se adopte una medida que le pueda afectar, sus mejores intereses hayan sido valorados y, en su caso, ponderados con otros intereses con los que pudieran concurrir; 2) un criterio interpretativo, de modo que cualquier norma jurídica se debe interpretar de la forma que mejor proteja los intereses del menor; y 3) una norma de procedimiento, ajustando todos los trámites y procedimientos a la mayor protección de los intereses del menor; todo ello con la finalidad de asegurar el respeto completo y efectivo de todos los derechos del menor, así como su desarrollo integral.
Por supuesto, este criterio será determinante también en materia vacunal. De hecho, este ha sido uno de los ejes que ha conducido la nueva doctrina constitucional sobre el consentimiento por representación como canon de constitucionalidad aplicable a la vacunación de los menores de edad.
El leading case es la STC 148/2023, de 6 de noviembre, que resuelve el recurso de amparo contra el auto de 21 de enero de 2022, dictado por el Juzgado de Primera Instancia núm. 5 de Zaragoza en expediente de jurisdicción voluntaria para la resolución de desacuerdo en el ejercicio de la patria potestad, que estima la petición de padre y le autoriza para que, sin intervención de la madre (contraria a la vacunación), realice las gestiones necesarias para la efectiva vacunación de la hija común de ambos, de once años, contra la Covid-19. También se impugna el auto de 27 de abril de 2022, dictado por la Sección Segunda de la Audiencia Provincial de Zaragoza, desestimatorio del recurso de apelación interpuesto contra el auto dictado por el juzgado de primera instancia.
El TC parte de esta premisa: “la capacidad general de autodeterminación de las personas que todavía no hayan alcanzado la mayoría de edad en relación con las actuaciones médicas que les afectan encuentra su límite en la protección de su interés superior, que se impone como obligación a los progenitores, en cuanto titulares de la patria potestad o autoridad familiar, y a todos los poderes públicos, incluida la autoridad judicial. A todos ellos corresponde garantizar que la decisión final relativa a la actuación médica en cuestión no trae consigo una quiebra relevante, persistente y/o irreparable de dicho interés superior”.
Desde este punto de partida, el TC analiza la “Obligación de los representantes legales de actuar en función del interés superior del menor”.
La sentencia señala que en el momento de prestar el consentimiento por representación a que se refiere el art. 9.3, letra c) de la Ley 41/2002, los representantes legales “no gozan de libertad para decidir lo que consideren conveniente según su propio criterio, sino que vienen directamente vinculados por la obligación de actuar en interés de la persona menor de edad, de acuerdo con su personalidad y con respeto a sus derechos y a su integridad física y mental (art. 154 CC).
Entra así en juego el estatuto de protección de las personas menores de edad que, de acuerdo con una reiterada doctrina de este tribunal, excede del ámbito estrictamente privado para tener una consideración más cercana a las normas de orden público, o ius cogens [SSTC 141/2000, de 29 de mayo, FJ 5; 185/2012, de 17 de octubre, FJ 4, y 106/2022, de 13 de septiembre, FJ 2 B)].
Este marco de protección se encuentra presidido por el art. 39 de nuestra Constitución, que en su apartado 3 dispone que «[l]os padres deben prestar asistencia de todo orden a los hijos habidos dentro o fuera del matrimonio, durante su minoría de edad y en los demás casos en que legalmente proceda»; y en su apartado 4 añade, en consonancia con lo establecido en el art. 10.1 CE, que «los niños gozarán de la protección prevista en los acuerdos internacionales que velan por sus derechos».
Entre estos acuerdos destaca la Convención sobre los derechos del niño, adoptada por la Asamblea General de las Naciones Unidas el 20 de noviembre de 1989 y ratificada por el Estado español el 30 de noviembre de 1990, que ha encontrado desarrollo normativo específico dentro de nuestro ordenamiento jurídico en diversas leyes, entre las que destaca la Ley Orgánica de protección jurídica del menor, reformada por la Ley Orgánica 8/2015, de 22 de julio, de modificación del sistema de protección a la infancia y a la adolescencia, cuyo art. 2.1 dispone que «todo menor tiene derecho a que su interés superior sea valorado y considerado como primordial en todas las acciones y decisiones que le conciernan, tanto en el ámbito público como privado».
Son muy numerosos los pronunciamientos de este tribunal acerca de la necesaria observancia del mandato dirigido a los poderes públicos en el art. 39 CE (SSTC 141/2000, FJ 5, y 178/2020, de 14 de diciembre, FJ 3). Hemos insistido, así, en que el interés superior del menor es la consideración primordial a la que deben atender todas las medidas concernientes a los menores que tomen las instituciones públicas o privadas de bienestar social, los tribunales, las autoridades administrativas o los órganos legislativos; y en que, en caso de que no puedan respetarse todos los intereses legítimos concurrentes, deberá primar el interés superior del menor sobre cualquier otro interés legítimo que pudiera concurrir (STC 64/2019, de 9 de mayo, FJ 4, por todas).
Por otra parte, cuál sea en cada caso el interés superior del menor tampoco puede determinarse de manera libre por los representantes legales y según su propio criterio, sino tomando en consideración los criterios legalmente establecidos en el art. 2 de la Ley Orgánica 1/1996 con carácter general, y en las leyes especiales que regulen de manera específica la materia a que se refiera la decisión; en concreto y en el caso que nos ocupa, los apartados 6 y 7 del artículo 9 de la Ley 41/2002.
De este modo, la decisión de los representantes legales relativa al otorgamiento o no del consentimiento informado por representación deberá atender a «la protección del derecho a la vida, supervivencia y desarrollo del menor y la satisfacción de sus necesidades básicas, tanto materiales, físicas y educativas como emocionales y afectivas» [art. 2.2, letra a) de la Ley Orgánica 1/1996] y buscar el mayor beneficio para la vida o salud del paciente que no ha adquirido la mayoría de edad, teniendo en cuenta las circunstancias concurrentes y las necesidades del menor que han de ser atendidas (art. 9, apartados 6 y 7 de la Ley 41/2002).
Aplicando esta doctrina al caso específico, esto es, el examen de si la decisión judicial de autorizar al padre para realizar las gestiones necesarias para la vacunación de la hija común responde a las exigencias constitucionales orientadas a la consecución de una finalidad constitucionalmente legítima, entiende el TC que: “la decisión de autorizar la vacunación tuvo como fundamento primero y esencial la protección del interés superior de la propia menor en sus dos vertientes fundamentales: protección de la salud física individual frente a una eventual infección por Covid-19; y protección de la salud mental mediante la preservación de sus relaciones interpersonales en el entorno social, familiar y escolar, finalidades ambas plenamente legítimas desde el punto de vista constitucional”.
3.6. Y en caso de conflicto, ¿puede vacunarse un menor de 12 años o más con el solo consentimiento de uno de sus progenitores, a pesar de la oposición del otro?
| Si la vacuna está en el calendario oficial, bastaría con el consentimiento de uno solo de los progenitores (la decisión la toma el custodio), oído el menor, salvo que conste la oposición del otro a la vacunación, en cuyo caso se precisa autorización judicial por la vía del procedimiento de jurisdicción voluntaria |
| En vacunas fuera del calendario oficial, si no hay acuerdo de los padres, la decisión precisa también de la intervención judicial |
3.6.1. Consentimiento por representación y patria potestad
Tal y como se expuso en el apartado anterior, de acuerdo con el artículo 9.3.c) de la Ley 41/2002 “Se otorgará el consentimiento por representación… c) Cuando el paciente menor de edad no sea capaz intelectual ni emocionalmente de comprender el alcance de la intervención. En este caso, el consentimiento lo dará el representante legal del menor, después de haber escuchado su opinión, conforme a lo dispuesto en el artículo 9 de la Ley Orgánica 1/1996, de 15 de enero, de Protección Jurídica del Menor".
Conforme a los artículos 158.6 del CC y 770 de la LEC, el menor tiene derecho a ser oído en condiciones idóneas, sin interferencias de otras personas, con ayuda de especialistas y con la información suficiente. Por ello, tal y como expresa la sentencia de la AP de Barcelona (Sección 12.ª), n.º 83/2015, de 17 de febrero de 2015, el juez deberá valorar la madurez del menor oído, no resolviendo conforme a su voluntad cuando sea contraria a su interés o fruto de la influencia de alguno de sus progenitores.
En el caso, al contar el menor con 12 años de edad, la madurez del menor se presume, como establece el artículo 9.2 de la Ley Orgánica 1/1996 de 15 de enero, de Protección Jurídica del menor, en su párrafo primero: Se garantizará que el menor, cuando tenga suficiente madurez, pueda ejercitar este derecho (a ser oído y escuchado) por sí mismo o a través de la persona que designe para que le represente. La madurez habrá de valorarse por personal especializado, teniendo en cuenta tanto el desarrollo evolutivo del menor como su capacidad para comprender y evaluar el asunto concreto a tratar en cada caso. Se considera, en todo caso, que tiene suficiente madurez cuando tenga doce años cumplidos.
Representación legal de los hijos
En cuanto a la representación legal de los hijos, la ostentan los titulares de la patria potestad (artículo 162 CC), salvo cuando exista conflicto de intereses entre los titulares o entre ellos y el hijo, en cuyo caso el juez procederá de oficio al nombramiento de un defensor judicial que represente al menor. De acuerdo con la Sentencia del Tribunal Supremo (Sala Civil, Sección 1.ª), núm. 339/2012, de 5 de junio:
“Dicho conflicto puede estar presente cuando los intereses y derechos de uno (titular o titulares de la patria potestad) y otro (el hijo) son contrarios u opuestos en un asunto determinado, de modo que el beneficio de uno puede comportar perjuicio para el otro… La situación de conflicto se identifique con supuestos en los que sea razonable entender que la defensa por los padres de sus propios intereses irá en detrimento de los de los hijos”.
Los titulares de la patria potestad son los dos progenitores, salvo que por sentencia se haya privado a uno de ellos de su titularidad.
El ejercicio de la patria potestad lo tiene el progenitor custodio cuando los padres no conviven, de acuerdo con el artículo 156 CC, pero no para todas las decisiones, para la toma de decisiones médicas relevantes el ejercicio lo ostentan los dos titulares, como se expone en la Circular 1/2012 de la Fiscalía General del Estado, sobre el tratamiento sustantivo y procesal de los conflictos ante trasfusiones de sangre y otras intervenciones médicas sobre menores de edad en caso de riesgo grave.
Para poder determinar si en el caso de las vacunas hace falta el consentimiento de los dos progenitores cuando uno sólo es el custodio, hay que atender a si la vacuna está incluida dentro del calendario oficial o es una vacuna no financiada. No hay ninguna resolución judicial que haya versado expresamente sobre esto, pero sí hay algunas resoluciones que determinan que la guardia y custodia “incluye la potestad de tomar decisores habituales y rutinarias tales como revisiones pediátricas ordinarias y vacunas previstas por las autoridades sanitarias” (Sentencias de la Audiencia Provincial de Alicante (Sección 6.ª) núm. 203/2015, de 5 de noviembre; y núm. 85/2016, de 13 de abril). Sin embargo, “ambos deberán intervenir necesariamente en la elección o cambio de centro o modelo educativo (público, concertado o privado), tratamiento médico no banal o tratamiento psicológico, vacunas no previstas en el calendario oficial publicado por las autoridades sanitarias competentes, tratamiento de quimioterapia” (Sentencias de la Audiencia Provincial de Alicante (Sección 6.ª) núm. 185/2014 de 23 de julio; y núm. 246/2014, de 11 de noviembre).
Las situaciones, además, pueden ser variopintas. Señalemos las principales, poniéndolas en relación con la vacunación.
1.- Los progenitores (convivientes) ejercen la patria potestad conjunta sin medidas sobre la guarda y custodia de los hijos
Tal y como indica el art. 156 CC, aplicable a los actos de ejercicio ordinario de la patria potestad, «la patria potestad se ejercerá conjuntamente por ambos progenitores o por uno solo con el consentimiento expreso o tácito del otro. Serán válidos los actos que realice uno de ellos conforme al uso social y a las circunstancias o en situaciones de urgente necesidad”. Tratándose de la vacunación del calendario u otra protocolizada (como lo fue en un primer momento la vacuna Covid-19), puede considerarse un acto sanitario ordinario para el cual: a) basta que el menor acuda acompañado por uno de los progenitores, y b) la información previa al consentimiento queda reducida a los efectos secundarios frecuentes, siendo la información sobre los riesgos infrecuentes sustituida por la información epidemiológica incluida en la información pública del protocolo de vacunación. C) Respecto del servicio sanitario (tercero de buena fe del art, 156 CC), se presumirá que cada uno de los progenitores actúa en el ejercicio ordinario de la patria potestad con el consentimiento del otro.
2.- Los progenitores no conviven juntos, y la guarda y custodia del menor está atribuida a uno solo de ellos
Dentro de este escenario se abren varias posibilidades:
a) Que el progenitor custodio decida que el menor se vacune, sin oposición del menor, pero el progenitor no custodio se manifieste contrario a dicha posibilidad
En este caso, es directamente aplicable, por tratarse de un acto sanitario de carácter ordinario, el primer párrafo del art. 156 CC, que atribuye la decisión al progenitor custodio sin que la oposición del no custodio sea oponible al servicio sanitario, aunque la discrepancia sea detectada antes de la vacunación. La guardia y custodia “incluye la potestad de tomar decisores habituales y rutinarias tales como revisiones pediátricas ordinarias y vacunas previstas por las autoridades sanitarias”, como señalan aquellas sentencias mencionadas. El progenitor no custodio puede acudir a la aplicación del art. 158.6.º CC por la vía del art. 87 LJV (expediente de jurisdicción voluntaria por ejercicio inadecuado de la patria potestad), si considera que, por alguna razón específica concurrente en el menor, la vacuna será un riesgo para su salud o su vida; pero mientras no exista una resolución conocida por el servicio sanitario, no será oponible a éste.
b) Que el progenitor custodio sea contrario a la vacunación del menor, y el no custodio, solicite la vacunación de éste
Partimos de la base de que el menor de dieciséis años debería acudir acompañado a la vacunación por uno de los representantes legales que exprese el consentimiento, expreso o tácito, por representación, y que la carga de averiguar la situación convivencial de los progenitores no puede hacerse recaer sobre los profesionales sanitarios. Por lo tanto, las situaciones de conflicto entre progenitores serán difícilmente detectables en los casos en los que el menor está de acuerdo en la decisión de vacunarse. No obstante, si se da la circunstancia de que la discrepancia es detectada, el progenitor no custodio que pretenda la vacunación del menor puede acudir al expediente de jurisdicción voluntaria de adopción de medidas de protección relativas al ejercicio inadecuado de la patria potestad (art. 87.1 LJV).
Y ello porque la autoridad judicial habrá de garantizar la audiencia de la persona menor de edad, y en dicha audiencia, el menor pondrá de manifiesto su deseo de ser vacunado conforme al protocolo sanitario establecido, volviendo al punto inicial: la medida acordada por el juez consistirá en autorizar la vacunación, con un retraso lamentable y el evidente riesgo de que se cause un perjuicio al interés del menor.
3.- Los progenitores viven separados, y la guarda y custodia del menor está atribuida a ambos de forma compartida
Según el art. 156.3 CC, “en caso de desacuerdo en el ejercicio de la patria potestad, cualquiera de los dos podrá acudir a la autoridad judicial (el trámite más rápido es, de nuevo, el del art. 87 LJV) quien, después de oír a ambos y al hijo si tuviera suficiente madurez y, en todo caso, si fuera mayor de doce años, atribuirá la facultad de decidir a uno de los dos progenitores”. Parece lógico pensar que el Juez decidirá en favor del progenitor que, de acuerdo con la opinión expresada por el menor, opte por la vacunación. Si éste es contrario a ser vacunado, su opinión será tenida en cuenta en función de su grado de madurez (que se le presume a este efecto a los 12 años), pero no prima en estos casos el principio de autonomía, sino el de beneficencia, de modo que el juez decidirá en función del interés superior del menor, que en circunstancias normales será su vacunación.
3.6.2.- La casuística entre los progenitores respecto a la vacunación de sus hijos menores
| La jurisprudencia ha avalado la autorización de la vacunación en contra del criterio de uno de los progenitores, porque la vacunación no puede quedar al mero arbitrio de los padres, debiendo primar en todo caso el interés superior del menor |
Antes de que el TC fijara su doctrina sobre el canon de constitucionalidad del interés superior del menor en materia de representación para la vacunación de menores, ya la jurisprudencia había resaltado la importancia de este criterio en caso de conflicto o discrepancias sobre la vacunación por los progenitores o representantes legales.
Una buena muestra de ella es el Auto 125/2019 de la Audiencia Provincial de Vigo, Sección: 6, de 22/07/201985, que expone que en la toma de decisiones de los padres debe primar el interés superior del menor: “Todo menor tiene derecho a que su interés sea valorado y considerado como primordial en todas las acciones y decisiones que le conciernen, tanto en el ámbito público como privado. No se discute el derecho de los progenitores a defender las creencias que estimen oportunas o el sistema de educación y de vida de sus hijos, pero siempre que no resulte perjudicial para los mismos”.
Entiende la Sala de la Audiencia Provincial que las vacunas son beneficiosas: “Las reticencias manifestadas por la madre no están avaladas por datos científicos ni objetivos (…) ya que no se ha acreditado desde el punto de vista médico que las vacunas causen un perjuicio para la salud. Todo lo contrario, porque la mayoría de los estudios científicos sobre esta materia llevan a concluir que los beneficios de las vacunas son innegables individual y poblacionalmente
Termina afirmando que: “evidentemente, no puede quedar al arbitrio de uno de los progenitores, decidir si desea vacunar y en qué momento”
En análogo sentido se pronunció recientemente el Tribunal Supremo alemán que, en un caso de disputa entre los progenitores sobre la vacunación de la hija, afirma que la ley establece que en caso de disputa en asuntos de "considerable importancia para el menor", el Tribunal de Familia puede conceder la custodia en una decisión concreta en exclusividad a uno de los progenitores si éste así lo ha solicitado. "El poder decisorio debe ser concedido al progenitor cuya propuesta se aproxima más al bienestar del menor", subraya la corte. El Tribunal Supremo considera "mejor capacitado al padre para decidir acerca de la aplicación de las citadas vacunas" a la menor, al no existir, además, circunstancias que apunten a un riesgo para la niña, al tiempo que subraya que el progenitor debe orientarse en las recomendaciones de la Stiko, consideradas por esta corte un "estándar médico".
El supuesto de desacuerdo de los progenitores respecto a la vacunación ha sido importante respecto a la vacuna Covid, generando una relevante y amplia jurisprudencia. En la que ha avalado la decisión favorable a la vacunación, los argumentos principales han sido: la vacuna como el medio más idóneo y efectiva para controlar la pandemia y los efectos del virus; la aprobación y recomendación por las autoridades sanitarias y los avales de la principales sociedades científica (como la AEP); la contribución de la vacunación a la inmunidad de grupo y, por tanto, como instrumento de solidaridad social; el balance entre riesgos y beneficios según los datos científicos es claramente favorable a la vacunación; el beneficio indirecto en la vida social, familiar y educativa del menor vacunado.
Señalemos una muestra de esta, con supuestos variados respecto a la discrepancia entre los padres:
- Auto Juzgado Primera Instancia e Instrucción núm. 7 de Avilés núm.º 11/22, de 13 de enero86: el caso responde a la capacidad para decidir sobre la inoculación de la vacuna COVID en una menor ante las discrepancias de sus progenitores, separados. Partiendo de que es innegable que desde la existencia de las vacunas, la mortalidad, la gravedad y las consecuencias que produce la infección por covid ha disminuido, y la asistencia sanitaria por causa grave corresponde proporcionalmente a más personas sin vacunar que vacunadas. Y que las personas vacunadas tienen no sólo menos riesgos de tener consecuencias graves en caso de infección, sino menor carga viral para transmitir frente a terceros, conlleva que, “de por sí, vacunar a la menor no va contra su interés, más aun cuando en el calendario de vacunas del año 2022 de la Asociación Española de Pediatría se incluye la vacunación de mayores de 5 años contra el covid, aparte de que las autoridades sanitarias españolas son las que facilitan y proporcionan la misma, no siendo una cuestión meramente nacional, sino mundial, y han considerado tras los estudios pertinente la conveniencia de vacunar a niños menores de más de 6 años, pues al día de hoy no hay estudios que consideren que a los menores les causa un mayor perjuicio para su salud la vacuna que no vacunarse”.
El Auto también valora que “el interés de la menor no es solo su salud, sino que, al ser dependiente y no autónoma, su interés es estar en todo momento cuidada, asistida y protegida por las personas que así lo vienen haciendo, y, estando demostrado que la capacidad de contagio es mayor en un niño no vacunado que en un vacunado, supondría un riesgo mayor para su entorno no vacunarse”. Además, el Auto trae a colación otros beneficios indirectos de la vacunación, como la posible mejora de su salud mental y su bienestar, el facilitar el regreso a la normalidad, incluida la presencialidad en las clases y de las interacciones sociales importantes para el desarrollo infantil, o el costo familiar de la enfermedad de sus padres, con el consiguiente impacto en la economía familiar y la situación de estrés crónico que puede generar para todos los miembros de la misma.
- Auto Juzgado Primera Instancia e Instrucción Tafalla (Provincia de Navarra) de 7 marzo 2022 (JUR\2022\162383). Se resuelve expediente de jurisdicción voluntaria (art. 86 Ley 15/2015 de 2 de julio de Jurisdicción Voluntaria) para la intervención judicial por desacuerdo en el ejercicio de la patria potestad, solicitando el padre que se dicte resolución "por la que se autorice la vacunación de dos hermanos, uno de ellos con TEA, contra COVID y gripe." El Auto se basa en los informes médicos que entienden pertinente y deseable la vacunación de ambos menores, e incluso recomendable para el menor con TEA (por ser uno de los grupos de riesgo). Es importante que el Auto judicial considera que: “es necesario matizar que con este procedimiento no se obliga a la vacunación de Diego e Edemiro, sino que se autoriza a uno de los dos progenitores (en este caso, el padre) para decidir sobre este punto concreto referente a la salud de sus hijos y sobre el que los progenitores no han alcanzado un consenso.
En atención a las circunstancias…, la petición del Sr. Constantino de atribuírsele la capacidad para decidir sobre este tema se considera justificada, resultando lo más ventajoso para los menores”.
- Auto Audiencia Provincial de Valladolid (Sección 1.ª) Auto núm. 180/2022 de 6 julio (JUR\2023\27386): resolviendo en apelación, en un supuesto también de disputa entre los progenitores, y habiendo resuelto el Juzgado la atribución de la capacidad para decidir sobre la administración de la vacuna Covid al padre de dos menores de 10 y 8 años, el Auto confirma la decisión, insistiendo en que: “ ha de recordarse que no es el Tribunal el que decide sobre la vacunación, sino que tan solo atribuye a uno u otro progenitor la facultad de decidir al respecto”. Se aplica el artículo 156.3 CC al objeto de decidir a quién de los dos se le atribuye la decisión sobre la vacunación, puesto que el indicado precepto reza así: "En caso de desacuerdo en el ejercicio de la patria potestad, cualquiera de los dos podrá acudir a la autoridad judicial, quien, después de oír a ambos y al hijo si tuviera suficiente madurez y, en todo caso, si fuera mayor de doce años, atribuirá la facultad de decidir a uno de los dos progenitores".
- También recuerda la doctrina sentada por el Auto de la Sección 2.ª de la Audiencia Provincial de Cantabria de 11 de abril de 2022, para señalar que en modo alguno debe entrar un tribunal “en una polémica científica, que adelantamos absolutamente estéril, sobre la bondad o no de la vacuna contra el COVID en los menores de 12 años… es tan solo el interés de éstos el que necesariamente ha de presidir los criterios para la resolución que se adopte”. Aun así, no deja de recordar la decisión judicial la no obligatoriedad de la vacuna, “pero con arreglo al informe del Médico Forense y a los criterios del Ministerio de Sanidad y de la Asociación Española de Pediatría acerca de la vacuna en menores de 5 a 11 años, la misma es beneficiosa para los menores (además de serlo para toda la sociedad en evitación de futuros contagios), a lo que debe añadirse la consideración de que ha sido autorizada por la Agencia Europea del Medicamento y aprobada para estas edades por la Agencia Española del Medicamento y Productos Sanitarios, con las consiguientes garantías de calidad, seguridad y eficacia”. Para terminar, señalando, como se hizo en anterior Auto 17 de febrero de 2022, “el balance riesgo/beneficio es claramente favorable a la vacunación. Conviene vacunarse para evitar contagiarse con el virus y poder padecer cualquiera de sus posibles complicaciones, incluso a pesar del riesgo de miocarditis y pericarditis más frecuentes en jóvenes pero que ocurren muy raramente, pues estas patologías son más frecuentes si se padece la infección natural del virus por contagio”.
- AP de Valencia (Sección 10.ª) Auto num. 299/2022 de 20 mayo (JUR\2022\269912): en este caso, también con disputa entre los progenitores, el hijo menor (de 12 años) se manifiesta a favor de recibir la vacuna, habiendo recibido información al respecto de ambos progenitores, por lo se le presume capacidad para entender los riesgos que implican ambas posturas, pues a partir de esas edad el legislador considera imprescindible la audiencia al menor antes de adoptar las decisiones que le afectan, salvo causa justificada. Si a ello se añade la conclusión del informe del médico forense respecto a la comparación entre los beneficios y los riesgos de la vacuna, pese a las dolencias (alergias, entre otras) que padece el menor, la conclusión es que la postura que mantiene el padre se encuentra en mejor sintonía con la voluntad del hijo y respaldada médicamente. El juez se limita a asignar a uno de los progenitores la facultad de decidir, siendo el facultado quien deberá resolver y llevar a efecto lo resuelto, en las condiciones que considera más beneficiosas para su hijo y teniendo en cuenta la voluntad del menor. Añadir por último, en cuanto a los derechos fundamentales de la apelante que para la resolución de la controversia se deben primar los del hijo menor de edad sobre los de sus progenitores (art.2 LO 1/1996).
- También contiene una doctrina elaborada, para el caso de la administración de la vacuna Covid en adolescentes, en caso de diferencias entre los progenitores, el Auto AP de Barcelona (Sección 18.ª) num. 329/2022 de 19 octubre (JUR\2023\60394), por la fundamentación fáctica de apoyo: “a mediados de 2021 la Comisión de Salud pública aprobó la recomendación de vacunación de la población adolescente sin antecedentes de reacciones alérgicas graves. A fecha 25 de octubre, la vacunación de adolescentes (12-19 años) con pauta completa alcanzaba al 82,0 %. La vacunación se presentaba pues como una medida necesaria de protección de la salud de la menor y ello implica el mayor beneficio de la menor del que dudaba el recurrente, y de la salud de los demás”. Y también por la jurídica, con apoyo en la doctrina del TEDH en una sentencia de 8-4-2021, Caso Vavrika y otros c. República Checa en un supuesto de negativa a vacunación de niños hace referencia a que según la jurisprudencia establecida por el Tribunal, “la vacunación obligatoria, como intervención médica involuntaria, es un injerencia en el derecho al respeto de la vida privada (art. 8) pero declara la injerencia como lícita en tanto perseguía el objetivo de proteger la salud y los derechos de los demás. En los casos planteados se consideró que las medidas adoptadas por el estado (multas y exclusión de la educación preescolar) podían considerarse necesarias en una sociedad democrática y que la necesidad se fundamenta en que la vacunación constituye la respuesta de las autoridades a la necesidad social urgente de proteger la salud individual y pública contra las enfermedades. Es decir, no se consideró que las medidas adoptadas para obtener la vacunación infringieran un derecho fundamental”.
- Auto AP (S.1.ª) Córdoba 265/2023, de 16 de junio (JUR 2024\214): donde repitiendo estos argumentos, avala la autorización para decidir sobre la administración de la segunda dosis de la vacuna, insistiendo en la no aparición de efectos adversos tras la primera inoculación.
- Audiencia Provincial de Cantabria (Sección 2.ª) Auto núm. 127/2023 de 10 octubre. JUR 2023\407288: es interesante esa resolución en tanto atribuye la facultad de decidir sobre vacunación hasta que el menor alcance la edad de doce años, momento en el que puede volver a revisarse la resolución judicial valorando las circunstancias concurrentes. Bien motivada, ante el desacuerdo sobre vacunación de los padres (biólogo y enfermera), se señala que: “El dictado de esta resolución judicial no puede estar presidido por la búsqueda de una verdad material de tipo científico (bondad o no de la vacuna) principio que no rige en el proceso civil a la vista de las limitaciones que para el mismo suponen los principios de alegación de parte, rogación y dispositivo. En consecuencia, no puede el tribunal entrar en una polémica científica sobre la bondad o no de la vacuna contra el COVID pues en el actual estado de conocimiento científico existen diversas y encontradas opiniones, muchas de aparente solvencia y otras no tanto, sobre la materia. Tal circunstancia excluye un examen científico pormemorizado de la abundante documentación sobre la cuestión”. Además, que “es un hecho notorio que la vacuna contra el COVID ha sido aprobada por la Agencia Europea del Medicamento y por la Agencia Española del Medicamento y Productos Sanitarios y está recomendada por los organismos públicos que según la CE deben velar por la salud de los españoles. La autorización sólo se concede cuando se comprueba que el promotor de la vacuna ha presentado y cumplido con todos los requisitos de calidad y eficacia del producto, contrastados además en las distintas fases del ensayo clínico”. Insistiendo en el hecho cierto de que existen en el ámbito científico serios desacuerdos sobre la conveniencia o no de la vacunación en menores, señala la resolución judicial que: “a la hora de establecer a cuál de los padres se le debe conceder la facultad de decidir sobre ello deberíamos inclinarnos por aquel que se encuentra amparado por los organismos oficiales. Sobre todo cuando en el presente caso se ha puesto de relieve que la menor no presenta enfermedades infectocontagiosas que supongan un problema añadido para la indicación de la vacuna del COVID, como se informó por su centro de salud. De la misma manera el informe forense llega a la conclusión de que la vacuna autorizada para administrar a este grupo de población: Comirnaty 10, es segura y eficaz en este grupo de edad. Habiéndose testado en Estados Unidos sin que hayan aparecido señales de alarma.
- Como se ha puesto de relieve por el auto de la Audiencia Provincial de A Coruña de 10 de enero de 2023: " ante una determinada situación sanitaria (pandemia) la respuesta de la administración competente es recomendar una determinada actuación sanitaria, y si ante tal situación uno de los padres sigue las recomendaciones de la administración competente en la materia y otro no, solo razones evidentes, compartidas de forma generalizada por los expertos y no visiones individuales o particulares (tan respetables como carentes de valor referencial), que constaten que tal recomendación es equivocada y que los riesgos de la administración de la vacuna no compensan sus ventajas, daría justificación a que el padre que se aparta -lo que no se duda que haga pensando que es lo mejor para su hijo- de lo recomendado por los organismos competentes en materia sanitaria sea quien deba decidir en tal disyuntiva".
| Decisiones judiciales que han hecho prevalecer el criterio contrario a la vacunación de uno de los progenitores |
Sin embargo, también hay algunas decisiones judiciales minoritarias que han seguido una línea contraria. Los argumentos principales han sido: la baja incidencia del Covid en menores de edad; los efectos adversos a largo plazo desconocidos; o la escasa certeza sobre la seguridad de la vacuna y el procedimiento acelerado utilizado para su autorización.
Veamos también una muestra de esta jurisprudencia.
Especialmente polémico fue el Auto de 10 de diciembre de 2021, del Juzgado de Primera Instancia n.º 2 de Icod de Los Vinos (Tenerife)87, En este caso, tanto el padre como su hijo menor de edad (al que se le concedió audiencia) optaban por la vacunación, frente a la madre que, para fundamentar su oposición, aportó abundante documentación que sirvió al juzgador para hacer prevalecer la decisión de la progenitora contraria a la vacunación. Los principales argumentos, basados en el “principio de prudencia” fueron:
- Baja incidencia de la covid en población menor de edad: en base a un informe del ISCIII, “La administración de una vacuna debe ir precedida de una ponderación de riesgos/beneficios, y en el presente procedimiento, ha quedado acreditado que los menores de edad apenas sufren las consecuencias del covid, atendiendo a la baja mortalidad (0,00023861%) y la baja hospitalización con pronóstico grave, en UCI (0,002484%), de los menores de 19 años, de forma que el posible beneficio que obtendría el menor de vacunarse es muy muy escaso".
- Efectos adversos desconocidos a largo plazo de la vacuna: “Es difícil, por no decir imposible, poner en una balanza los efectos adversos a medio o largo plazo de la vacuna del covid, cuando los mismos son desconocidos en el momento actual, de forma que, lo que se está poniendo en uno de los lados de la balanza es una interrogación, una incógnita, para la que a fecha de hoy nadie puede ofrecer una respuesta certera, pues nadie lleva varios años vacunado del covid… si bien desconocemos qué sucederá a medio o largo plazo, conforme consta en la documentación aportada por la progenitora, ya se han documentado efectos adversos graves a corto plazo, como lo son miocarditis y pericarditis, lo que sugiere cuanto menos, extremar la prudencia en la inoculación de la vacuna a los menores”.
- Escasa certeza sobre la seguridad de la vacuna, en base a su autorización condicional, ósea, sin haber finalizado sus ensayos clínicos.
- Rebate las “razones de solidaridad que se invocan para que el menor sea vacunado”, porque vacunar a los niños cuando el covid apenas tiene incidencia entre ellos, bajo el pretexto de que así protegen a sus abuelos, sería éticamente dudoso, máxime cuando hay mecanismos que se han revelado eficaces para evitar la propagación del virus”: y en segundo lugar vacunas que se suministran en España en la actualidad inmuniza frente al virus, ninguna evita el contagio ni impide la transmisión. De forma que, difícilmente se van a beneficiar los no vacunados de una inmunidad que no se da por el hecho de que los demás se vacunen”.
- Cuestionamiento de la eficacia de la vacunación para frenar contagios, basándose en los datos del Centro Nacional de Epidemiologia, para llegar a concluir: “Ello nos lleva a confirmar lo que ya se sabía, que las vacunas no inmunizan y a constatar igualmente, que nos movemos en un terreno de inseguridad científica, plagado de incertidumbre”.
Con argumentos muy similares, el Auto del Juzgado de Primera Instancia de Torrent (Provincia de Valencia/València) núm. 158/2022 de 30 marzo (JUR\2022\120666), abundaba en el caso en que no existe ningún informe médico que aconseje la vacunación; de que no consta que tenga ninguna patología previa de la que pueda derivarse que, en caso de padecer Covid, tenga un mayor riesgo a desarrollar síntomas graves; que hasta el momento el Covid 19, en niños de 5 a 11 años se ha desarrollado con síntomas leves, siendo minoritarios los graves, que en su mayoría padecían una patología previa; que actualmente ha disminuido de forma notoria la gravedad de la sintomatología; tampoco existe un conocimiento claro de los efectos secundarios que pueda tener la vacunación. Para concluir que “los argumentos del progenitor resultan más sólidos, al menos en este momento, que los de la progenitora solicitante: no puede justificarse la vacunación de un menor en el beneficio social que puede conllevar por la menor transmisibilidad, máxime teniendo en cuenta que, según los estudios, la transmisión de los menores es mucho menor que la de los adultos”.
En la mayoría de estos pronunciamientos judiciales se insiste en el hecho de que se desconocen por el momento los efectos secundarios que pudiera tener la vacuna a largo plazo:
Algún auto manifiesta que “los riesgos y efectos adversos de la vacuna covid, al igual que los de cualquier medicamento, fármaco o vacuna, pueden aparecer muchos años después de su ingesta o inoculación y que el hecho de que aparezcan tardíamente no significa que vayan a tratarse de efectos o secuelas leves, ya que nada obsta para que se trate de dolencias de gravedad” (Auto del Juzgado de Primera Instancia e Instrucción núm. 1 de Montilla y Juzgado de Violencia sobre la Mujer 81/2022, de 10 octubre 2022 (FJ 3º).
Otro pronunciamiento judicial reconoce que los estudios se han realizado “a marchas forzadas, no teniendo una perspectiva temporal suficiente para conocerlo en profundidad, lo que cabe extender a las vacunas que se han ido desarrollando que, si bien han dado signos de ser efectivas, se han elaborado de forma urgente y rápida, acortando los plazos que se suele exigir para la aprobación de este tipo de fármacos, por lo que tampoco se dispone de un conocimiento exacto de los efectos que dichas vacunas pueden producir” (Auto del Juzgado de Primera Instancia e Instrucción de Torrent 158/2022, de 30 marzo 2022, citado).
Incluso se recoge el contenido de “la ficha técnica del medicamento Comirnaty (Pfizer-BioNtech)” que señala que “la eficacia y seguridad de la vacuna no se podrá confirmar hasta diciembre de 2023” (Auto del Juzgado de Primera Instancia e Instrucción de Palencia, 10/2022, 1 febrero 2022 (FJ 2º)88. En este se señala que “para confirmar la eficacia y seguridad de Comimaty, el TAC deberá enviar el informe del estudio clínico final para el estudio aleatorizado, controlado con placebo y enmascaramiento para el observador. Fecha límite: Diciembre 2023”.
Audiencia Provincial de Jaén (Sección 1.ª) Sentencia núm. 210/2023 de 9 marzo. JUR 2023\283757: La resolución recurrida ante la Audiencia estimaba parcialmente la demanda de modificación de medidas presentada por parte del padre de una menor de 13 años y otra de 5, estableciendo “la obligación de la madre a vacunar a los dos menores del COVID, siguiendo el criterio médico del sistema nacional de salud”. La madre recurrió negándose a la vacunación por: se desconocen los efectos secundarios que pudiera producir la administración de la vacuna a los menores de 5 a 11 años; no se ha aportado al proceso ningún informe médico o diagnóstico que aconseje y justifique la vacunación solicitada; uno de sus hijos ya ha pasado la enfermedad y además está a la fecha de la demanda muy debilitada en cuanto a sus efectos.
Aun cuando la Audiencia reconoce que en los casos en los que se ha tenido que pronunciar sobre el suministro de la vacuna a ancianos o a menores de edad ha venido a resolver que es innegable que desde la existencia de las vacunas, la mortalidad, la gravedad y las consecuencias que produce la infección por Covid ha disminuido, y la asistencia sanitaria por causas grave corresponde proporcionalmente a más personas sin vacunar que vacunadas y que está acreditado que personas vacunadas tienen no sólo menos riesgos de tener consecuencias graves en caso de infección, sino menor carga viral para transmitir frente a terceros, en el caso objeto de autos se va a estimar el presente recurso de apelación y se va a eliminar la obligación de la madre a vacunar a los menores con base a los siguientes motivos:
- La vacunación no es obligatoria, y existe libertad de cada uno de tomar la decisión, y si ambos progenitores deciden no vacunar a sus hijos, nadie se lo impondrá. En este caso en principio el padre quería vacunar a los hijos menores, sin embargo, parece haberse perdido dicho interés por parte del progenitor paterno, pues como indica el propio menor en su exploración, indica que su padre le había permitido no vacunarse y que no tenía intención de obligarle a ello;
- El menor de 12 años y atendiendo a sus deseos y razones, manifiesta no querer vacunarse, puesto que ya ha pasado la enfermedad y que sufrió síntomas muy leves; en fin, la falta de concreción del informe médico al caso de autos y especialmente a la situación actual y la disminución del riesgo que ha supuesto esta enfermedad. Todo ello se entiende sin perjuicio de que a la vista de la modificación de la situación sanitaria y el empeoramiento de la situación el padre pueda recabar autorización judicial a través del correspondiente expediente de jurisdicción voluntaria para la prescripción de la vacuna de los menores.
Por todo ello, se estima el recurso de apelación y se revoca la resolución recurrida en el sentido de no obligar a la madre a la vacunación de sus hijos.
Otras decisiones judiciales que han mantenido esta línea son el Auto del Juzgado de Primera Instancia e Instrucción de San Lorenzo de El Escorial 119/2022, de 7 abril 2022, el Auto del Juzgado de Primera Instancia e Instrucción de Palencia 10/2022, de 1 febrero 2022 y el Auto 190/2022, 27 de junio 2022, del mismo Auto del Juzgado de Primera Instancia de Icod de los Vinos87.
Sin embargo, además de algunos errores jurídicos y confusiones de concepto en estas decisiones, como afirmar que la autorización condicional en España ha sido una autorización de emergencia, que no es lo mismo y que exige unos controles mucho mayores, estas sentencias ofrecen una interpretación muy corta del principio de prudencia, además de ser resultado de una lectura de la evidencia científica que ha terminado por demostrar lo contrario a lo que se afirma, en particular respecto a la seguridad y los efectos secundarios o adversos que se asocian a la vacuna en menores y adolescentes, sobre todo en relación a las miocarditis y pericarditis89.
| La respuesta en la doctrina consolidada del Tribunal Constitucional de los años 2023 y 2024 a las controversias sobre el consentimiento por representación de menores de edad. |
| El canon de constitucionalidad del interés superior del menor que avala la autorización judicial al progenitor del menor favorable a la vacunación |
En el último trimestre del año 2023 y primeros meses del 2024 el Tribunal Constitucional ha resuelto diversos asuntos relativos a la administración de la vacuna frente a la COVID-19 en supuestos de discrepancia entre progenitores. La STC 38/2023, de 20 de abril 2023 ya había sentado doctrina sobre la incidencia de la vacunación en el derecho fundamental a la integridad física en el caso de una persona con discapacidad, cuyos argumentos principales se extrapolan al caso de los menores de edad con los matices necesarios.
El leading case es la primera sentencia, la STC 148/2023, de 6 de noviembre de 2023 (BOE 18-12-2023,) en la que se resolverá el recurso de amparo formulado por un progenitor contrario a la administración de la vacuna Covid a su hijo, menor de edad, en base fundamentalmente a la vulneración del derecho a la integridad física y moral de su hijo. Esta Sentencia es la base para la resolución del resto de recursos, todos ellos planteados por el progenitor disconforme con la vacunación, encontrándonos supuestos de diferentes franjas etarias o de circunstancias concurrentes que, sin embargo, no cambian el núcleo de la doctrina constitucional (vid SSTC 154/2023, 155/2023, 156/2023, 157/2023, 158/2023, 159/2023, 160/2023, 162/2023 y 163/2023, todas ellas de 20 de noviembre 2023 (publicadas el 21 de diciembre 2023); SSTC 180/2023, 181/2023, 182/2023, 183/2023, 185/2023, 186/2023 y 187/2023, todas ellas de 11 de diciembre 2023 (publicadas el 18 de enero 2024); SSTC 4/2024, 5/2024, 6/2024, todas de 15 de enero, publicadas el 20 de febrero 2024).
En todas ellas el iter procesal precedente ante la discrepancia de los progenitores deriva del desarrollo del procedimiento de jurisdicción voluntaria (al que ya nos hemos referido) con el objeto de que un Juzgado de Primera Instancia (órgano competente en virtud del art. 86 LJV) decida mediante Auto a quien otorgar la decisión y facultad de decidir, en este caso, sobre la administración de una vacuna. En todos los casos también estas resoluciones judiciales habían sido impugnadas en apelación ante la correspondiente Audiencia Provincial.
La alegación principal de las demandas se refiere a la conculcación del derecho a la integridad física y moral de los menores, que será rechazado por el TC por haberse cumplido con el presupuesto básico que el art. 9.3, letra c) de la Ley 41/2002 establece para que pueda acudirse al consentimiento por representación –otorgado por los progenitores de común acuerdo o por la autoridad judicial en caso de desacuerdo– porque el menor carecía de la capacidad emocional e intelectual necesarias para comprender el alcance la intervención y los padres contaban con la información adecuada para la prestación del consentimiento desde un momento anterior incluso a la iniciación del procedimiento de jurisdicción voluntaria. Además, también se ha cumplido con el requisito de la motivación de las resoluciones judiciales, ya que tuvieron como fundamento esencial la protección del interés superior del menor en relación con la protección de su salud, teniendo en cuenta la recomendación de las autoridades sanitarias, que se mostraban a favor de la vacunación de menores haciendo una ponderación de riesgos y beneficios de la vacuna, que el TC no ha estimado desvirtuadas por los informes que aportó la recurrente. En las SSTC 5/2024 y 6/2024 también se resume la doctrina para el caso de menores con 13 años y 17, para atribuirles la capacidad suficiente, en el primero por la madurez que se le presume al menor y que se constata en la vía judicial previa, en el segundo por contar con más de 16 años de edad, para consentir sobre la administración de la vacuna. Al hilo de esta doctrina el TC realiza también precisiones importantes sobre el derecho a la información en materia vacunal.
Extractamos aquí las principales líneas argumentales de esta doctrina:
El TC comienza afirmando que la vacunación constituye un acto sanitario que consiste en la inoculación de un «preparado» de productos biológicos en el cuerpo humano a efectos de provocar una respuesta inmunitaria, “por lo que su administración entra, con claridad, dentro de las facultades de autodeterminación garantizadas por el derecho a la integridad personal del art. 15 CE”. También porque se trata de una actuación que puede producir efectos secundarios adversos (no deseados), aunque sean estadísticamente minoritarios, lo que determina, asimismo, un riesgo potencial para la salud.
Desde esta premisa el TC analiza el canon de constitucionalidad aplicable a la vacunación de personas menores de edad, que basará en estos argumentos:
- La administración de una vacuna, en cuanto medida injerente en el derecho fundamental a la integridad personal, requerirá para su constitucionalidad del consentimiento libre, válido e informado de la persona afectada. Cuando falte ese consentimiento o no pueda obtenerse por el motivo que sea, la constitucionalidad de la administración de la vacuna queda supeditada al cumplimiento de los requisitos que rigen la restricción de los derechos fundamentales sustantivos: (i) que la medida o actuación limitativa del derecho fundamental de que se trate esté prevista por la ley (habilitación legal), con la debida calidad normativa en la definición del supuesto de hecho y de sus consecuencias; (ii) que sea autorizada por resolución judicial que contenga una motivación reforzada relativa a la legitimidad constitucional de la medida autorizada; (iii) que esté dirigida al cumplimiento de un fin constitucionalmente legítimo; y (iv) que respete el principio de proporcionalidad, por derivarse de ella más beneficios o ventajas que perjuicios sobre otros bienes o valores en conflicto
- Habilitación legal para el supuesto de personas menores de edad: el art. 9, apartado 3, letra c) de la Ley 41/2002 articula la fórmula del «consentimiento por representación», que se atribuye a los representantes legales de la persona menor, siempre y cuando esta «no sea capaz intelectual ni emocionalmente de comprender el alcance de la intervención» y después de haber escuchado su opinión con arreglo a lo dispuesto en el art. 9 de la Ley Orgánica 1/1996, de 15 de enero, de protección jurídica del menor, (en adelante, Ley Orgánica 1/1996).
En el régimen general de representación de personas menores de edad recogido en el Código civil (CC), se atribuye el ejercicio de dicha representación legal a los progenitores, que la ejercerán de manera conjunta como regla general (arts. 154 y 156 CC) salvo defecto, ausencia o imposibilidad de uno de ellos, en cuyo caso la representación legal, como parte de las facultades que integran la patria potestad, será ejercida exclusivamente por el otro. Los desacuerdos entre los progenitores en el ejercicio de la facultad de representación de sus hijos e hijas menores de edad habrán de resolverse por la autoridad judicial (art. 156 CC) a través del expediente de jurisdicción voluntaria.
- Presupuestos del consentimiento por representación ante actuaciones sanitarias. Aquel precepto parte de la premisa de que la minoría de edad no implica per se la falta de capacidad para la prestación del consentimiento informado, ni autoriza el recurso automático al consentimiento por representación, que solo será legítimo si menor de edad carece de la capacidad intelectual o emocional necesarias para comprender el alcance de la intervención. En el mismo sentido, el art. 2.1 de la Ley Orgánica 1/1996, de 15 de enero, de protección jurídica del menor, dispone en su segundo párrafo que «[l]as limitaciones a la capacidad de obrar de los menores se interpretarán de forma restrictiva y, en todo caso, siempre en el interés superior del menor».
Recordando la doctrina de la STC 154/2002, de 18 de julio, FJ 10, se precisa que: (i) el reconocimiento excepcional de la capacidad del menor respecto de determinados actos jurídicos, como son los que afectan a su integridad física, no es de suyo suficiente para, por vía de equiparación, reconocer en todo caso eficacia jurídica a los actos –o decisiones– del menor; (ii) la exclusión de la representación legal en tales casos debe entenderse siempre sin perjuicio del deber de los progenitores de velar y cuidar del menor y salvaguardar su interés superior, obligaciones que no desaparecen por el hecho de que se reconozca a la persona menor cierto grado de autodeterminación; (iii) la validez y eficacia de las decisiones adoptadas por una persona menor de edad en ejercicio de su derecho a la integridad física habrán de determinarse teniendo siempre en cuenta la prevalencia de su interés superior, que ha de ser siempre tutelado por los padres y, en su caso, por los órganos judiciales, poniendo dicho interés en relación con los efectos previsibles de tales decisiones y su eventual permanencia o irreparabilidad.
En definitiva, la capacidad general de autodeterminación de las personas que todavía no hayan alcanzado la mayoría de edad en relación con las actuaciones médicas que les afectan encuentra su límite en la protección de su interés superior, que se impone como obligación a los progenitores, en cuanto titulares de la patria potestad o autoridad familiar, y a todos los poderes públicos, incluida la autoridad judicial. A todos ellos corresponde garantizar que la decisión final relativa a la actuación médica en cuestión no trae consigo una quiebra relevante, persistente y/o irreparable de dicho interés superior.
Por otra parte, el art. 9.3, letra c) de la Ley 41/2002 exige que, con carácter previo a la prestación del consentimiento por los representantes legales, se escuche la opinión de la persona menor concernida, con arreglo a lo dispuesto en el art. 9 de la Ley Orgánica 1/1996. Este precepto viene a desarrollar el derecho de las personas menores de edad a ser oídas y escuchadas en cualquier procedimiento administrativo, judicial o de mediación en que estén afectadas, así como el derecho a que su opinión sea tenida en cuenta en función de su edad y madurez, madurez que habrá de ser valorada por personal especializado, considerándose que en todo caso tienen madurez suficiente quienes hubieren cumplido los doce años (art. 9.2 de la Ley Orgánica 1/1996).
En su aplicación al caso, el TC asume las conclusiones de la fiscal, destacando que no consta informe profesional ni datos que permitan afirmar que la menor de 11 años contaba con la madurez a que se refiere el art. 9.3 c) de la Ley 41/2002 a efectos de responsabilizarse del acto de consentir con exclusión de sus padres. Por el contrario, del examen del expediente judicial se desprende que ambos progenitores asumieron de consuno el hecho de que la menor carecía de la capacidad emocional e intelectual para que pudiera prestar el consentimiento informado por sí misma y de forma autónoma; y que, en consecuencia, habían de ser ellos, en cuanto titulares de la autoridad familiar, quienes habían de prestarlo –o declinarlo– por representación. Los órganos judiciales tampoco pusieron en cuestión esta asunción de los progenitores, que no podía tacharse de injustificada dada la evidente complejidad científico-médica de la cuestión dirimida, de la que cabía inferir razonablemente que una menor, de once años, no había de contar con la capacidad intelectiva ni los elementos de juicio científico-técnicos precisos para emitir un consentimiento informado por sí misma.
En relación con este extremo, el TC se refiere a la omisión de la opinión de la menor, que justifica en que el procedimiento pasaba por efectuar una compleja ponderación de los riesgos y beneficios de la vacunación frente a la Covid-19 y requería, para un adecuado análisis, de la capacidad de comprender y someter a juicio crítico documentos médico-científicos contrapuestos que, a su vez, utilizaban argumentos técnicos, propios de la medicina, la farmacología y la estadística aplicada, notablemente sofisticados e intrincados. En este particular contexto, tanto los progenitores de la menor como los órganos judiciales asumieron plenamente el hecho de que una niña de once años no había de contar con los elementos de juicio precisos para poder llevar a cabo un análisis de la cuestión suficientemente profundo como para formarse una opinión que respondiera adecuadamente a su superior interés,
Finalmente, en lo relativo a la información que debe prestarse con carácter previo a la prestación del consentimiento (por la persona afectada o por quienes están llamados a prestarlo por representación), se argumenta en la demanda de amparo que no se entregó a los progenitores un consentimiento informado por escrito sobre la composición, riesgos y consecuencias de la administración de la «mal denominada “vacuna Covid-19”», en los términos exigidos por la Ley 41/2002. La información a que se refiere este argumento impugnatorio es la regulada en el art. 4 de la citada Ley y comprende, como mínimo, la finalidad y la naturaleza de cada intervención, sus riesgos y sus consecuencias. Deberá ser verdadera y habrá de proporcionarse a la persona que ha de prestar el consentimiento de manera comprensible y adecuada a sus necesidades, todo ello con la finalidad de ayudarle a adoptar la decisión que corresponda «de acuerdo con su propia y libre voluntad» (art. 4.2 de la Ley 41/2002). La Sentencia rechaza esta argumentación, pues en el proceso judicial previo se constató sobradamente la información que conocían ambos progenitores
- Obligación de los representantes legales de actuar en función del interés superior del menor. En el momento de prestar el consentimiento estos no gozan de libertad para decidir lo que consideren conveniente según su propio criterio, sino que vienen directamente vinculados por la obligación de actuar en interés de la persona menor de edad, de acuerdo con su personalidad y con respeto a sus derechos y a su integridad física y mental (art. 154 CC).
Este marco de protección se encuentra presidido por el art. 39 de nuestra Constitución, que en su apartado 3 dispone que «[l]os padres deben prestar asistencia de todo orden a los hijos habidos dentro o fuera del matrimonio, durante su minoría de edad y en los demás casos en que legalmente proceda»; y en su apartado 4 añade, en consonancia con lo establecido en el art. 10.1 CE, que «[l]os niños gozarán de la protección prevista en los acuerdos internacionales que velan por sus derechos».
El interés superior del menor es la consideración primordial a la que deben atender todas las medidas concernientes a los menores que tomen las instituciones públicas o privadas de bienestar social, los tribunales, las autoridades administrativas o los órganos legislativos; y en que, en caso de que no puedan respetarse todos los intereses legítimos concurrentes, deberá primar el interés superior del menor sobre cualquier otro interés legítimo que pudiera concurrir (STC 64/2019, de 9 de mayo, FJ 4, por todas).
Por otra parte, cuál sea en cada caso el interés superior del menor tampoco puede determinarse de manera libre por los representantes legales y según su propio criterio, sino tomando en consideración los criterios legalmente establecidos en el art. 2 de la Ley Orgánica 1/1996 con carácter general, y en las leyes especiales que regulen de manera específica la materia a que se refiera la decisión; en concreto y en el caso que nos ocupa, los apartados 6 y 7 del artículo 9 de la Ley 41/2002. De este modo, la decisión de los representantes legales relativa al otorgamiento o no del consentimiento informado por representación deberá atender a «[l]a protección del derecho a la vida, supervivencia y desarrollo del menor y la satisfacción de sus necesidades básicas, tanto materiales, físicas y educativas como emocionales y afectivas» [art. 2.2, letra a) de la Ley Orgánica 1/1996] y buscar el mayor beneficio para la vida o salud del paciente que no ha adquirido la mayoría de edad, teniendo en cuenta las circunstancias concurrentes y las necesidades del menor que han de ser atendidas (art. 9, apartados 6 y 7 de la Ley 41/2002).
En su aplicación al caso, el TC entiende que del contenido de las resoluciones judiciales impugnadas se desprende que la decisión de autorizar la vacunación tuvo como fundamento primero y esencial la protección del interés superior de la propia menor en sus dos vertientes fundamentales: protección de la salud física individual frente a una eventual infección por Covid-19; y protección de la salud mental mediante la preservación de sus relaciones interpersonales en el entorno social, familiar y escolar, finalidades ambas plenamente legítimas desde el punto de vista constitucional (en el sentido analizado en apartado 3.5.3, remisión).
__________
85 https://www.icaoviedo.es/res/comun/biblioteca/1027/AP%20PONTEVEDRA.pdf
86 Un comentario ampliado de esta decisión judicial, en este Manual, https://vacunasaep.org/profesionales/noticias/una-sentencia-judicial-destaca-el-valor-individual-y-social-de-las-vacunaciones. También el comentario de Federico de Montalvo, calificando la resolución como ejemplar en: https://theconversation.com/un-auto-judicial-ejemplar-a-proposito-de-la-vacunacion-de-los-ninos-frente-a-la-covid-175542
87 Un buen análisis de esta jurisprudencia sobre vacunación covid de menores, en MORENO SOLER, V., “El régimen jurídico de la vacuna contra la COVID-19 en la actualidad: de la imposición general a la resolución de conflictos entre progenitores”, Actualidad Jurídica Iberoamericana Nº 17 bis, diciembre 2022.
88 Este auto es uno de los pronunciamientos judiciales que contiene más informes, datos de evolución y decisiones en otros Estados. Así, puede verse también evidencias de la Alta Autoridad Sanitaria francesa (HAS) (Haute Autorité de Santé - Covid-19: la HAS précise la place de Spikevax® dans la stratégie vaccinale (has-sante.fr); un estudio europeo (Questions and answers on COVID-19_ Children aged 1 – 18 years and the role of school settings); otro de la Universidad de Columbia, denominado Vacunación COVID y riesgo de mortalidad por todas las causas estratificado por edad, realizado por Spiro Pantazatos y Herve Seligmann; por citar algunos.
89 Como demuestran las evidencias científicas y la información actualizada que puede comprobarse en la página del Centro para el Control y Prevención de Enfermedades Estadounidense CDC, en:
https://espanol.cdc.gov/coronavirus/2019-ncov/vaccines/safety/myo-outcomes.html
3.6.3. Breve referencia a las reglas de la patria potestad y consentimiento en el caso de menores con discapacidad tras la Ley 8/2021, de 2 de junio, por la que se reforma la legislación civil y procesal para el apoyo a las personas con discapacidad en el ejercicio de su capacidad jurídica. (BOE» núm. 132, de 03/06/2021)
Aunque sea brevemente, es preciso tener en cuenta que esta Ley 8/2021 es de aplicación en el caso de un menor con discapacidad. Se modifica el artículo 156 CC, aunque las reglas son similares a las señaladas en la legislación general:
«La patria potestad se ejercerá conjuntamente por ambos progenitores o por uno solo con el consentimiento expreso o tácito del otro. Serán válidos los actos que realice uno de ellos conforme al uso social y a las circunstancias o en situaciones de urgente necesidad.
En caso de desacuerdo en el ejercicio de la patria potestad, cualquiera de los dos podrá acudir a la autoridad judicial, quien, después de oír a ambos y al hijo si tuviera suficiente madurez y, en todo caso, si fuera mayor de doce años, atribuirá la facultad de decidir a uno de los dos progenitores. Si los desacuerdos fueran reiterados o concurriera cualquier otra causa que entorpezca gravemente el ejercicio de la patria potestad, podrá atribuirla total o parcialmente a uno de los progenitores o distribuir entre ellos sus funciones. Esta medida tendrá vigencia durante el plazo que se fije, que no podrá nunca exceder de dos años. En los supuestos de los párrafos anteriores, respecto de terceros de buena fe, se presumirá que cada uno de los progenitores actúa en el ejercicio ordinario de la patria potestad con el consentimiento del otro.
En defecto o por ausencia o imposibilidad de uno de los progenitores, la patria potestad será ejercida exclusivamente por el otro.
Si los progenitores viven separados, la patria potestad se ejercerá por aquel con quien el hijo conviva. Sin embargo, la autoridad judicial, a solicitud fundada del otro progenitor, podrá, en interés del hijo, atribuir al solicitante la patria potestad para que la ejerza conjuntamente con el otro progenitor o distribuir entre ambos las funciones inherentes a su ejercicio.»
El art. 287 se refiere expresamente al consentimiento en materia de salud, en estos términos:
“El curador que ejerza funciones de representación de la persona que precisa el apoyo necesita autorización judicial para los actos que determine la resolución y, en todo caso, para los siguientes: 1.º Realizar actos de transcendencia personal o familiar cuando la persona afectada no pueda hacerlo por sí misma, todo ello a salvo lo dispuesto legalmente en materia de internamiento, consentimiento informado en el ámbito de la salud o en otras leyes especiales”.
En caso de que estos actos recayeran en el guardador de hecho, el artículo 264 establece: cuando, excepcionalmente, se requiera la actuación representativa del guardador de hecho, este habrá de obtener la autorización para realizarla a través del correspondiente expediente de jurisdicción voluntaria, en el que se oirá a la persona con discapacidad. La autorización judicial para actuar como representante se podrá conceder, previa comprobación de su necesidad, en los términos y con los requisitos adecuados a las circunstancias del caso. La autorización podrá comprender uno o varios actos necesarios para el desarrollo de la función de apoyo y deberá ser ejercitada de conformidad con la voluntad, deseos y preferencias de la persona con discapacidad.
En todo caso, quien ejerza la guarda de hecho deberá recabar autorización judicial conforme a lo indicado en el párrafo anterior para prestar el consentimiento.
Sin embargo, la importancia de esta norma radica en que supone un enorme cambio de paradigma, al sustituir el criterio del mejor interés de la persona con necesidad de apoyos en su capacidad —la beneficencia final—, por el respeto a su autonomía personal. Por lo que pueden verse afectados los deberes de información asistencial y los requisitos de la prestación del consentimiento informado actualmente regulado en la Ley 41/2002.
Sin embargo, queda la duda sobre si debemos marcar diferencias con la representación legal de los menores por sus padres o tutores, que deben actuar siempre en beneficio del menor, esto es, que oírlos y tener en cuenta su opinión no implica seguirla necesariamente. La regla es bien distinta si se trata de una persona con necesidad de apoyos en el ejercicio de su capacidad que requerirá, precisamente, respetar su voluntad, deseos y preferencias, y llegado el caso, interpretar su trayectoria vital para deducir cuáles habrían sido estos de haber podido actuar sin representación.
La cuestión, tal como la formula GONZÁLEZ CARRASCO, “es si ello es exactamente así en el ámbito de las decisiones a adoptar en el ámbito sanitario, o si en el ámbito que nos ocupa existe algún límite que autorice, y que incluso obligue al curador representativo a actuar en beneficio de la salud y de la vida de la persona con discapacidad. En definitiva, se trata de saber si el apdo. 6 del art. 9 LAP ha de seguir vigente tras la Ley 8/2021, a pesar de que establece el deber del representante de adoptar la decisión atendiendo siempre al mayor beneficio para la vida o salud del paciente en cualquiera de los supuestos descritos en los apdos. 3 a 5, ordenando la puesta en conocimiento de la autoridad judicial de aquellas decisiones contrarias a tal interés, para que adopte la resolución correspondiente, y legitimando a los facultativos para adoptar las medidas necesarias en salvaguarda de la vida o salud del paciente en casos de urgencia, amparados por las causas de justificación de cumplimiento de un deber y de estado de necesidad”90.
En su opinión, estas reglas deben entenderse perfectamente subsistentes, a pesar del giro autonomista del nuevo paradigma en materia de capacidad. Primero porque a diferencia de lo previsto en el caso del menor mayor de 16 años en el art. 9.4 LAP -donde sí es relevante su autonomía-, no se está planteando aquí la posibilidad de representar al paciente discapacitado en atención al grave riesgo de la intervención, sino la necesidad de controlar judicialmente la decisión del representante si fuera contraria a la salud o a la vida de este. Pensemos en un apoyo representativo que decida rechazar o iniciar un tratamiento alternativo más arriesgado. La excepcionalidad de la actuación representativa en la Ley 8/2021 es cierto que implica que habrá fracasado todo intento de determinar la voluntad, deseos y preferencias de la persona representada. Como señala la autora, estaríamos aquí ante una decisión heterointegrada que ya habrá dejado atrás el principio de autonomía y que, por lo tanto, no puede primar sobre el deber de los poderes públicos de salvaguardar la vida y la integridad física de la persona con discapacidad (arts. 17 y 25 de la Convención de Nueva York y art. 10 del TR RDLeg 1/2013).
En segundo lugar, la propia modificación del art. 287 CC por la Ley 8/2021 da cuenta de las especialidades del ámbito sanitario cuando, tras enumerar los actos para los que el titular de la función representativa requiere autorización judicial, se remite a lo dispuesto en la legislación específica en materia de consentimiento informado y de internamiento no voluntario de la persona con discapacidad, lo que supone la subsistencia expresa de las cautelas.
Esta además ha sido la interpretación de las nuevas reglas por la STS (1.ª) de 8 de septiembre de 2021 (RJ 2021\4002), al entender la «crueldad social» de no intervenir sustituyendo la voluntad en contra manifestada por la persona afectada por un trastorno mental (en el caso, síndrome de Diógenes), que es, precisamente, el que no le permite ser consciente del proceso de degradación personal que sufre.
Como conclusión, estamos de acuerdo en que el art.9.6 Ley 41/2002 ha de seguir formando parte de la regulación legal del consentimiento informado a pesar del nuevo giro autonomista como paradigma en materia de capacidad. Generalizando la regla establecida en la legislación especial dirigida a determinadas intervenciones en el ámbito de la salud, la futura modificación de la LAP debería incorporar la necesidad de contar con el consentimiento de la persona requerida de apoyo junto con el de su representante, en función de su grado de autodeterminación, a través de una información adecuada a sus posibilidades de comprensión y garantizando así el ámbito de seguridad de la actuación del profesional sanitario91.
| Los jueces autorizan la vacunación obligatoria frente a la COVID-19 de ancianos con discapacidad, en contra del criterio de sus representantes. La posible extensión de esta doctrina en el caso de menores y la doctrina del TC sobre el canon de constitucionalidad basado en el interés superior del menor y la ponderación de las circunstancias personales y concurrentes |
Una cuestión importante también en época de pandemia ha sido la negativa de los representantes de las personas con incapacidad (normalmente, ingresados en residencias de ancianos) a que éstos sean vacunados, cuestión sobre la que se vienen pronunciando los Juzgados y Tribunales, la propia Fiscalía del Tribunal Supremo, e incluso el Tribunal Constitucional, como veremos a continuación.
El Auto de 4 de febrero de 2021, Juzgado de Primera Instancia núm. 16 Granada92 analiza el caso de un anciano con deterioro físico importante (Alzheimer, problemas bronquiales) PCR (-) con anticuerpos (+), sin pleno uso de sus facultades mentales e ingresado en una residencia de ancianos, cuyo hijo se niega a la vacunación frente a la COVID-19. La Consejería de Salud y Familias de la Junta de Andalucía puso el caso en conocimiento del Juzgado de incapacidades e internamientos competente.
Según informe del Médico Forense, emitido al efecto, no es imprescindible vacunar, bastaría con un control para verificar pérdida de inmunidad y, en su caso, vacunar.
Sin embargo, la decisión del Magistrado-Juez es que la decisión del representante debe adoptarse siempre atendiendo al mayor beneficio para la vida o la salud del paciente: el derecho a la salud debe prevalecer sobre la opinión contraria del familiar de referencia, teniendo en cuenta, además, que la posibilidad de sufrir una nueva infección no habría desaparecido, por lo que en las actuales circunstancias el riesgo de no vacunarse sería mucho mayor que el de hacerlo (art. 9.6 Ley 41/2002).
Por ello, autoriza al servicio médico-sanitario de la residencia al suministro de la vacuna contra el coronavirus SARS-CoV-2 al residente a pesar de la voluntad de su hijo.
Otros fallos similares son:
- Auto del Juzgado de Primera Instancia núm. 6 de Santiago de Compostela de 20 de enero de 2021, núm. 60/2021, rec. 32/2021: donde a pesar de la negativa del propio paciente con discapacidad, con argumentos similares a los expuestos, considera que el consentimiento informado por sustitución prestado por la entidad que lo tutela para la administración de la vacuna contra la COVID-19 debe ser otorgado93.
- Auto del Juzgado de Primera Instancia núm. 17 de Sevilla (Familia) de 15 de enero de 202194, tras comunicación de la Directora de la Residencia de Mayores en la que se encuentra ingresada una anciana con discapacidad de la negativa de la hija a autorizar la vacuna contra la COVID-19, el Ministerio Fiscal interesa la vacunación de la anciana, con informe favorable del Médico Forense (tanto en lo relativo a la seguridad de la vacuna, como en la indicación de la misma, sin que concurra contraindicación alguna en el caso de la residente). El Juzgado autoriza al Servicio Médico-sanitario de la residencia al suministro de la vacuna contra la Covid-19 a la residente, en las fechas y dosis previstas.
Obsérvese que el procedimiento judicial para la autorización de la vacunación es distinto al expuesto en el apartado 2.2 del presente capítulo, porque no estamos ante actos administrativos dictados por la autoridad competente en materia de salud pública (cuya revisión corresponde a la jurisdicción contencioso-administrativa), sino ante negativas del representante legal de menores y/o incapaces a que se les administre una vacuna, cuyo conocimiento corresponde a la jurisdicción civil, como detalla el auto analizado:
“Cuando se trate de personas cuya capacidad sea o deba ser modificada judicialmente, y cuya guarda o protección se encuentre bajo un cargo tutelar, o guarda de hecho, la protección de su salud constituye un deber de quien ejerce la citada protección y guarda, que debe ser ejercitada en su beneficio, quedando bajo la salvaguarda de la autoridad judicial, tal como lo prescribe el artículo 216 del CC.
En caso contrario, y por remisión del artículo 216 del CC, al artículo 158 del mismo texto legal, el juez podrá de oficio o a instancia de parte, entre otras, adoptar cualquier disposición a fin de apartar al menor-por remisión a la persona con presunta discapacidad-, de algún peligro, o de causarle algún perjuicio.
Esta idea de protección a la persona con capacidad disminuida se reproduce en la actual Ley de jurisdicción voluntaria, en los artículos 87 y ss., relativos a las medidas de protección al ejercicio inadecuado de la potestad de guarda de personas con capacidad modificada judicialmente (…).
(…) Nos encontramos ante un expediente de medidas cautelares, por un posible ejercicio inadecuado de la guarda de hecho, ante la negativa del familiar de referencia de otorgar su consentimiento para la citada vacunación”.
- También han sido numerosos los casos resueltos en sede judicial, respondiendo a la alegación de que una persona con necesidad de apoyo para el ejercicio de su capacidad que se encuentre en una residencia no tiene la consideración de paciente, a los efectos de la aplicación de las reglas del consentimiento. Sin embargo, la jurisprudencia es clara frente a este argumento: “la asistencia sanitaria para el mantenimiento de la salud también confiere la condición de paciente a los efectos de aplicación de la Ley 41/2002, cuyo artículo 9.6 dispone:
"En los casos en los que el consentimiento haya de otorgarlo el representante legal o las personas vinculadas por razones familiares o de hecho en cualquiera de los supuestos descritos en los apartados 3 a 5, la decisión deberá adoptarse atendiendo siempre al mayor beneficio para la vida o salud del paciente. Aquellas decisiones que sean contrarias a dichos intereses deberán ponerse en conocimiento de la autoridad judicial, directamente o a través del Ministerio Fiscal, para que adopte la resolución correspondiente, salvo que, por razones de urgencia, no fuera posible recabar la autorización judicial, en cuyo caso los profesionales sanitarios adoptarán las medidas necesarias en salvaguarda de la vida o salud del paciente, amparados por las causas de justificación de cumplimiento de un deber y de estado de necesidad." (Auto medidas cautelares Audiencia Provincial de Valencia (Sección 10.ª) num. 220/2022 de 11 abril; JUR\2022\225817)
La aplicación de esta normativa en supuestos similares aparece recogida en el Auto de esta Sala de fecha 4-6-2021 y en resoluciones de otras Audiencias Provinciales, como los Autos de la AP de Ourense de fecha 22-11-2021, AP de Santander de 3-11-2021 y 14-12-2021, AP de Jaén de 16-12-2021 y AP de Sevilla de 8-10-2021 y 13-10-2021.
Frente al criterio seguido por estas resoluciones judiciales, la Fiscalía del Tribunal Supremo emitió un dictamen el 24 de febrero de 2021 en contra de las vacunaciones forzosas contra la COVID-19 en residencias de ancianos95, afirmando que: “En tanto que la ley no establezca obligación de vacunarse, no cabe invocar razones genéricas de salud pública o específicamente basadas en la especial vulnerabilidad de determinados grupos de personas para justificar la administración forzosa de la vacuna”. El texto defiende la libertad de decisión individual para prestar o negar el consentimiento a las inyecciones.
Estas decisiones, explica la Fiscalía, se sustentan generalmente en razones de salud pública vinculadas al riesgo inherente a la expansión del contagio, la gravedad de la pandemia y, en particular, a la especial afectación a grupos vulnerables.
Pero, en opinión de este órgano, no son razones aptas para imponer la vacunación forzosa, ya que ni la legislación sanitaria ordinaria ni el decreto del estado de alarma se establece el carácter obligatorio de estos medicamentos. “Por lo tanto el propio legislador somete la administración de la vacuna a un régimen de libre consentimiento”, reza el texto, que también establece que en el caso de que el consentimiento tenga que otorgarlo un representante legal habrá que atender siempre “al mayor beneficio para la vida o la salud del paciente”. Es decir, si por ejemplo una persona con la tutela de un familiar se niega a que le vacunen, habrá que ponerlo en conocimiento de la autoridad judicial para que esta decida. Si hay “razones de urgencia”, serán los profesionales sanitarios los que determinen si administrar o no la dosis.
Sin embargo, dicho dictamen se refiere a la imposibilidad de imponer en la vía judicial civil una vacuna por razones ajenas al interés concreto de la persona vulnerable, esto es: el juez civil no puede imponer una vacuna basándose en razones de salud pública, sino en razones de protección individualizadas. En nuestro caso, habría que calibrar las decisiones en base al criterio del interés superior del menor. Por ello, la solución, como el propio dictamen sugiere, es otra cuando no se habla de una autorización civil para la vacunación en contra del criterio del representante legal (que era el caso enjuiciado), sino de la posibilidad de que un acto administrativo imponga una vacunación condicionante de actividades por razones de salud pública avalada a través de los trámites previstos en los arts. 8 y ss. LJCA (por ejemplo, admisión en una guardería pública).
La cuestión no es baladí, hasta el punto que ya se ha pronunciado nuestro Tribunal Constitucional en Auto (Pleno) núm. 139/2022 de 26 octubre (RTC\2022\139 AUTO) desestima la solicitud de suspensión de un Auto del Juzgado de Primera Instancia núm. 2 de Telde, por el que el órgano judicial resolvió “autorizar al servicio médico sanitario de la residencia de Ingenio, al suministro de la vacuna contra el Covid-19 ARNm -Comirnaty-" a paciente de edad avanzada, con la enfermedad de Alzheimer, dada la negativa del demandante de amparo, tutor de esta última, a consentir que se le aplicara esa medida terapéutica. Como señala el TC en el asunto “concurre una especial trascendencia constitucional (art. 50.1 LOTC), porque plantea un problema o afecta a una faceta de un derecho fundamental sobre el que no hay doctrina; y porque el asunto trasciende del caso concreto, al concernir a una cuestión jurídica de relevante y general repercusión económica y social”. El TC, valorando las circunstancias personales de la paciente, entiende que el otorgamiento de la suspensión interesada es susceptible de perturbar gravemente de sus derechos fundamentales, habida cuenta de la situación de semi aislamiento a la que por razones sanitarias quedó sujeta al ser la única interna no vacunada, con el consiguiente deterioro que esta medida supone para su indemnidad física y mental. Por tanto, levantando la suspensión, se autorizó la inoculación de la anciana96.
Posteriormente, la STC 4/2024, de 15 de enero, ha avalado también la autorización judicial de administración de la vacuna a una persona mayor que no puede decidir por sí misma, frente al criterio de una de sus hijas y la no oposición de otros dos hijos -sus guardadores de hecho- con la que convivía.
Este recurso de amparo se dirige contra el auto de 29 de septiembre de 2021, dictado por el Juzgado de Primera Instancia núm. 15 de Las Palmas de Gran Canaria, recaído en procedimiento de jurisdicción voluntaria, que acordó la administración de la vacuna frente a la covid-19 por parte del Servicio Canario de Salud a la madre de la recurrente, aquejada de una demencia severa que le impedía prestar por sí misma consentimiento a dicha actuación sanitaria. La demanda también se dirige contra el auto de 11 de marzo de 2022, de la Audiencia Provincial de Las Palmas Sec. 3.ª, apelación 1576-2021), que desestimó el recurso de apelación presentado por la demandante de amparo contra la resolución anterior.
Estando en discusión la vulneración del art. 15 CE, son plenamente trasladables al presente supuesto los criterios de ponderación contenidos en el fundamento jurídico 6 de la citada STC 38/2023, de 20 de abril97. Según se explica con mayor detalle en dicho fundamento: (i) ha de examinarse, en primer lugar, el contenido de la voluntad de la persona con discapacidad en la medida en que dicha voluntad haya podido manifestarse; (ii) la decisión adoptada ha de responder, en todo caso, al fin estricto de proteger a la persona con discapacidad, sin que puedan perseguirse intereses distintos, de terceros o públicos; (iii) la consiguiente ponderación de los beneficios y perjuicios ha de adecuarse a dicho fin, de modo que el criterio adoptado ha de ser proporcionado a las necesidades de la persona con discapacidad, de acuerdo con las circunstancias concurrentes.
En aplicación a este caso concreto, la decisión adoptada por la autoridad judicial, favorable a la vacunación, no desbordó los límites de cobertura del precepto habilitante (art. 9.6 de la Ley 41/2002). En el Auto del Juzgado se valora exclusivamente los beneficios y desventajas que la administración de la vacuna puede reportar a la madre, sin basar su decisión en factores distintos a la mayor protección de la salud de esta. En la misma línea, el auto de apelación declara que «la única perspectiva a ponderar en el caso es la individual del paciente, es decir la identificación de la mayor protección y del mejor beneficio para la salud del residente, debiendo quedar al margen cualquier otra consideración». De este modo, la finalidad legítima (tuitiva) que caracteriza la norma de cobertura es plenamente respetada.
El TC termina señalando que los criterios de ponderación empleados en las resoluciones judiciales responden inequívocamente a la finalidad legítima expuesta, en cuanto persiguen proteger, del mejor modo posible, los intereses de la persona vulnerable. Sintéticamente expuestos, esos criterios, claramente enunciados en ambas resoluciones, son los siguientes: (i) la fiabilidad asociada a la aprobación de la concreta vacuna por la Agencia Europea del Medicamento y la Agencia Española del Medicamento y Productos Sanitarios y su sometimiento a seguimiento permanente; (ii) la asimilación general de los márgenes de riesgo asociados a dicha vacuna a los habituales en cualquier otra vacuna recomendada por las autoridades sanitarias; (iii) la existencia de un contexto de riesgo para la salud, tanto por razón de su avanzada edad y consiguiente mayor vulnerabilidad frente al virus, como por razón de convivir con dos personas que desarrollan su actividad laboral en el exterior y pueden, por ello, contagiarla, en base al informe forense, que fue clave en las resoluciones judiciales previas, concluyendo que los peligros para la salud de la anciana derivados del contagio son, en principio, mayores que los inherentes a la vacunación. Tiene en cuenta, en este punto, que «reside con sus dos hijos, los cuales desempeñan una actividad laboral y tienen contacto, por tanto, con terceras personas, tal y como aquellos relataron en la vista, lo que supone un riesgo de contagio para ellos y, en consecuencia, para su madre». También valora que la anciana «sale al exterior en alguna ocasión, para ir a la peluquería […] y recibe visitas de familiares, lo que incide asimismo en ese riesgo de contagio»; (iv) la existencia de un informe pericial forense sometido a contradicción que acreditaba la inexistencia de contraindicaciones específicas; (v) la evidencia estadística, reflejada por los datos oficiales y avalada por la pericial practicada, según la cual, no existiendo contraindicación particular para la anciana, es mayor y más grave el riesgo de contraer la infección por coronavirus que la de padecer algún efecto secundario grave como consecuencia de la vacuna.
Puede concluirse, por todo ello, que las resoluciones judiciales impugnadas se atuvieron a los límites de habilitación legalmente previstos y realizaron una ponderación adecuada del interés de la persona vulnerable y proporcionada a sus necesidades de acuerdo con las circunstancias concurrentes, por lo que no lesionaron el derecho fundamental a la integridad personal (art. 15 CE).
Con esta doctrina, ¿pueden las autoridades sanitarias provocar la imposición judicial de la vacunación del menor?
Fuera de casos puntuales de indicación pediátrica, una vez comprobada la efectividad de la estrategia española de no obligatoriedad en sentido estricto, creemos que la cuestión debe transitar por la posibilidad de que las vacunas sean meramente condicionantes para la realización de algunas actividades (por ejemplo, la admisión o entrada en centros educativos) a las que el menor puede tener derecho en virtud de su interés superior.
Recordemos que la Sentencia del Tribunal Europeo de Derechos Humanos de 8 de abril de 2021, pronunciada tras el recurso planteado por padres de niños rechazados por guarderías en República Checa por no estar vacunados es un ejemplo de ello. Esta sentencia ha terminado avalando la vacunación infantil condicionante de admisión en guarderías en virtud del principio de “solidaridad social”, así como su "necesidad en una sociedad democrática.
Como se ha señalado certeramente98, Sanidad puede instarles a vacunar; pero parece que, de momento, no imponiendo coactivamente o forzosamente la vacuna -lo cual solo sería posible tras la intervención judicial en casos de riesgo grave para la salud y la vida del menor (ex art. 9 de la Ley 41/2002), o tras una autorización basada en el riesgo grave para la salud pública basada en los art. 8 y ss. LJCA)-, sino supeditando la admisión y derecho de entrada en centros educativos o de ocio a la vacunación previa (vacunación condicionante).
Ello plantea el problema -que el ejemplo checo y nuestros antecedentes jurisprudenciales en la misma materia no resuelven- de la privación del derecho del menor a la educación en una etapa de enseñanza obligatoria. Esto es, si aplicando los criterios de la doctrina constitucional sobre la necesidad de una ponderación adecuada del interés del menor y proporcionada a sus necesidades de acuerdo al entorno y las circunstancias concurrentes, respetando los límites del derecho de información y consentimiento, podría entenderse legítima la imposición judicial de vacunación a un menor. Entendemos a este respecto:
a) Que la afectación del derecho fundamental a la educación reconocido en el art. 27 CE, exige la intervención judicial en los términos de los artículos 8 y ss. LJCA (que establece distintas modalidades dependiendo de que la medida sea de alcance general o afectante a sujetos determinados).
b) Y que la inadmisión del menor en el centro donde cursa una etapa de enseñanza solo sería autorizable cuando, en una ponderación de derechos, se garantice la equidad en la posibilidad de acceso tanto a la vacuna, como a los recursos educativos perdidos (v. gr. mediante enseñanza online). Por otra parte, esa imposibilidad de acceso a los recursos educativos presenciales (incluso a los de ocio y deporte extraescolar) sí podrá dar lugar, en su caso, a la declaración de riesgo del menor; y ello porque la misma provoca la pérdida de la socialización necesaria en la etapa de escolarización presencial propia de la etapa de educación obligatoria (a partir de seis años), que, sin integrar el núcleo esencial del derecho a la educación (cubierto por la enseñanza online), si conforma el interés superior del menor.
A esta conclusión parece adecuarse la última doctrina constitucional en materia de vacunación al hacer extrapolable la doctrina sentada en la STC 38/2023 sobre la incidencia de la vacunación en el derecho a la integridad física referida a personas con discapacidad, y extender el canon de constitucionalidad aplicable a los menores de edad. La STC 148/2023, de 6-11 (tratándose el caso de una menor de 11 años en un supuesto de discrepancia entre los progenitores respecto a la inoculación) da una respuesta muy fundada para avalar la autorización judicial a la representación de un padre para la vacunación de la menor, basada en su superior interés, y las concretas circunstancias de la época pandémica y los datos científicos sobre la afectación a la salud mental de los menores y adolescentes. Creemos que estos fundamentos pueden resultar muy útiles y, con los matices pertinentes, hacerse extensivos a otras vacunas.
| El TC utiliza el canon de constitucionalidad basado en el interés superior del menor y la ponderación de las circunstancias concurrentes y personales de los menores para validar la autorización judicial que otorga la representación para el acto médico de la vacunación a uno de los padres, aunque este no tuviera la patria potestad, o en caso de ser esta compartida, al progenitor favorable a la vacunación |
La STC examina si las decisiones judiciales de autorizar al padre para realizar las gestiones necesarias para la vacunación de la hija común estaban orientadas a la consecución de una finalidad constitucionalmente legítima y cumplieron con el canon de motivación reforzada exigible para la adopción de una medida limitativa del derecho a la integridad física (art. 15 CE).
a) Del contenido de las resoluciones judiciales impugnadas se desprende que la decisión de autorizar la vacunación tuvo como fundamento primero y esencial la protección del interés superior de la propia menor en sus dos vertientes fundamentales: protección de la salud física individual frente a una eventual infección por Covid-19; y protección de la salud mental mediante la preservación de sus relaciones interpersonales en el entorno social, familiar y escolar, finalidades ambas plenamente legítimas desde el punto de vista constitucional.
b) En relación con la salud individual de la menor, las resoluciones judiciales previas se apoyan en un informe emitido por el CAV-AEP y la Sociedad Española de Infectología Pediátrica, donde se advertía que se habían identificado casos graves de infección por COVID-19 en niños sin factores de riesgo, como el síndrome inflamatorio multisistémico pediátrico, y también casos de COVID-19 persistente; en las recomendaciones de la AEMPS, el CISNS, la AEP y el Centro para el Control y la Prevención de Enfermedades. Todos estos documentos favorecen la vacunación en el segmento de edad de los cinco a los once años, pues los riesgos o probabilidad de complicaciones de salud por administrar la vacuna eran muy reducidos y los beneficios indudables (reducción del riesgo de contraer la enfermedad, así como del riesgo de sufrir complicaciones a corto y largo plazo), de modo que la ponderación riesgos/beneficios de la vacunación para la salud de los menores se inclinaba claramente a favor de estos últimos, no existiendo constancia de que la menor implicada en este caso sufriera enfermedad o alergia previas que pudieran hacer que la vacunación resultara contraindicada.
c) En relación con la protección de la salud mental de la menor –mediante la preservación de sus relaciones interpersonales en el entorno familiar, social y escolar– la resolución judicial dictada en primera instancia, confirmada en apelación, argumentó que era preciso considerar los efectos colaterales que la pandemia había tenido en los niños y adolescentes; entre los que se encontraba la falta de normalidad en la escolarización y los trastornos de salud mental, que se habían evidenciado como consecuencia de la pandemia.
Los efectos colaterales adversos de la pandemia de la covid sobre la salud mental de niños, niñas y adolescentes han quedado igualmente constatados a través de los estudios e informes emitidos por organismos oficiales acreditados. En un estudio publicado el 2 de marzo de 2022, «Salud mental y COVID-19: datos iniciales sobre las repercusiones de la pandemia», la Organización Mundial de la Salud indicaba que se había registrado un aumento significativo de los problemas de salud mental en la población general en el primer año de la pandemia, notificándose a menudo como factores de riesgo el hecho de tener menor edad, ser del sexo femenino y presentar afecciones de salud preexistentes. UNICEF, en su informe «Estado mundial de la infancia 2021: En mi mente. Promover, proteger y cuidar la salud mental de la infancia», publicado en octubre de 2021, alertó de que las tasas de depresión y ansiedad generalizadas y clínicamente significativas se habían duplicado en el transcurso de la pandemia, siendo las tasas más altas de ansiedad y depresión entre las niñas, e indicaba que estos hallazgos podían deberse, entre otros factores, al aislamiento social en un grupo de edad que depende enormemente de la socialización con los pares.
Partiendo de estos datos, resulta más que justificado considerar que, siendo las personas menores de edad vector de contagio del virus SARS-CoV-2, su vacunación habría de facilitar el retorno a la normalidad en sus relaciones con otras personas de su entorno familiar extenso, escolar y social (pares), mientras que la ausencia de vacunación podría favorecer una prolongación, siquiera parcial, del aislamiento social de la menor, con las consecuencias negativas derivadas de ello.
En definitiva, las resoluciones judiciales impugnadas justificaron la decisión de autorizar la vacunación de la menor en la realización efectiva de su interés superior, concretado en este caso en la preservación de su salud física y mental, que, conforme a los estudios, informes y recomendaciones de los organismos oficiales autorizados en materia de vigilancia de la salud, resultaba tutelado de un modo más efectivo y eficaz mediante la inoculación de la vacuna frente a la COVID-19.
Es por ello que se debe declarar su conformidad con el derecho fundamental a la integridad física y moral de la hija menor de edad de la demandante de amparo (art. 15 CE).
Para terminar, incluso la STC 5/2024, de 15 de enero, ha valorado la importancia de las circunstancias concretas de un menor (de 13 años) que, frente a la oposición de uno de los progenitores, mostró su interés en la vacunación. La juez apreció madurez en la menor durante la exploración judicial, cuando manifestó "que quería ponerse la vacuna para estar a salvo y, si llegara a contagiarse, «estar más segura y no sufrir tanto»; añadió que lo había hablado con ambos progenitores y que conocía las razones de cada uno al respecto, así como su intención de ir a estudiar a Inglaterra y que se sentía más segura si se contagiaba allí estando vacunada”.
__________
90 GONZALEZ CARRASCO, M. La prestación del consentimiento informado en materia de salud en el nuevo sistema de apoyos al ejercicio de la capacidad. Derecho Privado y Constitución, 2021, 39, 213-47.
91 Un análisis de los problemas interpretativos en la actuación profesional en el caso de menores (particularmente adolescentes) con una discapacidad mental, en GARRIDO CUENCA N. Seguridad de pacientes y salud mental en la infancia y la adolescencia: apuntes desde el derecho sanitario para una revisión del consentimiento informado, los tratamientos involuntarios y la respuesta a las conductas autolíticas. Revista Derecho y Salud, Volumen 33. Extraordinario - 2023.
92 Estos Autos de suspensión han sido también reincidentes, con la jurisprudencia constitucional consolidada y los precedentes (323/2023, de 19 junio, 181/2023, de 17 abril): ATC 325/2023, de 19 de junio, RTC 2023\325; http://icaoviedo.es/res/comun/biblioteca/2353/Jdo%20Primera%20Instancia%2016%20Granada%204%20feb%202021.pdf
93 https://www.iberley.es/jurisprudencia/auto-civil-n-60-2021-jpi-santiago-compostela- sec-6-rec-32-2021-20-01-2021-48145076
94 https://www.poderjudicial.es/cgpj/es/Poder-Judicial/Noticias-Judiciales/Un-juez-de-Sevilla-autoriza-vacunar-contra-el-Covid-19-a-una-usuaria-de-86-anos-de-una-residencia-de-mayores-tras-la-negativa-de-su-hijo
95 https://elpais.com/sociedad/2021-02-25/la-fiscalia-del-supremo-censura-la-vacunacion-forzosa.html
96 https://hj.tribunalconstitucional.es/HJ/es/Resolucion/Show/29125
97 Vid tb en este sentido STC (Sala Primera) Tribunal Constitucional (Sala Primera) 74/2023 de 19 junio. RTC 2023\74
98 CARRASCO GONZALEZ C, MORENO ALEMÁN J., “Vacunación contra el Covid 19 en menores. La capacidad decisoria en distintos escenarios”, en CESCO, Novedades, diciembre 2021.
4. Renuncia a la vacunación
4.1. ¿Deben firmar algún documento los padres o tutores que se nieguen a vacunar a sus hijos?
4.2. ¿Puede un menor de edad negarse a la vacunación?
4.1. ¿Deben firmar algún documento los padres o tutores que se nieguen a vacunar a sus hijos?
| Si los padres se niegan a firmar la renuncia a la vacunación de los hijos, debe anotarse en la historia clínica |
En todos aquellos casos en los que haya una negativa de padres o tutores a vacunar a sus hijos o representados, antes de cualquier consideración jurídica, deben extremarse las medidas de información sobre los riesgos y beneficios de la vacunación y sobre los riesgos de la no vacunación, sin considerar que dicha negativa es definitiva, manteniendo siempre abierta la relación del médico con los padres o tutores para facilitar, en su caso, la reconsideración del rechazo de las vacunas y su posterior aceptación.
El documento “Criterios de Evaluación para Fundamentar Modificaciones en el Programa de Vacunación en España” señala a este respecto que: “desde el punto de vista de salud pública, y tras haber suministrado la información adecuada, se considera recomendable documentar el rechazo o negativa a la vacunación sistemática o a la administración de alguna vacuna en particular. Esto deberá quedar reflejado en la historia clínica o registro de vacunación, pudiendo recogerse la negativa firmada del interesado o sus responsables si se considera pertinente”.
Así pues, la negativa de padres o tutores a vacunar a sus hijos o representados es conveniente que quede reflejada, al menos, en la historia clínica, con indicación de que dicha negativa se mantiene pese a haber sido informados tanto del riesgo/beneficio de la vacunación, como de los riesgos de la no vacunación.
Al margen de la constancia en la historia clínica, es recomendable que las negativas a la vacunación se hagan constar en registros, que deben mantenerse debidamente actualizados, pues de lo contrario, se corre el riesgo de que si posteriormente los padres o tutores cambian de opinión y autorizan la vacunación, en caso de una reacción adversa, esa persona constará en el registro como que en una fecha se negó a vacunarse y posteriormente se vacunó. En este caso, el elemento clave sería acreditar si hubo información suficiente sobre los posibles riesgos de la vacuna: el hecho de que inicialmente rechazase la vacuna y después la aceptase, es un indicio de que hubo información y, en base a ella, se rechazó la vacuna, aceptándola después; en este sentido podemos citar la Sentencia del Tribunal Superior de Justicia de Castilla y león, de 21 junio de 2010, en la que se afirma que: "D.ª Trinidad supo de los peligros de la intervención y; en un primer momento, rehusó su práctica por razones humanamente comprensibles; pero posteriormente, por sí o por consejo bienintencionado volvió sobre su idea y deseó someterse a esa operación peligrosa … Tal diferencia en el tiempo y la duplicación de las pruebas, unida a la falta de explicación alternativa coherente de los hechos, llevan sólo a una conclusión posible: D.ª Trinidad fue informada de los riesgos de la operación verbalmente al menos por la Administración sanitaria y no deseó, por los riesgos que comportaba, someterse a ella, pero luego, pese a esos riesgos, aceptó llevar a cabo la intervención”.
Al margen de hacer constar en la historia clínica y en registros la negativa de los padres a la vacunación, es conveniente desde el punto de vista legal que los padres o tutores sean invitados a firmar un documento de renuncia a la vacunación99, en el que, como mínimo deben constar:
- Datos identificativos del menor, de los padres o tutores y del profesional sanitario
- Información relativa al carácter voluntario de las vacunas y a su recomendación por las autoridades sanitarias, a través del calendario vacunal, por la protección individual y de grupo que las mismas dispensan
- Declaración de los padres o tutores de haber recibido información sobre los riesgos y beneficios de las vacunas, sobre el riesgo a que exponen a sus hijos o representados, asumiendo la responsabilidad de esa decisión
- Relación de vacunas recomendadas y aceptación o negativa sobre cada una de ellas
- Firmas de padres o tutores, del profesional sanitario y fecha del documento
La mayoría de las iniciativas en este sentido son de naturaleza privada, no obstante lo cual resultan evidentes las ventajas que desde el punto de vista legal supone la firma de este documento; ahora bien, no debe obviarse el hecho de que los padres o tutores pueden negarse a la firma del mismo, en cuyo caso debe hacerse constar dicha circunstancia en la historia clínica, sin tratar de forzar la firma, con el fin de mantener abierta la vía de diálogo del profesional con los padres, para facilitar, en un momento posterior, un cambio de criterio con autorización de la vacunación inicialmente rechazada.
__________
99 El Comité Asesor de Vacunas de la Asociación Española de Pediatría: "Rechazo de la vacunación: documento de declaración de responsabilidad de los padres", en el que hay una propuesta de hoja de declaración de renuncia a la vacunación y la Academia Americana de Pediatría también tiene este documento. Documenting Parental Refusal to Have Their Children Vaccinated.
4.2. ¿Puede un menor de edad negarse a la vacunación?
Tal y como se expuso en el apartado 2.4, el menor, a partir de los 12 años, atendidas sus condiciones de madurez a criterio del facultativo, puede legalmente manifestar su negativa a ser vacunado, sin que resulte de aplicación a estos efectos el art. 9.6 LAP y sin que se pueda llevar a cabo la vacunación del menor en contra del criterio de éste y de sus padres o representantes legales, salvo que en el menor concurran circunstancias de riesgo específicas.
También habría que tener en cuenta, a estos efectos, el dictamen que la Fiscalía del Tribunal Supremo emitió el 24 de febrero de 2021 en contra de las vacunaciones forzosas contra la COVID-19 en residencias de ancianos, afirmando que “en tanto que la ley no establezca obligación de vacunarse, no cabe invocar razones genéricas de salud pública o específicamente basadas en la especial vulnerabilidad de determinados grupos de personas para justificar la administración forzosa de la vacuna”.
A partir de los 16 años, el menor alcanza la mayoría de edad sanitaria y puede prestar su consentimiento o rechazar la vacunación, con las previsiones vistas en el apartado 2.4: si el facultativo considera que la negativa del menor a la vacunación supone un grave riesgo, los padres serán informados y su opinión será tenida en cuenta. En este supuesto es recomendable que la negativa del menor a vacunarse se recoja en un documento firmado —al menos— por el menor, en el que se refleje el proceso de información, tanto al menor como a los padres o tutores, con indicación de las consecuencias que para el menor puede tener esa negativa a la vacunación.
4.3. En el caso de personas que se niegan a vacunarse (o que rechazan la vacunación de sus hijos o representados), ¿pueden recaer en algún tipo de responsabilidad legal si enferman?
| No hay sanción prevista para el que se niega a vacunar, porque la vacunación es voluntaria |
No hay en nuestro sistema precedentes de que la Administración, en lo que se refiere al Derecho Sancionador —vía administrativa o penal— haya exigido responsabilidades a los padres o tutores que se negaron a la vacunación de los hijos o representados que, posteriormente, enfermaron, porque la participación en las actuaciones de salud pública es voluntaria en nuestro Derecho (artículo 5.2 Ley 33/2011, General de Salud Pública), de modo que, acreditado el daño y el nexo entre la negativa a la vacunación y el desarrollo de la enfermedad (por ejemplo en el caso de la difteria del niño de Olot), faltaría el hecho ilícito, al ser la vacunación voluntaria en nuestro Derecho, salvo los casos previstos en es la Ley Orgánica 3/1986, de 14 de abril, de Medidas especiales en materia de salud pública.
Es cierto que hay alguna propuesta favorable a la retirada de la patria potestad a los padres que se nieguen a vacunar a los hijos, entendiendo que no admitir las vacunas recomendadas supondría un ejercicio incorrecto de la patria potestad. Las alternativas que se plantean son las siguientes: “una es obligar a vacunar, lo cual es complicado; otra es educar y volver reforzar las campañas de las ventajas de las vacunas, que ya se está haciendo porque aquí hay muchos mitos y una tercera en la que se está trabajando que consiste es incentivar a los padres con ayudas económicas, que pueden ser en especie” 100.
4.4. ¿Podrían los hijos reclamar a sus padres por la vida enferma derivada de la negativa de éstos a la vacunación?
Se trata de las acciones relacionadas con la vida enferma que deben soportar los hijos a causa de la voluntad de sus padres contraria a la vacunación, lo que les privó de la oportunidad de vacunarse y evitar la enfermedad que posteriormente contrajeron. Podría encuadrarse en las denominadas acciones de wrongful life, de los hijos frente a sus progenitores, sobre las que no hay precedentes en nuestro Derecho.
La prosperabilidad de una y otra posible acción de exigencia de responsabilidad sería muy limitada, en la medida en que la Administración al no imponer con carácter obligatorio la vacunación en general, no puede exigir responsabilidades por incumplimiento de meras recomendaciones, como tampoco pueden responder los padres o tutores por negarse a una vacunación que no tenía carácter obligatorio.
A raíz del caso de Olot, es posible plantearse una posible tercera acción de reclamación, la de los padres contra los grupos contrarios a la vacunación que, al parecer, según manifestaciones de los padres, informaron de forma errónea sobre los riesgos de la vacunación. Tampoco consta ningún precedente en nuestro Derecho.
En conclusión, el carácter voluntario de la vacunación en nuestro Derecho limita el posible ejercicio de responsabilidades a los que rechazaron una vacunación que carece de la nota de obligatoriedad, salvo en los casos previstos en la Ley Orgánica 3/1986. En cambio, en países donde la vacunación es obligatoria, casos de Italia y Francia, sí hay precedentes de reclamaciones de la Administración contra los padres que rechazan la vacunación, siendo los pronunciamientos judiciales y constitucionales favorables a la constitucionalidad de la medida ablativa en materia de vacunación, por la protección individual y por la protección del grupo.
A continuación se expone una tabla con las posibles situaciones en relación con el consentimiento de los menores de edad y sus padres (tabla 46.3)
Tabla 46.3. Tabla de posibles situaciones en relación con el consentimiento de los menores de edad y sus padres.
| Padres | Hijos de 12 a 16 años | Protocolo |
| Conviven. Patria potestad conjunta sin medidas de guardia y custodia. A favor de vacunar | A favor de vacunar | Acto sanitario ordinario Basta que lo acompañe uno de los progenitores. Información efectos secundarios frecuentes Profesionales y servicio sanitario: terceros de buena fe |
| Ambos en contra de vacunar | A favor de vacunar Escala móvil: Puede consentir sólo si es capaz de comprender Criterio mixto: consiente el menor y los padres por su deber de velar por el Codecisión |
Decisiones contra el interés del menor: poner en conocimiento de autoridad judicial: expediente de jurisdicción voluntaria |
| Ambos a favor de vacunar | En contra de vacunar | No se le puede imponer |
| No conviven. Uno de ellos ostenta guarda y custodia | ||
| - Ambos en contra de vacunar | En contra de vacunar | No se le puede imponer |
| - El custodio en contra de vacunar y el no custodio a favor | A favor de vacunar Podría consentir si es capaz de comprender, pero la patria potestad en acto sanitario ordinario es del conviviente |
Si acude acompañado de un progenitor y el menor consiente. Profesionales y servicio sanitario: terceros de buena fe Si se detecta el conflicto: poner en conocimiento de autoridad judicial: expediente de jurisdicción voluntaria |
| - El custodio a favor de vacunar, el no custodio en contra | A favor de vacunar. Decide el custodio | Se puede llevar a cabo la vacunación, si bien el no custodio puede acudir a la vía judicial, vía de jurisdicción voluntaria |
| - El custodio a favor de vacunar, el no custodio en contra | En contra de vacunar | No se le puede imponer |
| No conviven. Guarda y custodia compartida. Desacuerdo en la vacunación | No se opone a la vacunación | Acudir a la vía judicial, vía de jurisdicción voluntaria |
| En cualquiera de las circunstancias | Mayor de 16 años, salvo casos de grave riesgo, decide por sí mismo | Se le puede vacunar |
__________
100 https://www.elmundo.es/espana/2019/01/22/5c460f2dfc6c837e1a8b4750.html
5. Prescripción médica obligatoria de las vacunas por denominación comercial
5.1. ¿Quiénes pueden prescribir medicamentos sujetos a prescripción médica?
5.2. Las vacunas está sujetas a prescripción médica obligatoria
5.3. La receta médica como instrumento de prescripción
5.4. Las vacunas deben prescribirse obligatoriamente por denominación comercial
5.5. ¿Es necesaria una receta para cada dosis, o se pueden prescribir varias dosis en una misma receta?
5.1. ¿Quiénes pueden prescribir medicamentos sujetos a prescripción médica?
| Las vacunas no financiadas precisan de receta médica normalizada, ya sea oficial o privada |
El artículo 6.2.a) de la Ley 44/2003, de 21 de noviembre, de ordenación de las profesiones sanitarias (en adelante LOPS) establece que corresponde a los médicos la indicación y realización de las actividades dirigidas a la promoción y mantenimiento de la salud, a la prevención de las enfermedades y al diagnóstico, tratamiento, terapéutica y rehabilitación de los pacientes, así como al enjuiciamiento y pronóstico de los procesos objeto de atención.
Como consecuencia de ello el artículo 79.1 LM atribuye en exclusiva a los médicos —podólogos y odontólogos— la facultad de recetar medicamentos sujetos a prescripción médica a través de la receta médica, pública o privada, o la orden hospitalaria de dispensación, como medio de asegurar la instauración de un tratamiento.
| Las vacunas financiadas y las campañas vacunales no precisan receta médica, prescribe la autoridad sanitaria |
Sin perjuicio de ello, el propio artículo 79 (párrafos 3 y 4) prevé que la enfermería pueda prescribir medicamentos sujetos a prescripción médica conforme a protocolos y guías de práctica clínica y asistencial. Esta facultad se desarrolla en el Real Decreto 954/2015, de 23 de octubre, por el que se regula la indicación, uso y autorización de dispensación de medicamentos y productos sanitarios de uso humano por parte de los enfermeros, modificado por el Real Decreto 1302/2018, de 22 de octubre101.
| Las vacunas financiadas y campañas vacunales son competencia de enfermería, basta con su orden de dispensación |
A continuación, analizaremos los principales requisitos que deben cumplir las enfermeras para ostentar dicha facultad en relación con los medicamentos sujetos a prescripción médica:
- ACREDITACIÓN: no se requiere acreditación ni formación complementaria para los enfermeros graduados, diplomados, ayudantes técnicos sanitarios o equivalente que acrediten una experiencia profesional mínima de un año o superen un curso de adaptación adecuado ofrecido por la Administración Sanitaria, de manera gratuita102.
El procedimiento para la acreditación de las enfermeras y enfermeros será regulado por las comunidades autónomas en el ámbito de sus competencias, en cumplimiento de lo dispuesto en la Sentencia del Tribunal Constitucional 76/2018, de 5 de julio103, al entender el TC que el establecimiento de los títulos, de las competencias y de la formación exigida para la obtención de esta capacitación profesional forma parte de la competencia estatal básica en materia de sanidad, en la medida en que tales condiciones han de ser uniformes e iguales para todos los profesionales en todo el territorio español, pero advierte de que, sin embargo, "no sucede lo mismo con el acto de comprobación del cumplimiento de tales condiciones, que tiene naturaleza ejecutiva, y forma parte de las competencias autonómicas en materia sanitaria”.
En la actualidad todas las CC. AA. han dictado sus respectivas normas para la acreditación de los enfermeros y enfermeras en relación con la indicación, uso y autorización de dispensación de medicamentos y productos sanitarios de uso humano104.
- PROTOCOLOS Y GUÍAS DE PRÁCTICA CLÍNICA: la indicación, uso y autorización de medicamentos de uso humano sujetos a prescripción médica se hará conforme a los protocolos o guías de práctica clínica y asistencial, que deberán contener necesariamente aquellos supuestos específicos en los que se precisa la valoración médica previa a la indicación enfermera, así como las actuaciones que, en el ámbito de sus respectivas competencias personal médico y de enfermería realizarán colaborativamente para garantizar la seguridad del paciente y la continuidad asistencial.
Las modificaciones introducidas en este punto son las que han generado más conflicto con la profesión médica, pues se ha sustituido la exigencia que contenía el proyecto de RD acordado de que esta facultad de enfermería se llevara a cabo en base a los protocolos o guías de práctica clínica y asistencial, validados previamente, en los que debería figurar necesariamente el diagnóstico y la prescripción médicas, por la identificación en protocolos y guías de los supuestos que se precisa valoración médica previa a la actuación enfermera.
Aunque se prevé que el proceso de aprobación de protocolos y guías clínicas va a ser lento, ya se han aprobado distintos protocolos de práctica clínica y asistencial que recopila la actuación enfermera en materia de indicación, uso y autorización de dispensación de medicamentos sujetos a prescripción médica, en este caso, en el campo de las heridas, quemados, ostomías, hipertensión, diabetes, fiebre y anticoagulación oral105. Por cierto, no sin debate y polémica, como demuestra que la OMC haya interpuesto en septiembre del 2022 un recurso administrativo entendiendo que estos protocolos invaden las competencias profesionales del médico106.
- COMPETENCIA ENFERMERA EN VACUNAS DE CALENDARIO Y CAMPAÑAS VACUNALES: salvo en aquellos casos en los que un paciente, en atención a sus condiciones particulares, precise de una valoración médica individualizada, la administración de las vacunas contempladas en el calendario vacunal y aquellas tributarias de campañas de salud que se determinen por las autoridades sanitarias, sólo precisará de la correspondiente orden de dispensación.
Se trata de una regulación novedosa que ya se apuntaba en texto acordado en octubre de 2017 y que se ha concretado más, limitándolo al ámbito de las vacunas de calendario y campañas vacunales.
Con esta medida las vacunas de calendario y las campañas vacunales quedan bajo el control de las enfermeras, salvo en el caso de pacientes que precisen de valoración médica individualizada. La razón última de esta medida se encuentra en que no se precisa prescripción médica por entenderse que la prescripción en ambos supuestos (campañas vacunales y vacunas de calendario) la hace la autoridad sanitaria, tal y como se expone con detalle en el apartado 5.2.
Además de los conflictos tradicionales en la materia, protagonizados por el colectivo médico y el de enfermería, parece que el RD 1302/2018 ha abierto conflictos con otros colectivos sanitarios:
- Por un lado los farmacéuticos: el Consejo General de Colegios de Farmacéuticos está estudiando un posible recurso contra la norma, al detectar que se ha incluido como competencia de los enfermeros en hospitales la “validación de la dispensación”, algo hasta ahora reservado para los farmacéuticos de hospital. Por otro lado, el Colegio de Farmacéuticos de Madrid ha dado orden a sus servicios jurídicos para estudiar el real decreto, con el fin de interponer un recurso contra esta norma, al entender que el experto del medicamento es el farmacéutico y que “la formación académica en Farmacología del farmacéutico consta de 825 horas y 33 créditos, frente a las 150 horas y 6 créditos de Enfermería”. La utilización de conceptos como “dispensación” y “administración” en el decreto también habrían dado la voz de alarma, que quiere mirar con lupa cada actividad de la Enfermería107.
- Por otro lado los fisioterapeutas, con la ayuda de los representantes de las enfermeras, vienen reclamando idénticas facultades de prescripción que la enfermería108.
__________
101 https://www.boe.es/buscar/act.php?id=BOE-A-2015-14028. Tras años de conflicto entre los colectivos de médicos y enfermeras en relación a esta facultad, el 24 de octubre de 2017 se había llegado a un acuerdo entre representantes de médicos y enfermeras por la prescripción de enfermería junto con el Ministerio de Sanidad. Resultado de ese consenso, el proyecto de Real Decreto de reforma del RD 954/2015 acordado venía a dar solución a los problemas que la aplicación de este último había planteado. Sin embargo, el Real Decreto 1302/2018 introdujo cambios no pactados con los representantes de los médicos que rompieron de nuevo el consenso alcanzado en octubre de 2017.
102 En el proyecto de Real Decreto acordado tan solo era necesaria acreditación específica para prescribir fármacos complejos e innovadores.
103 La Sentencia del Tribunal Constitucional de 5 de julio de 2018.
104 La información actualizada con los vínculos a todas las normas por Comunidad Autónoma en: https://www.consejogeneralenfermeria.org/profesion/prescripcion
105 Ver el listado actualizado en: https://www.consejogeneralenfermeria.org/profesion/prescripcion
106 https://www.redaccionmedica.com/secciones/medicina/las-claves-del-recurso-de-la-omc-contra-las-guias-de-prescripcion-enfermera-2956
107 https://www.diariomedico.com/farmacia/profesion/el-consejo-general-y-el-cof-de-madrid-estudian-recurrir-la-prescripcion-enfermera.html.
108 https://www.satse.es/w/satse-reclama-al-ministerio-de-sanidad-que-los-fisioterapeutas-puedan-prescribir-medicamentos
5.2. Régimen de prescripción de las vacunas como medicamento especial
De acuerdo a los artículos 8.1.d) y 45 LM, las vacunas se incluyen en la categoría de “medicamentos especiales”. Por ello, aunque estén sujetos al régimen normativo general de medicamentos, el propio precepto advierte de las “particularidades previstas en esta ley o que se establezcan reglamentariamente según su naturaleza y características de aplicación propia109.
Una de estas peculiaridades se encuentra en las modalidades de prescripción, que se recogen tanto en la propia LM como en el desarrollo reglamentario:
1.º) El art.79.1 LM habilitó al Gobierno para regular la indicación, uso y autorización de dispensación de determinados medicamentos sujetos a prescripción médica por los enfermeros, en el marco de los principios de la atención integral de salud y para la continuidad asistencial, así como en el ámbito de los cuidados tanto generales como especializados. Es la conocida como “prescripción enfermera”, que de acuerdo a este precepto tiene una sólida base legal.
2.º) Esta facultad se desarrolla en el Real Decreto 954/2015, de 23 de octubre, por el que se regula la indicación, uso y autorización de dispensación de medicamentos y productos sanitarios de uso humano por parte de los enfermeros, modificado por el Real Decreto 1302/2018, de 22 de octubre. Esta norma introduce un nuevo párrafo 3 en el artículo 3 donde se señala expresamente:
“Salvo en aquellos casos en los que un paciente, en atención a sus condiciones particulares, precise de una valoración médica individualizada, la administración de las vacunas contempladas en el calendario vacunal y aquellas tributarias de campañas de salud que se determinen por las autoridades sanitarias, sólo precisará de la correspondiente orden de dispensación.”
3.º) En la práctica, la Comisión de Salud Pública, de acuerdo a las decisiones adoptadas en la Ponencia de Vacunas del Consejo Interterritorial del SNS, así como las autoridades autonómicas competentes, han implementado las posibilidades explícitas de este régimen normativo. De modo que la Administración de las vacunas incluidas en calendario vacunal o decidida por las autoridades sanitarias competentes en materia de salud pública (como las vacunas frente al SARS CoV-2) no requieren diagnóstico ni prescripción previa. El ejemplo se encuentra en este documento de “Recomendaciones sobre vacunación gripe. Temporada 2022-2023" donde se lee explícitamente:
“ADMINISTRACIÓN DE LA VACUNA FRENTE A LA GRIPE. Esta vacunación se realiza como consecuencia de una decisión de la autoridad sanitaria en materia de salud pública, por un riesgo epidemiológico y en aras de preservar la salud colectiva y la de las personas con mayor riesgo de desarrollar complicaciones por esta enfermedad, por lo que no requiere diagnóstico ni prescripción previa. Estas recomendaciones de vacunación se formulan al amparo de lo establecido en la Ley 33/2011, de 4 de octubre, General de Salud Pública, y en la normativa de las Comunidades Autónomas en esta materia”. "La experiencia en las Comunidades Autónomas sobre la administración conjunta de vacunas frente a la gripe y a la COVID-19 fue favorable en la temporada pasada. Las publicaciones disponibles muestran que no se ha observado una diferencia en las respuestas inmunes de ambas vacunas tras su administración conjunta o por separado. Respecto al perfil de seguridad, tampoco se han observado diferencias significativas en cuanto a la reactogenicidad local y sistémica”.
4.º) El protagonismo en el proceso de toma de decisiones en materia de vacunación, en tanto competencia compartida entre Estado y Comunidades Autónomas, la tiene el Consejo Interterritorial del Sistema Nacional de Salud. El art.19.3 LGSP le encomienda la adopción de acuerdos sobre estas materias:
a) Un calendario único de vacunas en España. Las comunidades autónomas y las ciudades de Ceuta y Melilla sólo podrán modificarlo por razones epidemiológicas.
Por tanto, es el CISNS quien valora y aprueba, si procede, las propuestas elevadas por su Comisión de Salud Pública (coordinada por el DG Salud Pública del Ministerio y conformada por los Directores Generales de Salud Pública de las Comunidades Autónomas). De la Comisión depende un grupo de trabajo, la Ponencia de Programa y registro de Vacunaciones, a quien se encomienda la elaboración de propuestas de recomendaciones sobre vacunación para todo el Estado, que se aprobarán, en su caso, por la CSP. La Ponencia, coordinada por el área de Vacunas de la DGSP se conforma con representantes de las Comunidades Autónomas, el Instituto de Salud Carlos III, Ministerio del Interior, Defensa, INGESA, AEMYPS y la DGSP.
Por tanto, la implementación del procedimiento para decidir las vacunas de calendario o aquellas precisas en un determinado momento por razones de salud pública, pautas, indicaciones, etc. recae en la Administración, no en los facultativos que prescriben medicamentos por regla general. De ahí que, como ha señalado el RD 2018 solo sea necesaria la correspondiente orden de dispensación (que se rige por su normativa general) en vacunas de calendario.
Las reglas generales se encuentran en el documento “Criterios de Evaluación para Fundamentar Modificaciones en el Programa de Vacunación en España Ponencia de Programa y Registro de Vacunaciones”. En este enlace pueden leerse las Recomendaciones sobre programas vacunales específicos, campañas de vacunación y especialmente un apartado dedicado a la vacunación infantil frente al SARS-CoV-2.
Así pues, el régimen común de prescripción facultativa, regulado en el art. 45 LM (artículos 2 -párrafos 19 y 20-, 43, 44, 45, 66.2 del Real Decreto 1345/2007, en relación con los artículos 6 y concordantes de la LOPS y el art. 2 y Disposición Adicional 5 Ley 41/2002)78 debe tener en cuenta el desarrollo reglamentario.
Por tanto, no es obligatoria la prescripción médica en el caso de vacunas de calendario o las que se decidan en campañas de salud por las autoridades sanitarias. Así lo han dejado de claro las “Recomendaciones de vacunación frente a gripe y COVID-19 en la temporada 2023-2024 en España. Actualización. Aprobado por la Comisión de Salud Pública el 12 de septiembre de 2023. Elaborado por la Ponencia de Programa y Registro de Vacunaciones”.
“Esta vacunación se realiza como consecuencia de una decisión de la autoridad sanitaria en materia de salud pública, por un riesgo epidemiológico y en aras de preservar la salud colectiva y la de las personas con mayor riesgo de desarrollar complicaciones por estas enfermedades, por lo que no requieren diagnóstico ni prescripción previa”.
A sensu contrario, las vacunas que requieran una prescripción individualizada sobre un paciente determinado, o las vacunas no incluidas en alguno de los dos supuestos previstos normativamente, esto es: no financiadas ni recomendadas en calendario vacunal, sí precisan de la correspondiente prescripción médica y receta, de acuerdo con las reglas generales de prescripción y dispensación.
El resumen se refleja en la tabla 46.4.
Tabla 46.4. Situación legal de la prescripción de vacunas.
| Vacunas no financiadas | Prescripción médica obligatoria |
| Vacunas de calendario oficial | Orden de dispensación |
| Campañas vacunales | Orden de dispensación |
| Campaña vacunal ante un riesgo epidemiológico (Gripe/Covid 19) | No requiere diagnostico ni prescripción previa |
Las vacunas, como cualquier medicamento, están sometidas a un fuerte régimen de intervención pública, que se manifestará a lo largo de toda su vida útil: desde el procedimiento de autorización, los modelos de adquisición y compra, su puesta a disposición de los ciudadanos ya sea en el ámbito de la farmacia comunitaria u hospitalaria, la financiación, o el sistema de farmacovigilancia. Pero, además, en el caso de las vacunas, nos encontramos ante uno de los instrumentos más eficaces de las políticas de salud pública, sin duda la principal medida desde el punto de vista de la prevención. Desde ambas perspectivas, se plantean peculiaridades respecto al resto de medicamentos. La raíz de todas ellas es su naturaleza: son productos biológicos y su finalidad es preventiva, lo cual hace que su población diana sean casi siempre sujetos sanos. A partir de aquí se originan una serie de particularidades que convierten a las vacunas en medicamentos especiales, así caracterizadas desde el punto de vista estrictamente normativo, pero que se extienden a otras cuestiones de tipo económico o logístico que terminan imbricándose y repercutiendo en aquel. Esto es, la decisión de introducir una vacuna en el programa nacional de inmunización implicará muchos aspectos que se deben considerar al priorizar las inversiones en el sector salud. Los tiempos de pandemia que estamos viviendo nos han puesto sobre el tapete la relevancia de todas ellas y la necesidad de afrontarlas política y jurídicamente. Sintetizando las más importantes, para ponernos en contexto, señalamos:
- Producción: larga, compleja y con escaso número de productores, con especialidades en los procesos de ensayo clínico
- Seguridad y farmacovigilancia: los estándares son más exigentes que los de cualquier fármaco
- Acceso y financiación: los calendarios de vacunación y los modelos de financiación varían entre países e incluso dentro de los mismos, como es el caso de Italia o España debido a su alto grado de descentralización
- Procedimiento de toma de decisiones y autoridades implicadas, con un papel relevante del Consejo Interterritorial del SNS
Así lo declaró el Tribunal Superior de Justicia del País Vasco, en sentencia de 27 de junio de 2017, en la que se anula la Instrucción 7/2015 de 2 de mayo, del Director General del Servicio Vasco de Salud por la que exoneraba de prescripción médica las vacunas financiadas y las de campañas vacunales, afirmando que: dicha orden dejaría sin contenido a las normas que expresa e inequívocamente reconoce a estos profesionales la facultad de expedir recetas, de prescribir, de individualizar el tratamiento indicando a cada paciente la medicación que debe utilizar, eso y no otra cosa es prescribir.
Idéntica recomendación se contiene en la Orden SAN/863/2017, de 6 de octubre, por la que se dispone la vacunación de la Comunidad de Castilla y León frente a la gripe y el neumococo y la misma fue convalidada por Auto n.º 320 Tribunal Superior de Justicia Castilla y León, 24 noviembre 2017.
Esta es la línea que, finalmente se adoptó en el Real Decreto 1302/2018, de 22 de octubre, por el que se modifica el Real Decreto 954/2015, de 23 de octubre, por el que se regula la indicación, uso y autorización de dispensación de medicamentos y productos sanitarios de uso humano por parte de los enfermeros, que introduce un nuevo párrafo 3 en su artículo 3 para los casos donde no sea necesario el diagnóstico previo y la prescripción individualizada:
“Salvo en aquellos casos en los que un paciente, en atención a sus condiciones particulares, precise de una valoración médica individualizada, la administración de las vacunas contempladas en el calendario vacunal y aquellas tributarias de campañas de salud que se determinen por las autoridades sanitarias, sólo precisará de la correspondiente orden de dispensación.”
__________
109 Resulta importante señalar la peculiaridad de las vacunas como medicamento especial.
5.3. La receta médica como instrumento de prescripción
| La receta médica y la orden de dispensación se regulan en un Real Decreto de 2010 |
La materialización de la prescripción se lleva a cabo a través de la receta médica y las órdenes de dispensación hospitalaria. El artículo 79.1 LM dispone que:
“La receta médica, pública o privada, y la orden de dispensación hospitalaria son los documentos que aseguran la instauración de un tratamiento con medicamentos por instrucción de un médico, un odontólogo o un podólogo, en el ámbito de sus competencias respectivas, únicos profesionales con facultad para recetar medicamentos sujetos a prescripción médica”.
| Desde 2010, la receta médica, oficial o privada, debe ajustarse a la normativa que la regula |
El Real Decreto 1718/2010, de 17 de diciembre, sobre receta médica y órdenes de dispensación, en su artículo 1, define la receta médica:
“es el documento de carácter sanitario, normalizado y obligatorio mediante el cual los médicos, odontólogos o podólogos, legalmente facultados para ello, y en el ámbito de sus competencias respectivas, prescriben a los pacientes los medicamentos o productos sanitarios sujetos a prescripción médica, para su dispensación por un farmacéutico o bajo su supervisión, en las oficinas de farmacia y botiquines dependientes de las mismas o, conforme a lo previsto en la legislación vigente, en otros establecimientos sanitarios, unidades asistenciales o servicios farmacéuticos de estructuras de atención primaria, debidamente autorizados para la dispensación de medicamentos”.
Las recetas médicas, públicas o privadas, pueden emitirse en soporte papel, para cumplimentación manual o informatizada, y en soporte electrónico.
Si se trata de vacunas no financiadas, como indica la Disposición Adicional 3.ª del Real Decreto 1718/2010, de 17 de diciembre, sobre receta médica y órdenes de dispensación, la prescripción de medicamentos no financiados se realizará en el modelo de receta médica específico, de acuerdo con los criterios contenidos en el anexo de este real decreto, y deberán ajustarse en todo lo que les afecte, incluidos los requisitos de prescripción, a lo dispuesto en los capítulos III y IV de este real decreto.
En consecuencia, desde el año 2010, la receta médica no es válida en cualquier soporte, por tratarse de un documento sanitario normalizado y obligatorio. A estos efectos, debemos alertar sobre la no idoneidad como receta para la dispensación de vacunas en oficina de farmacia de los documentos informativos sobre vacunación que se elaboran en muchos centros de salud y consultas privadas, los mismos son útiles a título informativo, pero no son en ningún caso, recetas normalizadas que permitan acudir a la farmacia comunitaria para que las mismas sean dispensadas por el farmacéutico.
El artículo 3.2 del RD 1718/2010 establece los datos obligatorios que debe contener la receta médica: relativos al paciente, al medicamento, al prescriptor y otros datos tales como la fecha de prescripción, la fecha prevista de dispensación, etc.
La receta médica es válida en todo el territorio nacional, y garantizará que el tratamiento prescrito pueda ser dispensado al paciente en cualquier oficina de farmacia del territorio nacional, tanto en sanidad pública, como en sanidad privada (artículo 2 RD 1718/2010).
5.4. Las vacunas deben prescribirse obligatoriamente por denominación comercial
| Las vacunas deben prescribirse obligatoriamente por denominación comercial, como cualquier medicamento biológico |
Si bien se parte de un principio de libertad de prescripción, pues el ejercicio de las profesiones sanitarias se llevará a cabo con plena autonomía técnica y científica (artículo 4.7 LOPS), esta libertad está sujeta a ciertas limitaciones, ya sea por motivos sanitarios o por motivos económicos.
Limitación de la prescripción a los medicamentos financiados en el ámbito del SNS, al uso racional de los recursos disponibles, por principio activo o por marca. En la actualidad, se respeta, la libertad de prescripción por marca, con matices; pero incluso en los supuestos en los que se exige la prescripción por principio activo, es posible la prescripción por denominación comercial, “siempre y cuando se respete el principio de mayor eficiencia para el sistema y en el caso de los medicamentos considerados como no sustituibles” (artículo 87.3 LM).
La prescripción de los medicamentos biológicos, y por tanto de las vacunas, debe hacerse por denominación comercial, tal y como establece el artículo 3.2.b). 2.º del Real Decreto 1718/2010, de 17 de diciembre, sobre receta médica y órdenes de dispensación:
2. El prescriptor deberá consignar en la receta y en la hoja de información para el paciente los datos básicos obligatorios, imprescindibles para la validez de la receta médica, indicados a continuación:
b) Datos del medicamento:
2.º Denominación del medicamento si se trata de un medicamento biológico
De acuerdo con lo expuesto en este apartado y en el anterior, podemos concluir que las vacunas, como el resto de los medicamentos biológicos, están sujetas a prescripción médica obligatoria por marca, no siendo válidos como receta médica para su dispensación en oficina de farmacia los documentos informativos sobre vacunación que se elaboran en muchos centros de salud y consultas privadas.
5.5. ¿Es necesaria una receta para cada dosis o se pueden prescribir varias dosis en una misma receta?
| Seria posible prescribir varias dosis en una misma receta, respetando los plazos de validez de la receta y de duración del tratamiento |
Para dar respuesta a esta cuestión debemos tener en cuenta lo dispuesto en el Real Decreto 1718/2010, de 17 de diciembre, sobre receta médica y órdenes de dispensación, artículo 5, para las recetas oficiales del Sistema Nacional de Salud:
5. Criterios de prescripción, validez de la receta y duración del tratamiento (tabla 46.5).
a) Criterios de prescripción:
1.º En cada receta médica en soporte papel se podrá prescribir un solo medicamento y un único envase del mismo, con las excepciones previstas en los apartados 2.º y 5.º
2.º En el caso de los medicamentos que se relacionan, sólo podrá prescribirse un medicamento y hasta cuatro envases por receta:
i. Presentaciones en unidosis y por vía parenteral del grupo terapéutico J01 «Antibacterianos para uso sistémico», a excepción de los subgrupos J01E, J01M y J01R.
En el caso de presentaciones orales deberá tenerse en cuenta que se podrán prescribir hasta dos envases siempre que tengan la misma Denominación Común Internacional (DCI), dosis, forma farmacéutica y formato.
ii. Viales multidosis (excepto cartuchos multidosis) del grupo terapéutico A10A «Insulinas y análogos».
iii. Medicamentos que contengan sustancias estupefacientes incluidas en la lista I de la Convención Única de 1961 de estupefacientes, de acuerdo con la normativa específica de aplicación.
iv. Medicamentos de diagnóstico hospitalario. (…)
b) Validez de la receta:
En cada receta médica oficial en soporte papel se consignará obligatoriamente la fecha de prescripción (…).
La receta médica oficial en soporte papel es válida para una dispensación por la oficina de farmacia con un plazo máximo de diez días naturales a partir de la fecha de prescripción o, cuando conste, de la fecha prevista por el prescriptor para su dispensación. Una vez transcurrido este plazo, no podrán solicitarse ni dispensarse medicamentos ni productos sanitarios con su presentación. (…)
Por las especiales características de las vacunas individualizadas antialérgicas y vacunas individualizadas bacterianas, el plazo de validez de estas recetas será de un máximo de noventa días naturales a partir de la fecha consignada. Asimismo, el plazo de validez de la receta médica oficial podrá ser inferior a los diez días establecidos, en el caso de medicamentos sometidos a disposiciones específicas por el Ministerio de Sanidad.
c) Duración del tratamiento:
1.º Con carácter general, el plazo máximo de duración del tratamiento que puede ser prescrito en una receta es de tres meses. La Dirección General de Farmacia y Productos Sanitarios del Ministerio de Sanidad, Política Social e Igualdad, mediante resolución, podrá establecer un plazo distinto para las presentaciones de medicamentos autorizados en unidosis cuyo embalaje exterior coincida con su acondicionamiento primario. (…)
De acuerdo con ello, en principio, sería posible la prescripción en una sola receta médica de varias dosis de una misma vacuna, siempre que se cumplan los criterios temporales de validez de la receta: 10 días desde la fecha de prescripción o, cuando conste, de la fecha prevista por el prescriptor para su dispensación y de duración del tratamiento: 3 meses.
Tabla 46.5. Criterios de prescripción, validez de la receta y duración del tratamiento.
| Prescripción | 1 medicamento y 1 envase por receta, con excepciones |
| Validez | 10 días naturales desde la fecha de prescripción o desde la fecha prevista para su dispensación 90 días naturales desde la fecha consignada para vacunas individualizadas antialérgicas y vacunas individualizadas bacterianas |
| Duración del tratamiento | 3 meses máximo |
6. Atención farmacéutica: dispensación y sustitución de medicamentos.
| El farmacéutico juega un papel esencial en la vacunación |
6.1. Sustituibilidad de la prescripción médica por el farmacéutico
6.2. La prescripción médica de la vacuna no es sustituible por el farmacéutico
La prestación farmacéutica en oficina de farmacia es una pieza esencial de la asistencia sanitaria; sus funciones esenciales son la adquisición, custodia, conservación y dispensación de medicamentos y productos sanitarios, en régimen de colaboración con el SNS, para garantizar el acceso de los ciudadanos a los medicamentos en todo el territorio nacional. Integran la atención farmacéutica, fundamentalmente:
1) La indicación farmacéutica: a demanda del paciente, debiendo el farmacéutico discriminar en qué caso procede recomendar remedios para la dolencia del paciente y en qué caso debe derivarlo al médico, la dispensación de medicamentos.
2) El seguimiento de la medicación: en colaboración con el paciente y el resto de los profesionales sanitarios, identificando, previniendo y resolviendo los problemas relacionados con el tratamiento.
3) La dispensación de medicamentos: dando al paciente los consejos necesarios para que el paciente pueda usar adecuadamente los medicamentos prescritos. El artículo 86.1 dispone que: “En las oficinas de farmacia, los farmacéuticos, como responsables de la dispensación de medicamentos a los ciudadanos, velarán por el cumplimiento de las pautas establecidas por el médico responsable del paciente en la prescripción…” Además, los farmacéuticos cooperarán con el prescriptor en el seguimiento del tratamiento a través de los procedimientos de atención farmacéutica, contribuyendo a asegurar su eficacia y seguridad. Igualmente, los farmacéuticos participarán en la utilización racional de los medicamentos, en particular a través de la dispensación informada al paciente.
| El farmacéutico no puede dispensar vacunas sin receta médica, que debe contener la denominación comercial |
No será posible la dispensación de medicamentos sujetos a prescripción médica obligatoria si el paciente no presenta la correspondiente receta en documento normalizado y obligatorio, así lo establece el artículo 79.2 LM: “El farmacéutico dispensará con receta aquellos medicamentos que la requieran. Dicho requisito deberá especificarse expresamente en el embalaje del medicamento.”
El incumplimiento de este deber es constitutivo de infracción administrativa grave en materia de medicamentos (artículo 111 LM), con multas que van desde los 30 001 a los 90 000 €, en tres grados: mínimo, medio y máximo. Validez y deber de conservación de la receta.
El Real Decreto 1718/2010 establece en su artículo 5.5. b) que la receta oficial del SNS en soporte papel es válida para una dispensación por la oficina de farmacia con un plazo máximo de diez días naturales a partir de la fecha de prescripción o, cuando conste, de la fecha prevista por el prescriptor para su dispensación. Sin embargo, “por las especiales características de las vacunas individualizadas antialérgicas y vacunas individualizadas bacterianas, el plazo de validez de estas recetas será de un máximo de noventa días naturales a partir de la fecha consignada”. y en el c) Duración del tratamiento: Con carácter general, el plazo máximo de duración del tratamiento que puede ser prescrito en una receta es de tres meses. El artículo 18.3 RD 1718/2010, establece que: “Una vez dispensadas y diligenciadas, las recetas médicas en soporte papel serán conservadas en la oficina de farmacia durante tres meses”.
6.1. Sustituibilidad de la prescripción médica por el farmacéutico
| El farmacéutico no puede sustituir la vacuna indicada por el médico sin su autorización |
El artículo 89.1 de la Ley del Medicamento, comienza indicando que el farmacéutico dispensará el medicamento prescrito por el médico, si bien nuestra normativa contempla la posibilidad de sustitución por parte del farmacéutico el medicamento prescrito por el médico, en los términos y condiciones previstas por la legislación110.
Sin embargo, el farmacéutico carece de facultad de sustitución en relación con los medicamentos biológicos, en general, y con las vacunas, en particular, tal y como se expone a continuación.
__________
110 El artículo 15.1, párrafo segundo, del Real Decreto 1718/2010 dispone que: “El farmacéutico dispensará el medicamento prescrito. En el caso de tener que proceder a su sustitución, tendrá en cuenta los criterios legales vigentes, informando al paciente sobre la sustitución efectuada. En los casos de sustitución, el farmacéutico responsable de la dispensación consignará en la receta el medicamento que dispensa, la fecha y su firma y el motivo de la sustitución”. La sustitución por el farmacéutico de la prescripción médica es posible en los siguientes supuestos:
- Desabastecimiento o urgencia (artículo 89.2 Ley del Medicamento): cuando no se disponga en la farmacia del medicamento prescrito o concurran razones de urgente necesidad en su dispensación, el farmacéutico podrá sustituirlo por el de menor precio, que deberá tener igual composición, forma farmacéutica, vía de administración y dosificación.
- Fijación de precios (artículo 89.5 Ley del Medicamento): si el medicamento prescrito por denominación comercial tiene un precio superior al precio menor de su agrupación homogénea, el farmacéutico sustituirá el medicamento prescrito por el de precio más bajo de su agrupación homogénea y, en caso de igualdad, dispensará el medicamento genérico.
6.2. La prescripción médica de la vacuna no es sustituible por el farmacéutico
En el caso de los medicamentos biosimilares, se respetarán las normas vigentes según regulación específica en materia de sustitución e intercambiabilidad (artículo 89.5, párrafo segundo, LM).
El artículo 89.4 LM establece que:
“Quedarán exceptuados de esta posibilidad de sustitución aquellos medicamentos que, por razón de sus características de biodisponibilidad y estrecho rango terapéutico, determine el Ministerio de Sanidad, Servicios Sociales e Igualdad”.
El citado precepto fue desarrollado por la Orden SCO 2874/2008, de 28 de septiembre, por la que se establecen los medicamentos que constituyen excepción a la posible sustitución por el farmacéutico con arreglo al artículo 86.4 de la Ley 29/2006, de 26 de julio, de garantías y uso racional de los medicamentos y productos sanitarios —léase 89.4 LM—, que establece en su Artículo único. Medicamentos no sustituibles:
1. De acuerdo con lo dispuesto en el artículo 86.4 de la Ley 29/2006 de 26 de julio, de garantías y uso racional de los medicamentos y productos sanitarios —léase 89.4 Ley del Medicamento—, no podrán sustituirse en el acto de dispensación sin la autorización expresa del médico prescriptor los siguientes medicamentos: a) Los medicamentos biológicos (insulinas, hemoderivados, vacunas, medicamentos biotecnológicos)…
2. La Agencia Española de Medicamentos y Productos Sanitarios elaborará un listado de medicamentos no sustituibles, que será de acceso público.
En cumplimiento de ello, la AEMPS publicó el 24 de abril de 2009 (y viene actualizando periódicamente, siendo la más reciente del 31 octubre de 2023111) la nota informativa de medicamentos que no deben ser objeto de sustitución por otros medicamentos con el mismo principio activo sin la autorización expresa del médico prescriptor112.
__________
111 Nota informativa de medicamentos no sustituibles
112 Dicha modificación no está exenta de polémica y ha generado descontento en las sociedades científicas, al entender que atenta contra la facultad de prescripción del médico en favor del criterio que se pueda fijar en el ámbito hospitalario en comisiones interdisciplinarias.
7. Administración de vacunas por el personal de enfermería
| La administración de las vacunas por la enfermería se hará conforme a la presripción de la autoridad sanitaria (financiadas) o del médico (no financiadas) |
La LOPS (artículos 6, 7 y 9.3) establece que en el trabajo en equipo priman los principios de coordinación y colaboración, conjugándose la idoneidad técnica o capacidad real con la no exclusividad, de acuerdo con las competencias y los conocimientos de cada profesión en función de su formación universitaria, evitando monopolios competenciales, sin perjuicio de la competencia esencial de cada profesión y la diferencia con las restantes profesiones.
Conforme al artículo 79 LM —ya visto—:
“La receta médica, pública o privada, y la orden de dispensación hospitalaria son los documentos que aseguran la instauración de un tratamiento con medicamentos por instrucción de un médico, un odontólogo o un podólogo, en el ámbito de sus competencias respectivas, únicos profesionales con facultad para recetar medicamentos sujetos a prescripción médica”.
De lo expuesto se deriva que la receta médica no sólo implica la obligación del farmacéutico de dispensar el medicamento prescrito, sino que obliga a todos los profesionales sanitarios que integran los equipos, en función de sus respectivas competencias, correspondiendo al profesional de enfermería la obligación de administrar la vacuna prescrita por el médico, como medio de garantizar la instauración del tratamiento prescrito.
Al igual que la administración de vacunas la deben llevar a cabo los profesionales sanitarios habilitados y autorizados para ello, la misma debe hacerse en centros sanitarios preparados para dar respuesta a eventuales reacciones adversas, debiendo evitarse la administración de vacunas en domicilios y otros lugares no idóneos al efecto.
En síntesis, podemos esquematizar todo lo expuesto en la siguiente tabla 46.6:
Tabla 46.6. Asignación de tareas de vacunación a profesionales sanitarios.
| TAREA | QUIÉN | CÓMO | CALENDARIO |
| Prescripción | Médico | Por denominación comercial | No·financiadas |
| Autoridad sanitaria | Aprobación de calendario oficial | Vacunas de calendario y campañas vacunales | |
| Indicación, uso y autorización | Enfermería | Orden de dispensación | |
| Dispensación | Farmacéutico | La vacuna indicada en la receta, por denominación comercial | No·financiadas |
| Centro de vacunación autorizado | Orden de dispensación | Vacunas de calendario y campañas vacunales | |
| Administración | Enfermería | Conforme a las advertencias del prescriptor, velando porque se administra la vacuna prescrita, en centro autorizado | Financiadas / No·financiadas |
8. RESPONSABILIDAD PATRIMONIAL DE LA ADMINISTRACIÓN
8.1. ¿Cuál es la responsabilidad de la Administración sanitaria en relación con las vacunas?
8.1. ¿CUÁL ES LA RESPONSABILIDAD DE LA ADMINISTRACIÓN SANITARIA EN RELACIÓN CON LAS VACUNAS?
La responsabilidad patrimonial de la Administración por los daños que cause a los particulares en el ejercicio de su actividad se consagra, con carácter general, en el art. 106 de la Constitución y se desarrolla en los arts. 32 y siguientes de la Ley 40/2015, de 1 de octubre, del régimen jurídico del sector público, donde se establece que:
“Los particulares tendrán derecho a ser indemnizados por las Administraciones Públicas correspondientes, de toda lesión que sufran en cualquiera de sus bienes y derechos, siempre que la lesión sea consecuencia del funcionamiento normal o anormal de los servicios públicos salvo en los casos de fuerza mayor o de daños que el particular tenga el deber jurídico de soportar de acuerdo con la Ley.”
La actividad de la vacunación es un excelente banco de ensayo para reflexionar sobre la responsabilidad patrimonial, que en este ámbito puede analizarse desde dos perspectivas complementarias, con sus propias manifestaciones en materia de responsabilidad:
- Por un lado, la del propio acto médico-sanitario que supone el acto de la vacunación, como modalidad de asistencia sanitaria y como prestación farmacéutica especial
- Por otro, como manifestación de la principal política preventiva en el ámbito de la salud pública
No hay demasiada jurisprudencia específica, seguramente porque el perfil de seguridad de las vacunas es muy alto y no se producen demasiados acontecimientos adversos, salvo las reacciones leves propias al acto de inmunización. Tampoco es significativa la jurisprudencia que haya hecho aplicación de la responsabilidad por productos defectuosos, ya consolidada en casos de acontecimientos adversos en materia de medicamentos o productos sanitarios en general. Sin embargo, alguna de esta doctrina jurisprudencial se ha intentado extrapolar a otros ámbitos de la responsabilidad sanitaria, manifestando la tensión del debate dogmático sobre el abandono progresivo de la responsabilidad patrimonial objetiva.
La responsabilidad de la Administración sanitaria, en lo que a la vacunación se refiere trae causa113, fundamentalmente, de dos situaciones:
- Por un lado, las reacciones adversas que provocan las vacunas sistemáticas incluidas en el calendario vacunal, donde la Administración —a título de ejemplo—, fue declarada responsable por el síncope vasovagal con traumatismo cráneo encefálico que sufrió un alumno de 18 años tras la administración de una vacuna en un centro escolar; en otro caso por la reacción adversa que sufrió un niño de 15 meses por la vacuna triple vírica; por la amputación de una pierna a una niña de 9 años tras sufrir una sepsis meningocócica en una campaña de vacunación frente a meningitis meningocócica destinada a individuos de 2 a 5 años de edad y, finalmente, por el fallecimiento de una menor de 13 años tras haber administrado dos dosis de la vacuna del VPH.
En cambio, no se observa responsabilidad de la Administración por la autorización e inclusión de vacunas en el calendario infantil al no quedar acreditado que el conservante tiomersal sea la causa del autismo que sufrían los niños cuyos padres reclamaron; tampoco hay responsabilidad por la eosinofilia tras la administración de tres dosis de la vacuna del VPH, ni por los daños que pueda ocasionar un producto defectuoso (Ala Octa), si el mismo está autorizado por la AEMPS y la prescripción, indicación y administración se ajustó a la lex artis ad hoc.
- Por otro lado, por las omisiones o limitaciones de determinadas vacunas en el calendario vacunal, donde la Administración —a título de ejemplo— fue condenada por la muerte de una niña a causa de una neumonía neumocócica sin estar vacunada por no ser una vacuna incluida en el calendario sistemático; y en otro caso por el cáncer de cuello de útero que sufrió una mujer que no se vacunó por estar fuera del intervalo de edad fijado en el calendario vacunal cuando esta vacuna se incluyó en el mismo.
A continuación, analizaremos, a título ilustrativo, algunas de estas sentencias de forma más detallada.
| Condena a la Administración por un cuadro vagal pospunción |
Sentencia del Tribunal Superior de Justicia de Castilla y León, Sala de lo Contencioso-Administrativo, Secc. 3.ª, de 5 de abril de 2010: reacciones adversas de la vacuna.
Se analiza el caso de un alumno de 18 años que, tras la administración de la vacuna contra la meningitis meningocócica A+C en un centro escolar, sufrió en los 10 minutos posteriores, cuando se encontraba solo, sin vigilancia médica, un cuadro vasovagal o reacción anafiláctica con traumatismo craneoencefálico provocándole lesiones.
Acreditado el nexo de causalidad entre la actuación sanitaria y el referido episodio, entiende la Sala que: “… se debe concluir que en la administración de la vacuna al actor en el centro educativo de Puebla de Sanabria se incidió en un factor conocido de riesgo de que se produjese un síncope vasovagal, o una reacción anafiláctica sin que se haya acreditado que se hayan adoptado por la Administración sanitaria las medidas preventivas correspondientes. Se recuerda que el alumno, D. Simón, tras ser vacunado, permaneció uno o dos minutos en la Sala de vacunaciones sin que conste que recibiesen ninguna indicación concreta sobre las prevenciones a tener en cuenta, máxime dadas sus circunstancias especiales de antecedentes de labilidad emocional a la sangre, y a continuación se dirigió a su aula donde fue encontrado solo, sin vigilancia médica, por sus compañeros recostado sobre su banca y mareado aproximadamente a los 10 minutos de haber sido vacunado” … “En consecuencia el daño sufrido por el actor debe ser calificado como antijurídico pues no existe deber de que el mismo sea soportado por aquél”, siendo condenada la Administración a indemnizar al perjudicado por importe de 19·329,49 €.
| Condena a la Administración por falta de información del riesgo de encefalitis tras inocular la vacuna triple vírica |
Sentencia del Tribunal Superior de Justicia de Castilla y León, Sala de lo Contencioso-Administrativo, Secc. 3.ª, de 2 de enero de 2012: reacciones adversas de la vacuna.
Se analiza el caso de un niño de 15 meses de edad, con desarrollo, normal que tras la inoculación en el Ambulatorio de la vacuna triple vírica (sarampión, rubeola y parotiditis) presentó un cuadro de encefalitis y tetraparesia espástica, en probable relación con el virus del sarampión.
La vacuna no estaba contraindicada por el hecho de que el niño días antes hubiera tenido amigdalitis y fiebre y que el día de la vacuna presentara “discreta rinorrea, apirético, BEG”, siendo banal el cuadro previo en relación con la reacción adversa que presento posteriormente.
Aunque los padres consintieron la vacunación de la triple vírica, “no fueron informados ni advertidos del, aunque muy excepcional, posible riesgo de encefalitis secuente a su administración: no consta ningún consentimiento por escrito en tal sentido, ni obra referencia alguna en la historia clínica, omisión que los miembros del Grup Medic de Reflexio sobre les Vacunes consideraron que se venía dando con habitualidad”. El riesgo de encefalitis tras inoculación de triple vírica está descrito en la literatura, es muy raro por excepcional (1/millón de dosis) y grave por la importancia e irreversibilidad de las secuelas. Es preciso informar, si no de todos los riesgos, si de los señaladamente graves, por más que sea un riesgo atípico por infrecuente.
La falta de información supone una pérdida de oportunidad para el paciente de sustraerse a la acción médica.
Si el calendario de vacunación es obligatorio: el perjudicado ha sufrido un daño antijurídico, que no tiene el deber de soportar (Sentencia del Tribunal Superior de Justicia de Valencia 18/12/2010), pese a tener su origen en un acto lícito de la Administración. “Por lo que si bien la obligación de vacunación constituye una carga del ciudadano de asumir los efectos adversos derivados de la administración de vacunas que sean calificados como leves o moderados, el principio de evitar que unos ciudadanos sean de peor condición que otros, impone que cuando la consecuencia dañosa suponga perjuicios graves y permanentes, ésta debe ser indemnizada por la comunidad, representada por la Administración, porque de otro modo se produciría un sacrificio individual a favor de la salud colectiva de la sociedad, perjudicando su integridad personal sin obtener el debido reconocimiento al derecho a la máxima protección en nuestro ordenamiento constitucional, como es el derecho a la vida y a la integridad personal”. En términos similares: Sentencia del Tribunal Superior de Justicia de Asturias de 26 de abril de 2006 y Sentencia del Tribunal Superior de Justicia de Castilla y León, Sala de Burgos, de 7 de octubre de 2003
Si el calendario de vacunación es voluntario, la demanda debe estimarse por falta de información. Analiza el Decreto 116/1993 de 27 de mayo de Castilla y León “los niños residentes en Castilla y León deberán recibir, antes de los 2 años…” (conducta cuasiobligatoria en el sentir general de la población) que se centra en la información sobre las ventajas, pero omite los riesgos, y singularmente los de mayor gravedad, por lo que “sí hubo violación del derecho a los recurrentes a optar por rechazar sin más la vacunación de su hijo tras la información que la Administración sanitaria debió suministrarles”
Dada la gravedad de las secuelas, se aplica la doctrina del daño desproporcionado, por lo que se invierte la carga de la prueba, siendo la Administración la que debe probar que no hay nexo de causalidad entre la vacunación y las secuelas, lo que no se ha conseguido, por ello condena a la Consejería de Sanidad de Castilla y León a indemnizar en 350·000 € al perjudicado y en 120 000 € a favor de los padres por perjuicios morales y la alteración de la vida y cuidados que ha precisado su hijo.
| Condena a la Administración por solidaridad con un Guillain- Barré tras vacuna de gripe |
Sentencia del Tribunal Supremo, Sala de lo Contencioso-administrativo, de 9 de abril de 2012: reacciones adversas a la vacuna.
Se analiza el caso de un varón sano de 37 años de edad que desarrolla un cuadro de Guillain-Barré tras la inoculación de la vacuna de la gripe correspondiente a la campaña 2002-3. Afirma la Sala que, acreditado el nexo de causalidad y la corrección de la lex artis material y formal: “En otros términos, fuera en este caso el desorden neurológico del recurrente, o bien la plasmación de un riesgo propio del medicamento o una excepcional reacción autoinmune a la vacuna, lo relevante es que la sentencia EDJ 2010/242878 tuvo por acreditada la relación causal entre el Síndrome de Guillain-Barré y la previa vacunación, por lo que el supuesto se manifiesta como una carga social que el reclamante no tiene el deber jurídico de soportar de manera individual, sino que ha de ser compartida por el conjunto de la sociedad, pues así lo impone la conciencia social y la justa distribución de los muchos beneficios y los aleatorios perjuicios que dimanan de la programación de las campañas de vacunación dirigidas a toda la población, con las excepciones conocidas, y de modo especial a los distintos grupos de riesgos perfectamente caracterizados, pero de las que se beneficia en su conjunto toda la sociedad”, condena a la Generalitat de Catalunya a indemnizar con 468 699,42 € la tetraparesia flácida con limitación funcional del 85 % consecuencia del síndrome.
| No se condena si no se acredita nexo entre la vacuna de la gripe y una enfermedad extremadamente rara, sobre la que no había obligación de informar |
Sentencia de Tribunal Superior de Justicia del País Vasco, Sala de lo Contencioso-Administrativo, de 8 de octubre de 2019: reacciones adversas a vacuna, no hay nexo de causalidad y no hay que informar de riesgos extraordinarios.
La Sentencia analiza adecuadamente las pericias practicadas a su instancia y considera que ninguna fue concluyente en cuanto al nexo causal entre la vacuna y el síndrome y coinciden en que se trata de una enfermedad extraordinariamente rara.
La mera relación temporal entre la vacunación y el síndrome, tampoco puede, por si sola y al contrario de lo que parece pretender el perito de la parte actora, demostrar causalidad alguna.
Respecto del vínculo entre vacunaciones y síndrome que recoge la OMS y esgrime la apelante es destacable que en el relato de esta última no se vincula con la vacuna de la gripe que le fue inoculada al contrario del detalle que se observa en la Sentencia y que induce a considerar que no hay nexo causal consistente entre ambas.
También es razonable la valoración que sobre el consentimiento realiza la Sentencia y es que, no se olvide, nos hallamos ante una simple vacuna contra la gripe y por lo tanto, según los arts. 4, 8 y 10 de la Ley 41/2002, de 14 de noviembre, básica reguladora de la autonomía del paciente y de derechos y obligaciones en materia de información y documentación clínica bastaría con la información verbal y si la información ha de ser la suficiente en los supuestos de consentimiento escrito -esto es, en general aquellas actuaciones que supongan riesgos de notoria y previsible repercusión negativa en el paciente- lógicamente también ha de ser la misma, como máximo, en aquellos procedimientos en los que baste el consentimiento verbal. Por lo tanto no es necesario una información agotadora, exhaustiva, de todas y cada una de las posibles consecuencias sino que ha de ser la de los riesgos probables en condiciones normales conforme a la experiencia y estado de la ciencia respecto de la intervención concreta de que se trate.
No era exigible por ello informar sobre un supuesto no solo tan excepcional sino además respecto del que no está demostrada la relación causal con el tipo de vacuna que se iba a inocular a la actora
| No responde la Administración de las reacciones adversas, no acreditadas, del conservante de mercurio de algunas vacunas |
Sentencia de la Audiencia Nacional, Sala de lo Contencioso-Administrativo, de 30 de noviembre de 2011: reacciones adversas al mercurio del conservante tiomersal que contienen algunas vacunas.
Esta es una de otras muchas sentencias (hasta 52, según la base de jurisprudencia ) que se dictaron en la Audiencia Nacional entre 2011 y 2013 a causa de la supuesta intoxicación por mercurio que sufrieron los niños vacunados con vacunas de calendario oficial que tenían como conservante mercurio. Valga por todas la reseña de esta sentencia en lo referido a argumentos de las demandas y pronunciamientos judiciales, pues son sustancialmente idénticos.
Plantean los demandantes responsabilidad de la Administración por la indebida autorización y comercialización de vacunas con mercurio como conservante, por la inclusión de las mismas en el calendario vacunal obligatorio y por defectos en la función de farmacovigilancia.
Pese a considerar prescrita la acción, la AN se pronuncia sobre las cuestiones de fondo planteadas:
Principio de precaución: entiende la Sala que: “la aparición de resultados adversos no implica por sí mismo ni que se esté ante una especialidad farmacéutica defectuosa, ni que se esté ante un daño antijurídico resarcible por la Administración”. Por tanto, “la decisión de retirar un medicamento o, como en el caso de autos, que en virtud del principio de precaución se aconseje prescindir de uno de sus componentes, en este caso, el tiomersal en las vacunas, no implica per se un anómalo ejercicio de la potestad de autorización ni de sus revalidaciones”
Principio de riesgo: la Sala considera que “toda autorización se efectúa en un contexto en el que no hay plena certeza acerca de la eficacia del medicamento -se habla así de "incertidumbre científica"-, lo que llama al principio de precaución. Esto es así por cuanto toda autorización de medicamentos se basa en un juicio de ponderación riesgo/beneficio, de ahí que se hable también de riesgos en desarrollo, lo que da sentido a las potestades que se ejercitan a propósito de las revalidaciones, modificaciones, más las potestades propias de la farmacovigilancia y que pueden concluir en actos de suspensión y hasta revocación, todo presidido por la constante invocación al estado de la ciencia"
“Que con esa incertidumbre se autorice un medicamento no implica necesariamente un funcionamiento anormal de la potestad de autorización, antes bien es normal o regular pues la incertidumbre es consustancial como lo demuestra esa invocación al estado de la ciencia…”
Ausencia de nexo causal: de forma rotunda entiende la Sala que “En suma, no existe evidencia científica de que la causa y origen de la enfermedad que se documenta en la historia clínica con la que contamos sea una reacción de sensibilización a etilmercurio presente en algunas vacunas pediátricas, o que padezca o haya padecido una intoxicación por mercurio, puesto que los resultados de laboratorio no revelan niveles tóxicos.”
| Responsabilidad de la Administración por no avisar a la población de la necesidad de revacunar frente al meningococo C |
Sentencia del Tribunal Supremo, Sala de lo Contencioso-Administrativo, de 25 de junio de 2010. Omisión de vacuna por no estar incluida en al calendario vacunal.
Se analiza el caso de una niña nacida en 1987, que había sido vacunada en 1997 contra meningococo C con vacuna de polisacáridos A+C (entre 18 meses y 19 años). En el año 2000 se dispuso de una nueva vacunación anti-meningococo C con vacuna conjugada, más eficaz, para los menores de 6 años.
En abril de 2003, la niña que en ese momento tenía 16 años, sufre meningitis C con púrpura fulminante, shock severo y fallo multiorgánico, hemorragia cerebral y necrosis de ambos pies, que le fueron amputados.
En noviembre de 2003, la Consejería de Sanidad de la Junta de Comunidades de Castilla La Mancha inició una nueva campaña de vacunación anti-meningococo C con vacuna conjugada para todos los menores de 19 años que no la hubieran recibido.
Los padres de la menor interpusieron una reclamación de responsabilidad patrimonial por falta de información sobre las limitaciones de cobertura de la vacuna anti-meningitis C de polisacáridos y la no revacunación que hubiera evitado el contagio; dicha reclamación no fue resuelta y se interpuso contra la desestimación presunta recurso contencioso administrativo, que fue desestimado por el Tribunal Superior de Justicia de Castilla La Mancha, contra cuya desestimación se interpuso recurso de casación.
Entiende el Tribunal Supremo que: “Lo que es evidente es que nadie se revacuna de una enfermedad como la meningitis C, si no tiene noticia de la insuficiencia de la vacuna anterior y es aquí, en la falta de información que provoca la pérdida de oportunidad de proteger a los menores excluidos de la campaña, donde radica la dejación de funciones de la Administración que, si bien puede ser libre para adoptar la decisión de revacunar gratuitamente, no lo debe ser para rectificar informaciones incompletas que colocan a los ciudadanos en la falsa seguridad de estar protegidos frente a una enfermedad como la que nos ocupa, de suerte que, si como ocurre en el caso de la joven Natividad, el riesgo llega a materializarse, el administrado no tiene el deber de soportar el daño consistente en las lesiones provocadas por la nefasta enfermedad, debiendo la Administración, en consecuencia, responder”.
La falta de actividad de la Administración es causa de los daños moral, físico y económico de la perjudicada, que se valora en 800 000 €, ya que las lesiones, las secuelas y la incapacidad que las mismas suponen para cualquier actividad, de por vida, determinan unos gastos extraordinarios que constituyen un daño real y efectivo ya producido. En cambio, no se indemnizó a los padres porque ejercitaron la acción en nombre de su hija, no en su propio nombre y, en consecuencia, nada se puede reconocer a quien no pide para sí.
| No responde la Administración de las reacciones adversas extraordinariamente raras tras la vacunación del VPH, que no había obligación de informar |
Sentencia de la Audiencia Nacional, Sala de lo Contencioso-Administrativo, de 17 de mayo de 2017: reacciones adversas a la vacuna del Virus del Papiloma Humano (VPH), procedimiento de autorización, información sobre los riesgos, farmacovigilancia, inclusión en calendario oficial “obligatorio” y falta de consentimiento informado.
Se trata de una sentencia especialmente interesante por la cantidad de cuestiones a las que da respuesta y por la jurisprudencia que sienta sobre ellas. Las cuestiones analizadas son, sintéticamente, las siguientes:
Procedimiento de autorización de vacunas: aclara la Sala que la autorización de comercialización de las dos vacunas disponibles para el Virus del Papiloma Humano (VPH) no se hizo en España, “Tal y como corresponde a este tipo de productos, el procedimiento de autorización se lleva a cabo por la Comisión Europea a través de un procedimiento centralizado que es coordinado por la Agencia Europea de Medicamentos (EMA). En cualquier caso, el citado procedimiento de autorización siguió el cauce y tiempos establecidos legalmente para ello.” Desde su autorización por la Comisión Europea en 2006, en España se están utilizando ambas vacunas al igual que en la mayoría de los países de la Unión Europea, sin que la relación riesgo-beneficio se haya visto alterada desde entonces en la actividad de farmacovigilancia.
La inclusión de las vacunas frente al VPH en el calendario de vacunación español: fue aprobada en la Comisión de Salud Pública del SNS y ratificada por el Pleno del Consejo Interterritorial del SNS en 2007 y se revisó en 2013, concluyendo que: “su mantenimiento en el calendario vacunal sigue estando sustentada desde los análisis económicos a los que se añaden varios beneficios «no esperados» en su momento tales como la protección cruzada frente a genotipos de alto riesgo no incluidos en la vacuna, la protección comunitaria frente a algunas patologías, la duración de la protección, la efectividad contrastada en los programas masivos de vacunación y la sustancial rebaja económica en el precio de la vacuna merced a la puesta en marcha por parte del MSSSI de «Acuerdos Marco» para la adquisición centralizada. Por otra parte, y tras varias decenas de millones de dosis de vacunas administradas en todo el mundo, se mantiene inalterable su excelente perfil de seguridad no siendo obstáculo para que prosigan rigurosas actividades de vigilancia postcomercialización”
Información sobre los efectos adversos de las vacunas: “Al ser un medicamento autorizado por un procedimiento centralizado (es decir, por la Comisión Europea), España ni ningún otro país de la Unión europea pueden modificar la información contenida en ficha técnica (información para profesionales) y prospecto (información para el paciente)"
Farmacovigilancia: a criterio de la Sala, “las especialidades farmacéuticas -incluidas las vacunas- pueden presentar efectos adversos cuya manifestación efectiva -de producirse- constituye uno de los supuestos en los que la causación del daño viene determinada por la necesidad de evitar un mal mayor, debiendo el administrado soportar el riesgo de los efectos adversos que se consignan en la ficha técnica y el prospecto, y salvo que se aprecie una mala praxis en relación con la situación particular del paciente o la vigilancia y tratamiento de las posibles reacciones, lo que, en su caso, abriría las puertas a otro tipo de responsabilidades distintas a las derivadas de la autorización del medicamento”
Y es que, continúa afirmando la sentencia, “la simple notificación de un acontecimiento adverso producido tras la vacunación no implica automáticamente que el mismo sea atribuible a la vacuna” concluyendo que “a pesar de que la vacuna puede causar reacciones adversas en algunos casos, no se trata de un hecho generalizado y en la mayoría de los casos se trata de reacciones leves que remiten pocos días después de la administración de la vacuna, y que no tienen entidad suficiente para cuestionar la relación beneficio/riesgo que determinó la autorización de la vacuna y su inclusión en el calendario vacunal, en todo caso con carácter voluntario, aunque se intente fomentar por las autoridades sanitarias por los beneficios que reporta en orden a la prevención el cáncer de cérvix”.
Falta de consentimiento informado previo a la administración de la vacuna: aclara la Sala que “en materia de vacunación no se está ante un tratamiento médico o quirúrgico singular sino ante una actuación masiva que está previamente testada en cuanto a seguridad y sujeta a informes técnicos previos que lo avalan, sin perjuicio de las consecuencias de las reacciones adversas que pueden producirse y que de estar asociadas a una mala praxis pudieran ser objeto de indemnización”.
A continuación, la AN recoge la doctrina del Tribunal Supremo en relación con la vacunación:
No integra un acto de medicina satisfactiva sino curativa en la que el consentimiento informado no alcanza a aquellos riesgos que no tienen un carácter típico, siempre que tengan carácter excepcional.
En supuestos de vacunación, en todo caso voluntaria —si bien aconsejada y promovida por la Administración por los beneficios sociales que de la misma derivan—, es bastante con que en el acto de la inoculación del virus se advierta verbalmente a la persona que lo recibe de aquellas consecuencias leves que pueden presentarse y que desaparecerán en breve tiempo y se indique los medios para paliar sus efectos.
El deber de información no puede entenderse genérico o en términos de probabilidad hipotética, ni ampara la exigencia de la información excesiva y desproporcionada con las finalidades curativas o preventivas de la ciencia médica, como es la relativa a los riesgos no normales, no previsibles de acuerdo con la literatura médica, o que se basan en características específicas del individuo, que previamente podían no haberse manifestado como relevantes o susceptibles de una valoración médica.
Finalmente, la información no puede ser ilimitada o excesiva, so pena de producir el efecto contrario, atemorizante o inhibidor y que ha de ofrecerse en términos comprensibles, claros y adaptados al usuario de la asistencia.
Una vez sentado lo anterior, la eosinofilia no está prevista entre los riesgos adversos de la vacuna y tampoco ha quedado demostrado que entre las reacciones adversas notificadas dicha patología sea frecuente, por lo que la obligación de informar no comprendía dicho riesgo, que no podía ser conocido por los profesionales sanitarios que administraron la vacuna a la actora. Por todo lo expuesto, la Sala desestima la demanda de la recurrente.
En análogo sentido, se pronuncian las siguientes sentencias:
Sentencia de la Audiencia Nacional de 12 de junio de 2019 (Rec. 335/2016) -Gardasil-.
Sentencia de la Audiencia Nacional, Sala de lo Contencioso, de 10 de julio de 2019 (Rec. 484/2015).
Sentencia de la Audiencia Nacional, Sala de lo Contencioso, de 17 de julio de 2019 —Cervarix—: reacciones adversas a la vacuna del Virus del Papiloma Humano (VPH), procedimiento de autorización, información sobre los riesgos, farmacovigilancia, inclusión en calendario oficial “obligatorio” y falta de consentimiento informado.
Entiende la Sala que la prueba practicada a instancias de la parte actora no pone en evidencia la relación de causalidad entre la sintomatología que presentó la actora y la administración de la vacuna.
Pero es que además, aunque pudiera establecerse la relación causa efecto entre los padecimientos de las demandantes y la administración de las vacunas, siendo el título de imputación la infracción del deber de información y de la actividad de farmacovigilancia, cabe descartar que el daño sea objetivamente imputable a la actividad de información y farmacovigilancia desenvuelta por la Administración en tanto que:
La autorización de las vacunas Gardasil y Cervarix no puede considerarse que haya sido fruto de la precipitación, ya que el procedimiento europeo que se siguió respetó en todo momento la legislación vigente y los estándares de calidad exigibles.
La decisión de inclusión de las vacunas frente al VPH en el calendario de vacunación español fue fruto de amplios debates y jomadas de trabajo en el seno de los foros pertinentes, por lo que fue una decisión consensuada y meditada.
La información que contenían la ficha técnica y prospecto de las citadas vacunas fue lo más completa posible en todo momento, teniendo en cuenta la evidencia científica disponible. Además, el contenido de ambos documentos fue acordado mediante un procedimiento europeo coordinado, sobre el que no se pueden tomar decisiones unilaterales que lo modifiquen por parte de los Estados Miembros de la Unión Europea.
El mineralograma y el test de Melisa no son técnicas estándar dentro de la práctica clínica habitual, ni se recomienda su realización de forma protocolizada en las fuentes de información más relevantes al respecto
Las actividades de farmacovigilancia realizadas respecto al uso de estas vacunas en nuestro país han sido en todo momento las apropiadas.
Finalmente, la STJUE de 21 de junio de 2017 (asunto C-621/15), aducida en otros procesos semejantes a este, no obsta a la conclusión expuesta, pues en este caso los hechos alegados en la demanda no constituyen "indicios sólidos, concretos y concordantes" que permitan concluir que la vacuna adolece de un defecto y que existe una relación de causalidad entre dicho defecto y la enfermedad.
Por todo ello se procedió a la desestimación del recurso.
| Condena a la Administración tras administrar la segunda dosis de la vacuna del VPH, sin advertir que la primera dosis había causado reacción adversa |
Sentencia del Tribunal Superior de Justicia de Asturias, Sala de lo Contencioso-Administrativo, de 20 de febrero de 2017: condena a la Administración sanitaria por el fallecimiento de una menor de 13 años tras dos dosis de la vacuna del VPH, sin que se advirtiera reacción adversa tras la administración de la primera dosis114.
La menor tenía antecedentes de asma bronquial desde los 18 meses de vida, con medicación prescrita desde el año 2001 (broncodilatadores en cámara y corticoides orales). Tras la primera dosis de la vacuna del VPH sufre un nuevo episodio de agudización de su enfermedad. A las 12 horas de administrar la segunda dosis, sufre empeoramiento brusco que le ocasiona el fallecimiento.
Las cuestiones analizadas por la Sala son las siguientes:
Aplicación a la menor de la vacuna del virus del papiloma humano: afirma la sentencia que “dada la dolencia de la menor, y la necesidad acreditada del Programa de prevención del VPH no pueden formularse reproches a la aplicación del tratamiento de vacunación y la primera dosis, puesto que estamos ante un programa general, anclado en recomendaciones europeas y con implantación generalizada autonómica, bajo sólidos estudios que respaldan la positiva relación riesgo/beneficio, y cara a combatir la infecciones responsables del cáncer de útero y conexas”, si bien advierte la Sala que: “un panorama de aprobación oficial no relaja el deber de vigilancia por la administración sanitaria ante las reacciones adversas que puede provocar su aplicación”
Deberes de información sobre los riesgos de la vacunación: la Sala recuerda que en materia de campañas de vacunación no se está ante un tratamiento médico o quirúrgico singular sino ante una actuación masiva que está previamente testada en cuanto a seguridad y sujeta a informes técnicos previos que lo avalan, sin perjuicio de las consecuencias de las reacciones adversas que pueden producirse y que de estar asociadas a una mala praxis puedan ser objeto de indemnización. En suma, ha de estarse a lo sentado por el la STS de 9 de Octubre de 2012 (ver apartado 3.1, Capítulo 44.1 Parte 1. Voluntariedad-obligatoriedad, consentimiento y renuncia a la vacunación)
En particular la STS de 20 de Abril de 2007 ha calificado de "efectos adversos de una vacunación" o "reacciones impredecibles ", que no permiten determinar la infracción de un deber de información que se revelaría desproporcionado absolutamente y que impediría el ejercicio de la función médica de curar puesto que todo medicamento y toda actuación en el ámbito de la salud, conlleva un riesgo. Y así una información exhaustiva, detallada y con reseña de todos los riesgos inmediatos, accesorios, diferidos o serios, comportaría el condicionamiento de la elección o el rechazo de una determinada terapia ante el subjetivo temor a la materialización de sus riesgos, pese a que la vacunación por definición, no debe generar más que simples molestias totalmente conocidas por la población.
Por ello, conocedores de la campaña de vacunación y bajo el aval público de su promoción, los padres asumían los riesgos inherentes a la misma, aunque claro está, no renunciaban al tratamiento idóneo de la posible materialización de las contraindicaciones.
Nexo de causalidad entre la administración de la primera dosis y la crisis asmática sufrida por la paciente cinco días después: sobre la base del informe elaborado por el responsable del centro de Farmacovigilancia de Asturias, la Sala alcanza la convicción de que en este caso particular existía una relación de causalidad entre la primera dosis y la disnea progresiva y crisis asmática que brotó con virulencia cinco días después.
1.- Responsabilidad de la Administración por los siguientes motivos:
Se trata de un Programa preventivo incentivado por la propia administración sanitaria que nos sitúa ante una menor cuyos padres de buena fe y bajo confianza legítima la someten al mismo.
Se trata de un Programa que cuenta con la administración de una vacuna concreta, Gardasil, cuya elección ha correspondido a la administración dentro de las posibles
Se trata de una vacuna en fase de implantación, y como tal, impone no solo el cumplimiento de los deberes de Farmacovigilancia normativamente impuestos, sino una actividad de diligencia y atención y atención a sus resultados y riesgos. Especialmente cuando tiene por destinatarios al colectivo de menores de edad
De acuerdo con la bibliografía y en informe del Center for Desease Control de USA para la vacunación del HPV con Gardasil, impone especial vigilancia
Se trata de una vacuna cuya ficha técnica expone como contraindicaciones, la "Hipersensibilidad a los principios activos de los excipientes. Los individuos que desarrollen síntomas indicativos de hipersensibilidad después de recibir una dosis de Gardasil no deben recibir más dosis de Gardasil". Tal hipersensibilidad presta cobertura a las reacciones alérgicas graves frente a la administración de las dosis; incluso entre los trastornos respiratorios incluye expresamente el broncoespasmo como reacción adversa.
Se trata de una paciente que desde mediados de 2010 no consta que hubiese tenido ninguna crisis asmática merecedora de asistencia hospitalaria, de manera que la existencia de una crisis asmática grave tras la ingesta de la primera a mediados de 2012 demuestra bajo criterios lógicos, cuando menos un panorama de vinculación o riesgo entre la aplicación de la vacuna y la respuesta inmunológica de la menor.
2.- Por todo ello, la Administración fue condenada a indemnizar a los progenitores de la fallecida en 122 170,58 euros, correspondiendo 20 000 de ellos a la indemnización del daño moral derivado del dolor de los progenitores de haber propiciado de buena fe la vacunación que finalmente desembocó en la muerte de su hija.
Esta sentencia tuvo una gran repercusión social y a raíz de ella se planteó la alternativa de crear en nuestro país un programa de compensación de daños por vacunas, del que nos ocuparemos al final de este apartado.
Sentencia de 21 de junio de 2017, del TJUE, C-621/2015 sobre la relación entre la vacuna contra la hepatitis B y la esclerosis múltiple.
Dicha sentencia ha sido objeto de numerosos comentarios, según los cuales el TJUE considera que existe relación de causalidad entre la administración de una vacuna contra la hepatitis y el desarrollo de una esclerosis múltiple, pese a que la investigación médica determina lo contrario. Dichas valoraciones son erróneas, tal y como se expone en la Tribuna publicada en Diario Médico115.
La sentencia de 21 de junio de 2017, del TJUE, C-621/2015 no resuelve el fondo del asunto, ni determina si la vacuna fue o no la causa de la esclerosis. El Tribunal de Casación Francés plantea al TJUE una cuestión prejudicial (instrumento por el que los jueces de los estados miembros de la UE preguntan al TJUE cómo debe interpretarse una determinada norma comunitaria, manteniendo el juez nacional la competencia plena respecto al litigio principal).
La sentencia en nada afecta al régimen de responsabilidad de los profesionales sanitarios, pues versa sobre la directiva de productos defectuosos y el régimen de responsabilidad del productor, en este caso, del laboratorio farmacéutico.
La sentencia interpreta exclusivamente la adecuación de la normativa francesa, en materia de prueba, al derecho de la Unión; no falla sobre el asunto concreto, por lo que, en ningún caso, el TJUE considera probado, al margen de la investigación médica, que la vacuna contra la hepatitis B haya causado esclerosis múltiple.
Cuando la investigación médica no ha demostrado ni refutado la relación de causalidad entre el producto defectuoso y el daño, para garantizar el principio de efectividad de la responsabilidad del productor, el TJUE entiende que, es posible que se considere acreditado el nexo si concurren indicios sólidos concretos y concordantes, en la medida en que ello no supone una inversión de la carga de la prueba que, en todo caso, pesa sobre el perjudicado/demandante.
El TJUE, en cambio, entiende que no es acorde al derecho de la Unión Europea considerar probada la existencia de una relación de causalidad entre una vacuna y el daño en base a meros indicios fácticos predeterminados de causalidad, en la medida en que ello supondría invertir la carga de la prueba.
La sentencia comentada vincula al Tribunal de Casación Francés en materia de prueba, pero es ese mismo Tribunal de Casación Francés el que, en última instancia, deberá resolver el fondo del asunto en los próximos meses.
| Fallecimiento de menor tras inoculación de la segunda dosis de la vacuna Varivax. Relación causal no determinada y correcta aplicación de la lex artis ad hoc, bastando el consentimiento verbal a la información sobre los efectos leves de la vacuna |
Sentencia del Tribunal Superior de Justicia de Castilla-León 114/2024, de 8 de febrero (Rec. 995/2021, - ECLI:ES:TSJCL:2024:547).
La sentencia desestima la pretensión de responsabilidad patrimonial que la madre intentaba ligar como nexo causal al fallecimiento del menor, que se produce por parada cardiorrespiratoria al día siguiente de la inoculación. Los argumentos del Tribunal, tras una exhaustiva prueba pericial, se centran en tres cuestiones:
1.ª) Sobre la pretendida falta de información sobre los posibles efectos adversos, prospecto de la vacuna y protocolos de actuación en caso de sospecha de acontecimientos adversos. El Tribunal entiende acreditado que la enfermera sí informó a los padres, verbalmente, de los efectos (reacciones) adversos típicos --o más frecuentes-- derivados de la administración de la vacuna, como la fiebre; como también de cómo proceder en estos casos y en la propia historia clínica, con ocasión de la administración de la segunda dosis, se hace constar expresamente " información reacciones adversas". De esta forma se cumplió con la normativa: tanto en lo que se refiere a que la información se suministrase verbalmente (cfr. arts. 8 de la Ley estatal, como en lo concerniente al contenido y extensión de lo informado, por cuanto se les trasladó lo que constaba en la ficha técnica como muy frecuente, sin que por lo demás se manifestara (o se acreditara después) que cuando se le administró la vacuna (recordar, además, que se trataba de la segunda dosis) al menor éste presentaba algún síntoma que hiciera sospechar de la existencia de algún problema que aconsejara una valoración previa más detallada de su estado de salud. De hecho, tanto el informe de la inspección médica como los peritos, al tratar estos extremos, no pusieron objeción alguna al proceder de la enfermera en este caso, explicando las razones por las que en actos como el examinado no era necesaria la intervención del facultativo pediatra.
2.ª) - Sobre la infracción de la lex artis ad hoc. El Tribunal responde a los reproches fundamentales de la demandante:
A/ En relación con la pretendida defectuosa administración de la vacuna, no se admite, puesto que la vacunación es un acto sencillo, y no consta desde luego que el menor desarrollase un bulto, hemorragia u otro resultado que pudiera ser indicativo de una mala administración. El informe de la inspección médica es claro también al excluir la existencia de indicios en la historia clínica que pudieran sugerir esa mala praxis en la administración de la vacuna.
B/ En relación con la pretendida falta de protocolo a la hora de inocular la vacuna, o la pretendida falta de seguimiento por el pediatra de las recomendaciones de la asociación de pediatría, la sentencia entiende que en relación con el supuesto protocolo o test que debería haber hecho el pediatra, la perito de la codemandada, tanto en su informe como en el acto de la vista, fue clara a la hora de desmentir este punto, con referencias aquí a lo indicado en el Manual de Vacunaciones (hoy Manual de Inmunizaciones) elaborado por el Comité Asesor de Vacunas de la AEP. Y que, además, el pediatra comunicó la sospecha de reacción adversa a la vacuna, con resultado de muerte, a la AEMPS, por venir obligado a ello; pero sin que desde luego pueda identificarse, sin más, en dicha comunicación una suerte de indicio o confirmación de que la muerte se produjo precisamente por ese acontecimiento.
C/ En relación con la pretendida falta de revisión de la historia clínica, el informe de la inspección médica es claro al indicar que no se aprecia conducta inadecuada en el mecanismo asistencial del SACYL, ni del pediatra ni de la enfermera; que éstos disponían de la historia clínica del niño y la cumplimentaron tras la asistencia prestada las veces que acudió el niño a la consulta y no existía ninguna causa que contraindicara la vacunación.
3.ª) Relación de causalidad y pérdida de oportunidad. Tampoco se estima esta alegación, pues el informe definitivo de la autopsia de los médicos forenses señaló que no se había podido establecer que el fallecimiento “tuviera una etiología médico legal violenta de tipo accidental relacionada con la administración de la vacuna". A partir de aquí, la Sala entiende que la incertidumbre que pueda existir sobre el motivo o causa determinante del fallecimiento del menor no puede llevarnos a afirmar, como por la recurrente se pretende, que la causa del fallecimiento se debe --a un efecto adverso-- a la administración de la segunda dosis de la vacuna. Y menos que este juicio de probabilidad (realmente, posibilidad) se construya, fundamentalmente, en atención al dato temporal o cronológico de que el fallecimiento del menor tuvo lugar horas después de la administración de la segunda dosis. Los peritos intervinientes y documental médica obrante en autos identificaron como la más probable la parada cardíaca secundaria a una alteración del ritmo cardíaco, bien relacionada con la genopatía SNTA1, bien con otra de carácter no conocido o investigado, o de los criterios de las OMS (en particular el relativo a la inexistencia de casos conocidos de muerte por la vacuna en niños sanos; y no sufrir este ninguna enfermedad o tratamiento que produjera inmunodepresión.
| Los daños vacunales deben ser indemnizados a través de fondos públicos, nacionales o europeos, según el regulador que apruebe la vacuna |
Compensación de daños vacunales a través de fondos estatales
Se trata de un modelo implantado en 19 países, la mayoría de ellos europeos, pero el más completo es el programa "National Vaccine injury Compensation Program", operativo desde 1988.
Las “Razones para un programa de compensación de daños por acontecimientos adversos relacionados con las vacunas en España” son las siguientes116:
Necesidad de recuperar el mercado de vacunas estableciendo un reparto de riesgos entre laboratorios y fondos estatales. Las presiones económicas y políticas derivadas de la preocupación por la seguridad de algunas vacunas.
La necesidad de aumentar la confianza de la población. Evitar o disminuir la conflictividad judicial.
Los principios éticos de equidad y justicia, que imponen compensar el sacrificio individual que puede suponer un efecto no deseado de la vacunación frente al beneficio social para la colectividad que conllevan los programas de inmunización, de acuerdo con la lógica de la solidaridad
Sin embargo, se plantean dudas en relación con esta propuesta117:
1) Las vacunas presentan diferencias sustanciales con otros medicamentos: se aplican a sujetos sanos y los programas de vacunación son medidas de salud pública que persiguen, en última instancia, el beneficio de la colectividad y no sólo el individual. Este fondo podría producir agravios comparativos frente a otras medidas sanitarias que también deben ser sufragadas por la colectividad en base a la solidaridad (p. ej. Medicamentos huérfanos, tratamientos innovadores en enfermedades como la Hepatitis C). Es preciso un exhaustivo análisis de costes sobre su conveniencia y efectividad y la comparación con otros retos que deberá afrontar nuestro sistema sanitario.
2) La dotación de este programa podría suscitar dudas en la población que, mayoritariamente, no desconfía de la seguridad de las vacunas (coberturas vacunales cercanas al 96 %).
3) El fondo se aleja de los presupuestos de la responsabilidad patrimonial: el nexo causal se presupone y los requisitos condicionantes de la responsabilidad no son determinantes para obtener una indemnización. Nuestro sistema de responsabilidad patrimonial, sin ser perfecto, ha hecho efectivo el principio de solidaridad para hacer frente a reacciones adversas de vacunas como la gripe o triple vírica, siendo generosa la jurisprudencia también en los casos de defectos de información o en el propio diseño de campañas de vacunación.
4) No está claro que este fondo evitara la conflictividad judicial.
5) Estos sistemas compensatorios se han instaurado, en su mayoría, en países con sistemas de vacunación obligatoria, donde parece que “tiene más sentido para equilibrar una medida coercitiva de tal calado, siendo cuestionable que un modelo de recomendación pueda generar una específica partida presupuestaria para compensar decisiones que definitivamente son voluntarias”118 .
| Ni los servicios de salud, ni los profesionales sanitarios responden de los daños causados por productos defectuosos (caso Ala Octa) |
Sentencia del Tribunal Supremo, Sala de lo Contencioso-Administrativo, Secc. 5.ª, núm. 1806/2021, de 21 de diciembre: el prestador -público o privado- del servicio no responde del producto sanitario defectuoso, si está debidamente autorizado119.
Aunque estas sentencias no se refieren propiamente a vacunas, su doctrina es aplicable a la responsabilidad patrimonial y profesional que pudiera derivar de los efectos adversos de las mismas.
El Servicio Cántabro de Salud no responde por las lesiones causadas a un paciente (pérdida total de visión en un ojo) como consecuencia de la utilización de un producto sanitario defectuoso (Ala Octa, gas tóxico de uso quirúrgico) autorizado por la AEMPS. El Tribunal Supremo:
Rechaza la infracción de la lex artis por culpa in vigilando (al Servicio autonómico no le es exigible un control complementario sobre el realizado por el controlador estatal).
Rechaza la aplicación del artículo 148 TRLCU a las intervenciones quirúrgicas, aunque el daño provenga de la utilización de un producto defectuoso.
Rechaza el criterio de la responsabilidad por riesgo en el ámbito de la asistencia sanitaria.
Considera que la responsabilidad corresponde al fabricante del producto defectuoso, cuando está identificado, rechazando que pueda extenderse al centro sanitario que lo adquiere, prescribe o aplica.
Afirma que la responsabilidad debe recaer en el productor individual o juntamente, en su caso, con la Administración con competencias para autorizar y vigilar los medicamentos y productos sanitarios, de concurrir las concretas circunstancias necesarias para ello.
Entiende la Sala del TS que: “la Administración sanitaria —cuyos facultativos realizan correcta y adecuadamente una intervención quirúrgica de conformidad con la lex artis— no debe responder de las lesiones causadas a un paciente como consecuencia de la utilización de un producto sanitario defectuoso, cuya toxicidad se descubre y alerta con posterioridad a su utilización, autorizada por la Agencia Española de Medicamentos y Productos Sanitarios, debiendo la responsabilidad recaer en el productor o, en su caso, en la Administración con competencias para autorizar y vigilar los medicamentos y productos sanitarios, de concurrir las concretas circunstancias necesarias para ello”.
Por una parte, niega la existencia de una responsabilidad por riesgo en el ámbito de la asistencia sanitaria.
Y por otra, entiende que no existe título de imputación basado en la infracción de la lex artis, y, por lo tanto, la Administración sanitaria no responde, cuando la causa de los daños se concreta en la utilización de un producto sanitario defectuoso cuya toxicidad es alertada por la autoridad de control (AEMPS) con posterioridad a su aplicación en una intervención quirúrgica.
Ahora bien: aunque la responsabilidad de los profesionales sanitarios no es objetiva, la del establecimiento sanitario por los daños causados por fallos organizativos o funcionales del servicio se establece (al menos, teóricamente) con este carácter en el art. 148 TRLCU (RDLeg. 1/2007). El problema más importante consiste en determinar si deben responder esta forma por los daños derivados del carácter defectuoso de los productos que adquieren para ser utilizados en el ámbito de la asistencia sanitaria.
Por lo que la STS fija una doctrina según la cual la responsabilidad objetiva por los daños producidos por los medicamentos o productos sanitarios defectuosos no se extiende a quienes, de forma pública o privada, los adquieren, prescriben o aplican, lo que constituye un elemento de tranquilidad en relación con la responsabilidad legal relacionada con el uso de las vacunas.
Justamente esta es la doctrina que ya está sirviendo de base para que los órganos consultivos rechacen la existencia de responsabilidad patrimonial por administración de vacuna Covid, en concreto la vacuna Astrazeneca, si esta ha producido alguno de los efectos adversos más típicos, aunque bastante infrecuentes, de miocarditis. Es lo que se constata en DICTAMEN del Pleno de la Comisión Jurídica Asesora de la Comunidad de Madrid aprobado por unanimidad en su sesión de 26 de enero de 2023, en sentido desestimatorio de la responsabilidad patrimonial de la Administración Madrileña120.
Interesante también resulta el DICTAMEN 74/2022 del Consejo Consultivo de Castilla-León, de 17 de marzo de 2022121, más completo, que encaja los argumentos que deben basar la existencia de responsabilidad patrimonial, recoge el caso de un fisioterapeuta de 39 años que reclamaba a la Junta de Castilla y León el abono de 7500 euros por la pérdida de ingresos que le produjo tener cerrado su negocio por una baja médica, jalonada con ingresos hospitalarios, que achaca a efectos secundarios de la primera dosis de la vacuna AstraZeneca. Termina emitiéndose informe desestimatorio, en base a los siguientes motivos:
1.º) Inexistencia de responsabilidad concurrente de las Administraciones Públicas (art.33.1 Ley 40/2015): “en la medida en la que no deriva de fórmulas conjuntas de actuación más o menos formalizadas, sino que pudiera hallarse en la cláusula residual del artículo 33.2, que contempla otros supuestos, distintos del anterior, de concurrencia de varias Administraciones, en los que la responsabilidad se fija para cada Administración atendiendo a los criterios de competencia, interés público tutelado e intensidad de la intervención, por lo que en principio habrá que exigir la responsabilidad individualmente a cada una de las Administraciones Públicas concurrentes en función de su participación en el hecho lesivo; y solo en el caso de que no sea posible la determinación de su participación, se podrá exigir la responsabilidad de forma solidaria como vía para facilitar el resarcimiento del daño”.
2.º) Título de imputación de la responsabilidad patrimonial. En relación con el acto de administración de la vacuna, hay que tener en cuenta que la lesión puede derivar del acto de vacunación mismo o del propio producto, bien porque sea defectuoso o provoque efectos adversos no advertidos. La propuesta de resolución admite que la Administración Autonómica pueda eventualmente responder desde el parámetro de la lex artis, del acto sanitario de vacunación en sí mismo o del diagnóstico y tratamiento de la miocarditis padecida por el reclamante, pero, por el contrario, niega el segundo título de imputación, con fundamento en que la Administración Autonómica no es la competente para la autorización y control de la vacuna administrada. En aplicación de la doctrina “Ala Octa”, señala el dictamen que la vacuna administrada al reclamante se ajustó a los criterios acordados en la Estrategia de vacunación vigente en el momento en que la recibió, donde no se reconocen contraindicaciones de esta vacuna, que aparecen posteriormente. Para concluir que “al carecer de competencia para la autorización, homologación y control de los medicamentos y productos sanitarios y, en particular, de la vacuna en cuestión, no procede atribuir a la Administración Autonómica la responsabilidad fundada en este título”.
3.º) Relación de causalidad entre la asistencia sanitaria prestada y la lesión. Partiendo de la carga de la prueba que corresponde al demandante, aun en aplicación de la doctrina jurisprudencial de la facilidad probatoria que podría llegar a invertir la carga de la prueba, En este caso, el reclamante no ha acreditado, ni tan siquiera alegado, una actuación sanitaria contraria a la lex artis en el acto mismo de inyección de la vacuna o en el diagnóstico y tratamiento de la miocarditis padecida, por lo que no procede tampoco derivar responsabilidad por esta causa. Tampoco, de acuerdo con la cláusula de progreso recogida actualmente en el artículo 34.1 de la Ley 40/2015, cabe exigir a la Administración, en el ámbito de la salud pública, sino la aplicación de los medios posibles en función del estado de la ciencia en el momento en que aquella presta sus servicios, puesto que, en todo caso, esta prestación es de medios y no de resultado. La Administración sanitaria no está obligada, como es natural, a obtener un resultado siempre positivo, pues entender otra cosa supondría aceptar un principio de aseguramiento universal, que convertiría a la Administración en una especie de aseguradora de todas las enfermedades, independientemente de la prestación de todos los medios que pone a su alcance la ciencia en cada momento. Y en aquel momento no existía evidencia científica contrastable para no inocular la vacuna que causó la miocarditis.
4.º) Se preocupa además el Dictamen de corroborar la diligente actuación administrativa: “Por último, procede indicar que del informe de alta hospitalaria de 26 de marzo de 2021 se extrae una actuación administrativa diligente, acomodada al estándar de funcionamiento de los servicios públicos, cuando indica que “Ante la sospecha clínica, se ha realizado RMN cardiaca que confirma diagnóstico de miocarditis aguda. Pese a que en revisión de literatura científica específica de la vacuna contra SARS-COVID 19 de AstraZeneca no nos consta que pueda provocar dicho cuadro, ante la coincidencia temporal con primera dosis de la misma se efectúa notificación al sistema de farmacovigilancia español como posible efecto adverso. (…) Dada la posible relación causal con vacunación COVID 19, se recomienda no continuar con siguiente dosis”.
En definitiva, de acuerdo con las consideraciones anteriores, cabe concluir que no se aprecia en este caso la concurrencia de los presupuestos exigidos por la ley para declarar la responsabilidad patrimonial del servicio autonómico de salud.
Todas las sentencias de este apartado se pueden consultar en: https://www.poderjudicial.es/search/indexAN.jsp#.
Figura 46.1. Resumen de la responsabilidad patrimonial por reacción adversa a la vacunación.
*Los conceptos indemnizables del sistema de vacunación voluntaria se refieren al supuesto específico de responsabilidad patrimonial por ausencia de consentimiento informado, dejando al margen otros posibles (responsabilidad del fabricante por defecto de la vacuna o de la administración por errores en su autorización, conservación, distribución y administración).
Tomado de MEDINA ALCOZ L. “Responsabilidad patrimonial por reacción adversa a la vacunación: régimen general con referencia especial al caso del covid-19”. Revista de Derecho Público: Teoría y Método. 2022;6:51-91.
__________
113 Un estudio reciente sobre la responsabilidad patrimonial sanitaria, en MORENO ALEMÁN J, BOJ ALBARRACIÍN I, GONZÁLEZ CARRASCO MC, GARRIDO CUENCA N. Claves actuales de la responsabilidad patrimonial sanitaria. Colección Los Diez Esenciales de Aranzadi, 2023. En particular, la responsabilidad en materia de vacunación, pp.244 y ss.
114 https://www.poderjudicial.es/stfls/TRIBUNALES%20SUPERIORES%20DE%20JUSTICIA/TSJ%20Asturias/DOCUMENTOS%20DE%20INTER%C3%89S/TSJ%20Asturias%20Contencioso%2020%20febrero%202017.pdf
115 https://www.diariomedico.com/medicina/opinion/dos-visiones-de-la-sentencia-del-tjue-sobre-vacunas-y-enfermedades.html. En el mismo sentido, véase la nota del CAV-AEP, disponible en: https://www.diariomedico.com/normativa/el-comite-asesor-de-vacunas-calma-al-sector-sobre-los-efectos- del-fallo-del-tjue.html
116 Tuells, J, “Razones para un programa de compensación de daños por acontecimientos adversos relacionados con las vacunas en España”, en Medicina Clínica. 2013;140:554-7.
117 Garrido Cuenca NM. “Seguridad, riesgos y efectos adversos en materia de vacunación. Jurisprudencia sobre responsabilidad administrativa. Y reflexión: ¿Es necesario o conveniente un fondo específico de compensación por daños vacunales?” REDA Revista española de Derecho Administrativo, 2018;189;129-72.
118 RAMOS GONZÁLEZ S. “Daños vacunales: responsabilidad patrimonial y fondos de compensación”, en P. de Barrón Arniches (dir.). La salud y los derechos de la persona. Thomson Reuters-Aranzadi, Cizur Menor, 2022, pp. 207-42.
REBOLLO PUIG M. “Responsabilidad y ayudas públicas por daños de las vacunas contra la covid”. El Cronista del Estado Social y Democrático de Derecho, núms. 93-94, 2021, pp. 68-79.
119 Han sido un buen número de sentencias recaídas hasta la fecha sobre los efectos adversos de este medicamento, siendo la última de ellas, con cita de las precedentes, la STS (3.ª) de 23 de febrero 2022 (RJ 2022, 1107)
120 Texto integro en: https://www.comunidad.madrid/sites/default/files/dictamenes/2023/dictamen_40-23_des_0.pdf
121 https://www.cccyl.es/es/dictamenes/responsabilidad-patrimonial/covid-19/vacunas/2022-b1b5/dictamen-74-2022.ficheros/82155-Dictamen%2074-2022.pdf
9. VACUNAS Y RESPONSABILIDAD PROFESIONAL
9.4. ¿Qué responsabilidad asume el profesional sanitario que inyecta suero en lugar de la vacuna?
9.1. EN EL CASO DE QUE UN PEDIATRA DEL SISTEMA PÚBLICO PRESCRIBA UNA VACUNA NO INCLUIDA EN EL CALENDARIO VACUNAL. ¿ESTÁ OBLIGADO EL ENFERMERO DEL SISTEMA PÚBLICO A ADMINISTRARLA?
| La administración de las vacunas por la enfermería se hará conforme a la prescripción de la autoridad sanitaria (financiadas) o del médico (no financiadas) |
TRABAJO EN EQUIPO
El ejercicio de las profesiones sanitarias en la actualidad se lleva a cabo en equipos asistenciales que integran diversos profesionales; de las cuestiones relativas a las relaciones entre los distintos profesionales sanitarios y cómo se distribuyen las responsabilidades entre ellos se ocupa la Ley 44/2003, de 21 de noviembre, de ordenación de las profesiones sanitarias.
Los principios generales del ejercicio de las profesiones sanitarias se fijan en el art. 4, señalando en su punto 7 que:
“El ejercicio de las profesiones sanitarias se llevará a cabo con plena autonomía técnica y científica, sin más limitaciones que las establecidas en esta ley y por los demás principios y valores contenidos en el ordenamiento jurídico y deontológico, y de acuerdo con los siguientes principios: d) La continuidad asistencial de los pacientes, tanto la de aquellos que sean atendidos por distintos profesionales y especialistas dentro del mismo centro como la de quienes lo sean en diferentes niveles, requerirá en cada ámbito asistencial la existencia de procedimientos, protocolos de elaboración conjunta e indicadores para asegurar esta finalidad. e) La progresiva consideración de la interdisciplinariedad y multidisciplinariedad de los equipos profesionales en la atención sanitaria".
Los arts. 6 y 7 de la citada Ley se ocupan de fijar las competencias de los licenciados y diplomados sanitarios, si bien dichas competencias no se definen de forma cerrada, al entender el Legislador que deben primar los pactos interprofesionales, si bien es preciso destacar que corresponde a los licenciados sanitarios “la dirección y evaluación del desarrollo global de dicho proceso, sin menoscabo de la competencia, responsabilidad y autonomía propias de los distintos profesionales que intervienen en el mismo”.
Así pues, sin perjuicio de que todos los profesionales que integran el equipo asistencial gozan de autonomía técnica y científica, la Ley 44/2003 parece establecer cierta jerarquía académica en el funcionamiento de los equipos asistenciales, pues la decisión última le corresponde al médico en su condición de licenciado.
Según nuestro criterio, carece de sentido mantener como uno de los criterios de funcionamiento de los equipos asistenciales la categoría académica cuando la misma se ha visto modificada, tal y como establece la Disposición Adicional undécima de la propia Ley: “Las referencias que en esta ley se hacen a los licenciados y diplomados sanitarios se entenderán realizadas también a los graduados universitarios, de acuerdo con la normativa de ordenación de las enseñanzas universitarias oficiales”. Habrá, en consecuencia, que adaptar el funcionamiento del equipo asistencial a las novedades que se están produciendo en los planes formativos universitarios (el conocido como “Plan Bolonia”)122.
El art. 9 se ocupa de regular las relaciones interprofesionales y trabajo en equipo, señalando en su apartado 3 que: “Cuando una actuación sanitaria se realice por un equipo de profesionales, se articulará de forma jerarquizada o colegiada, en su caso, atendiendo a los criterios de conocimientos y competencia, y en su caso al de titulación, de los profesionales que integran el equipo, en función de la actividad concreta a desarrollar, de la confianza y conocimiento recíproco de las capacidades de sus miembros, y de los principios de accesibilidad y continuidad asistencial de las personas atendidas”.
De los preceptos expuestos resulta que en el trabajo en equipo priman los principios de coordinación y colaboración, conjugándose la idoneidad técnica o capacidad real con la no exclusividad, de acuerdo con las competencias y los conocimientos de cada profesión en función de su formación universitaria, evitando monopolios competenciales, sin perjuicio de la competencia esencial de cada profesión y la diferencia con las restantes profesiones.
| Las vacunas no financiadas deben ser prescritas por el médico en receta normalizada, pública o privada, por denominación comercial |
EL VALOR DE LA PRESCRIPCIÓN MÉDICA DE LAS VACUNAS NO FINANCIADAS
Aunque con carácter general se viene considerando que la administración de vacunas en el marco de una campaña de vacunación o de un calendario vacunal derivado de una decisión de la autoridad sanitaria en materia de salud pública no precisa prescripción médica, un Auto del Juzgado de lo Contencioso-Administrativo número 2 de Vitoria, de 22 de noviembre de 2016, al resolver una medida cautelar provisionalísima, contra la Instrucción 7/2015 de 2 de mayo, del Director General del Servicio Vasco de Salud por la que exoneraba de prescripción médica las vacunas financiadas y las de campañas vacunales, afirma que el régimen de las vacunas como medicamento inmunológico (art. 45 Lay de Garantía y Uso racional de medicamentos y productos sanitarios) está sujeto al común régimen de prescripción facultativa (art. 2 —19 y 20—, 43, 44, 45, 66.2 del Real Decreto 1345/2007, en relación con los artículos 6 y concordantes de la LOPS y el art. 2 y Disposición Adicional 5 Ley 41/2002).
El punto de partida para dar respuesta a la cuestión concreta que se nos plantea, es que las vacunas, tanto las financiadas como las no financiadas, son medicamentos sujetos a prescripción médica, por tratarse de medicamentos biológicos, tal y como se expone a continuación.
Conforme al artículo 19 del Real Decreto Legislativo 1/2015, de 24 de julio, por el que se aprueba el texto refundido de la Ley de garantías y uso racional de los medicamentos y productos sanitarios, la Agencia Española del Medicamento y Productos Sanitarios (AEMPS), cuando autoriza un medicamento debe determinar sus condiciones de prescripción, clasificándolos conforme se expone en la siguiente tabla 46.7:
Tabla 46.7 Medicamentos sujetos y no sujetos a prescripción médica. Tipología de prescripciones.
| Medicamentos no sujetos a prescripción médica | ||
| Medicamentos sujetos a prescripción médica a) Que puedan presentar un peligro, directa o indirectamente, incluso en condiciones normales de uso, si se utilizan sin control médico. b) Que se utilicen frecuentemente, y de forma muy considerable, en condiciones anormales de utilización, y ello puede suponer, directa o indirectamente, un peligro para la salud. c) Que contengan sustancias o preparados a base de dichas sustancias, cuya actividad y/o reacciones adversas sea necesario estudiar más detalladamente. d) Que se administren por vía parenteral, salvo casos excepcionales |
||
| Tipos de prescripciones médicas | ||
| Prescripción·médica de dispensación renovable o no renovable | Prescripción médica especial (estupefacientes, riesgo de adicción, sustancias que, por su novedad o propiedades, requieran especial precaución) | Prescripción médica restringida, de utilización reservada a determinados medios especializados (de uso hospitalario, de diagnóstico hospitalario y de especial control médico) |
Según se dispone en el art. 1 del Real Decreto 1718/2010, de 17 de diciembre, sobre receta médica y órdenes de dispensación: “la receta médica es el documento de carácter sanitario, normalizado y obligatorio mediante el cual los médicos, odontólogos o podólogos, legalmente facultados para ello, y en el ámbito de sus competencias respectivas, prescriben a los pacientes los medicamentos o productos sanitarios sujetos a prescripción médica, para su dispensación por un farmacéutico o bajo su supervisión, en las oficinas de farmacia y botiquines dependientes de las mismas o, conforme a lo previsto en la legislación vigente, en otros establecimientos sanitarios, unidades asistenciales o servicios farmacéuticos de estructuras de atención primaria, debidamente autorizados para la dispensación de medicamentos”.
La regulación contenida en el citado Real Decreto, sobre recetas médicas y órdenes de dispensación es aplicable, conforme establece el art. 2, “a la actuación de los profesionales sanitarios autorizados, en el ejercicio de sus funciones, en el ámbito de la asistencia sanitaria y atención farmacéutica del Sistema Nacional de Salud, incluidos los Regímenes Especiales de la Mutualidad General de Funcionarios Civiles del Estado (MUFACE), del Instituto Social de las Fuerzas Armadas (ISFAS) y de la Mutualidad General Judicial (MUGEJU), así como de las demás entidades, consultas médicas, establecimientos o servicios sanitarios similares públicos o privados, incluidos los dependientes de la Red Sanitaria Militar del Ministerio de Defensa, así como centros sociosanitarios y penitenciarios”. Al mismo tiempo, la receta médica constituye una garantía de que el tratamiento prescrito pueda ser dispensado al paciente en cualquier oficina de farmacia del territorio nacional.
Así pues, la receta médica, en este caso de una vacuna no financiada, es un instrumento que asegura la instauración de un tratamiento con medicamentos, siendo responsabilidad del resto de los profesionales sanitarios dar cumplimiento a la prescripción contenida en la receta: el farmacéutico ajustarse en la dispensación a lo pautado y la enfermería facilitar su administración.
__________
122 La normativa de ordenación de enseñanzas universitarias oficiales a tener en cuenta es: Ley Orgánica 2/2023, de 22 de marzo, del Sistema Universitario BOE 23 de marzo.
9.2. ¿CUÁL ES EL RIESGO LEGAL DEL PROFESIONAL SI TRAS LA ADMINISTRACIÓN DE UNA VACUNA NO INCLUIDA EN EL CALENDARIO OFICIAL APARECE UNA REACCIÓN ADVERSA?
| Las vacunas no oficiales, recomendadas por las sociedades científicas, avalan la lex artis de los profesionales sanitarios |
Para que haya responsabilidad legal sanitaria, deben concurrir, en todo caso, tres requisitos: daño, relación de causalidad entre el resultado dañoso y actividad sanitaria y, finalmente, un elemento de ilicitud, que en el ámbito sanitario se concretaría en la infracción de la lex artis ad hoc, entendida ésta como un criterio técnico para determinar la corrección o no de la actividad sanitaria exigible en una asistencia concreta (atendidas las circunstancias de lugar, tiempo, medios humanos y materiales disponibles, estado de la ciencia, etc.), que puede venir fijada —excepcionalmente— por normas jurídicas (lex artis codificada), por protocolos y guías clínicas y por informes periciales.
Resulta evidente que ajustar las recomendaciones de vacunación y la administración de vacunas al calendario oficial disminuye el riesgo legal del profesional sanitario, toda vez que el calendario oficial funcionaría como un criterio para la fijación de la lex artis, que en este caso vendría incluso reforzado por el hecho de tratarse de una lex artis que está recogida en una norma jurídica, siendo la prescripción de las mismas responsabilidad de la autoridad sanitaria.
Si la vacuna no está incluida en el calendario oficial, pero sí está aprobada por la autoridad competente y recomendada por la literatura médica y la comunidad científica (a través, por ejemplo, de sociedades científicas como, el Comité Asesor de Vacunas de la Asociación Española de Pediatría), aunque el riesgo legal se incrementa mínimamente, dichas recomendaciones permitirán sostener, al igual que con el calendario oficial, que la recomendación y administración de vacunas se ajusta a la lex artis, criterio éste que vendrá reforzado, en su caso, por informes periciales, si fueran precisos para la defensa del profesional.
Fuera de estos supuestos, la recomendación y administración de una vacuna que no esté incluida en el calendario oficial, ni en el calendario de sociedades científicas, incrementa considerablemente el riesgo legal, lo que exige que los profesionales sanitarios extremen el celo en justificar por qué está indicada la prescripción/administración de una determinada vacuna.
Identificados los escenarios de menor a mayor riesgo legal y centrándonos en el supuesto de que la vacuna recomendada no esté incluida en el calendario oficial, el profesional sanitario incurriría en responsabilidad si la vacuna no estaba médicamente indicada en el caso concreto, si no informó adecuadamente sobre los riesgos y no consta prueba de ello a través del consentimiento informado o medios alternativos de prueba, como la anotación en la historia clínica.
La responsabilidad personal del médico se podría exigir:
En vía civil (al pediatra privado), solicitando la indemnización de los daños y perjuicios ocasionados como consecuencia de la reacción adversa de la vacuna.
O en vía penal (tanto al pediatra privado, como al pediatra del sistema público), exigiendo la imposición de las penas correspondientes al ilícito penal y la responsabilidad civil derivada del mismo.
No cabe plantearse en estos supuestos una responsabilidad de la Administración, al no estar la vacuna incluida en el calendario oficial, sin perjuicio de la responsabilidad en que pudiera incurrir por la autorización de la vacuna a través de la Agencia Española de Medicamentos y Productos Sanitarios (AEMPS).
| En vacunas no financiadas es preciso informar sobre riesgos graves e infrecuentes |
Con el fin de reducir el riesgo legal y evitar la responsabilidad, es conveniente justificar médicamente la indicación de aplicar la vacuna no incluida en el calendario oficial (literatura médica y científica, calendarios recomendados de sociedades científicas, anotaciones en la historia explicando la motivación en base a los antecedentes médicos, etc.), extremar la información sobre los posibles riesgos y aunque podría ser recomendable que se firmara un consentimiento informado por escrito, lo cierto es que esto no forma parte de la práctica habitual, como vienen reconociendo los Tribunales.
Si la reacción adversa se debe al lote de vacunas, no habría responsabilidad para el profesional sanitario, siendo la responsabilidad objetiva por producto defectuoso del laboratorio fabricante de la vacuna. Véase en este sentido la Sentencia del Tribunal Supremo, Sala de lo Contencioso-Administrativo, Secc. 5.ª, núm. 1806/2021, de 21 de diciembre, según la cual la responsabilidad objetiva por los daños producidos por los medicamentos o productos sanitarios defectuosos no se extiende a quienes, de forma pública o privada, los adquieren, prescriben o aplican, lo que constituye un elemento de tranquilidad en relación con la responsabilidad legal relacionada con el uso de las vacunas (apartado 9.1).
9.3. ¿CUÁL ES LA RESPONSABILIDAD LEGAL DEL PEDIATRA SI RECOMENDÓ NO VACUNAR FRENTE A UNA DETERMINADA ENFERMEDAD Y POSTERIORMENTE EL PACIENTE LA DESARROLLA?
| Los profesionales que desaconsejan, de forma injustificada, la vacunación se exponen al riesgo de inhabilitación |
Cualquier recomendación del pediatra en este sentido debe estar basada en la literatura médica y científica en la materia, atendiendo a los antecedentes médicos del paciente, dejando constancia de todo ello en la historia clínica, con indicación de las razones y de la información suministrada a los padres o representantes legales.
En los casos más dudosos el pediatra debería buscar el amparo de un colectivo, ya sea una sesión clínica, el consejo o el dictamen de una sociedad científica (CAV-AEP), o evacuar una consulta a la Administración sanitaria.
Incurriría en responsabilidad profesional el pediatra: si la recomendación no estaba justificada médicamente, si no consta anotado en la historia clínica las razones médicas de la no indicación de una determinada vacuna y la información sobre los riesgos, o si el pediatra se apartó de las recomendaciones de la comunidad científica, de lo acordado en la sesión clínica, de las recomendaciones de la sociedad científica (CAV-AEP), o de la consulta evacuada a la Administración.
Las responsabilidades legales de aquellos profesionales sanitarios que desaconsejan la vacunación empezaron a plantearse con ocasión del caso de la difteria diagnosticado en Olot (2015): el Colegio Oficial de Médicos de Barcelona formuló consulta a la Organización Médica Colegial (OMC) sobre la posibilidad de imponer sanciones a los médicos que desaconsejan la aplicación de vacunas, tratamientos en caso de necesidad u otras medidas sanitarias que han probado su eficacia y eficiencia. Ya en ese momento la OMC entendió que es claro que se les puede aplicar el Código de Deontología Médica, pudiendo acarrear suspensión123, si bien la decisión al respecto dependerá de cada Colegio de Médicos.
Según el art. 26.2 del Código de Deontología Médica 2011 de la OMC124, no son éticas las prácticas carentes de base científica. Así lo establecen los arts. 22.3 “La promoción de una actividad preventiva solo es deontológicamente correcta cuando tiene un valor probado científicamente” y el art. 23.1 “El médico en su actuación profesional solo debe emplear procedimientos diagnósticos y terapéuticos que cuenten con base científica”.
En abril de 2018, el Colegio de Médicos de Barcelona sancionó con cinco años de inhabilitación a un facultativo por haber “divulgado y puesto en práctica con pacientes oncológicos el llamado Método Hamer, también conocido como Nueva Medicina”. En esa ocasión fue el propio facultativo el que dio motivo al inicio del procedimiento sancionador al remitir al Colegio un escrito defendiendo sus prácticas125.
En junio de 2019, tras una denuncia por la Confederación de Autismo de España, el Colegio de Médicos de Madrid inhabilitó durante 364 días a una pediatra por propagar que las vacunas causan el autismo, por difundir tesis no avaladas y contrarias a la ciencia médica. Considera el ICOMEM que la citada doctora incurre en “la divulgación de tesis no avaladas y contrarias a la evidencia acerca del origen y las causas del Trastorno del Espectro Autista” y la difusión de tratamientos e intervenciones “carentes de total evidencia y con importantes riesgos para la salud de las personas”.
El ICOMEM inhabilitó a la pediatra porque estos hechos vulneran diversos artículos del Código de Deontología Médica, como el 21.1, que dice “el médico tiene el deber de prestar a todos los pacientes una atención médica de calidad humana y científica" y el 23.1 "el médico debe disponer de libertad de prescripción, respetando la evidencia científica y las indicaciones autorizadas, que le permita actuar con independencia y garantía de calidad".
Idénticas responsabilidades serían exigibles al resto de los profesionales sanitarios con sus respectivos colegios profesionales.
__________
123 En países de nuestro entorno se imponían ya sanciones similares.
124 https://www.cgcom.es/sites/main/files/minisite/static/828cd1f8-2109-4fe3-acba-1a778abd89b7/codigo_deontologia/.
125 http://www.medicosypacientes.com/articulo/el-com-barcelona-inhabilita-un-medico-por-divulgar-y-practicar-procedimientos-sin-evidencia.
⌂
9.4. ¿QUÉ RESPONSABILIDAD ASUME EL PROFESIONAL SANITARIO QUE INYECTA SUERO EN LUGAR DE LA VACUNA?
| Responsabilidad penal de los que administren suero simulando que inoculan la vacuna |
Aunque los casos han sido aislados, han llegado a la vía penal algunos supuestos donde profesionales simulan inocular la vacuna y, en su lugar, inyectan suero o directamente no vacunan. El primer caso que fue juzgado en Sentencia de la Audiencia Provincial de Valencia, Tribunal del Jurado, de 7 de diciembre de 2017126, condenó a dos años de prisión por un delito de estafa y otro de falsedad a una pediatra que inyectaba suero fisiológico a los niños engañando a sus padres, a quienes hacía creer que eran vacunas por las que les cobraba cantidades que oscilan entre los 60 y los 1200 euros. Los hechos ocurrieron entre 2007 y 2011. La doctora recomendaba las vacunas a los padres de los menores para prevenir la varicela, el sarampión o el virus del papiloma humano. Le ofrecía la medicina a un precio inferior del que pagarían si tenían que adquirirla en una farmacia.
La doctora, funcionaria pública que engañó a los pacientes cuando trabajaba en el centro de Salud de Carlet y en el Hospital de La Ribera de Alzira, ha sido inhabilitada para ejercer cualquier profesión relacionada con la medicina durante dos años y tres meses. La sentencia es el resultado del acuerdo alcanzado entre la Fiscalía y la defensa de la médico, que hizo innecesaria la convocatoria del jurado popular para la celebración del juicio previsto.
Gran impacto mediático ha tenido también el caso de la enfermera vasca que supuestamente simuló vacunar a los niños del ambulatorio de Kabiezes en Santurtzi (Bizkaia). 42 familias han presentado una denuncia conjunta en los Juzgados de Instrucción de Barakaldo por los presuntos delitos de falsificación de documentos y de malversación de fondos. Se denuncia que rellenaba el calendario de vacunas del menor con la dosis correspondiente; y tiraba la jeringuilla con la dosis en su interior, lo que también podría suponer un claro perjuicio patrimonial a la Administración. Las sospechas de los padres, ante comportamientos extraños, comentarios antivacunas, El servicio de pediatría de la OSI Ezkerraldea Enkarterri Cruces inició un proceso de investigación para esclarecer los hechos y realizó pruebas serológicas a algunos de los niños a fin de detectar la presencia de anticuerpos en su organismo. Finalmente, convocó a medio centenar de familias para explicarles los resultados de los análisis y les propuso "una dosis adicional para lograr una correcta vacunación" para los niños que no tenían "unos niveles adecuados de anticuerpos".Osakidetza abrió un expediente informativo a la profesional y amplió la investigación a los 400 incluidos en el cupo de esa enfermera. Resulta grave este tipo de conductas, que podrían llegar a suponer un importante problema de salud pública, además de la comisión de los delitos denunciados.
__________
10. CALENDARIO ÚNICO DE VACUNACIÓN
10.2. ¿Cuáles son los límites legales que tiene un pediatra para prescribir una vacuna fuera de calendario?
10.3. Libertad de prescripción en relación con la ficha técnica del medicamento
10.4. Libertad de prescripción en relación con el calendario común de vacunación
10.1. TRAS LA APROBACIÓN DEL CALENDARIO ÚNICO POR PARTE DEL MINISTERIO DE SANIDAD EN 2013, CON UNA ÚLTIMA ACTUALIZACIÓN EN 2024 en el Calendario para toda la vida, ¿PUEDE UNA COMUNIDAD AUTÓNOMA MODIFICARLO O DEBE RESPETARLO SALVO QUE CONCURRAN RAZONES EPIDEMIOLÓGICAS?
| La inclusión de vacunas no previstas en el calendario único del Consejo Interterritorial del Sistema Nacional de Salud exige razones epidemiológicas y suficiencia financiera |
La declaración de coordinación de las políticas en materia de salud pública se establece en la Ley 16/2003, de 28 de mayo, de cohesión y calidad del SNS (arts. 65 y 71.1.l) y corresponde al Ministerio de Sanidad, previo acuerdo del Consejo Interterritorial del SNS.
La idea de un calendario único de vacunación en nuestro SNS tiene su antecedente inmediato en el acuerdo del 18 de marzo de 2010 entre Administración General del Estado y las CC. AA., en el seno del Consejo Interterritorial, dicho acuerdo fue aprobado por unanimidad integrado en un paquete de medidas orientadas a garantizar la sostenibilidad de nuestro sistema sanitario, en plena crisis económica.
Posteriormente, con la aprobación de la Ley 33/2011, General de Salud Pública, el art. 19.3.a), establece que:
“El Consejo Interterritorial del SNS acordará: a) un calendario único de vacunas en España. Las CC. AA. y las ciudades de Ceuta y Melilla sólo podrán modificarlo por razones epidemiológicas”. La formulación del precepto parece obligar a su cumplimiento a todas las CC. AA., que deberán ajustarse a él, salvo que concurran razones epidemiológicas que justifiquen su modificación.
El Pleno del Consejo Interterritorial del SNS, en su reunión del 21 de marzo de 2013 aprobó un calendario común de vacunación infantil, posteriormente se publicó la Resolución de 24 de julio de 2013, de la Dirección General de Salud Pública, Calidad e Innovación, por la que se hacía oficial el Acuerdo del Consejo Interterritorial del SNS sobre el calendario común de vacunación infantil. En 2019 se aprobó por el CISNS un calendario común para toda la vida. El calendario común de “vacunaciones e inmunizaciones a lo largo de toda la vida” para el año 2023 introduce algunas novedades importantes, al incluir cuatro nuevas vacunas: del Meningococo B y la de la gripe en la población infantil, la del Virus del Papiloma Humano (VPH) en los varones de 12 años y la del Herpes Zóster para mayores de 65 años.
En 2024, el calendario común de inmunización mantiene estas premisas. La gran novedad con respecto al del 2023 es la incorporación de la vacunación contra el rotavirus en lactantes a partir de las seis semanas, con la instrucción de que esta vacunación “deberá estar incorporada en todas las Comunidades Autónomas (CC. AA.) antes del fin de 2025”. La misma obligación se establece para la vacunación antimeningocócica tetravalente, Herpes Zóster y VPH. No se hacen recomendaciones sobre inmunización frente al VRS ni vacunación contra el SARS-CoV-2, con la aclaración a pie de calendario de que estas recomendaciones se “valorarán a finales de la actual temporada 2023-2024”127.
El calendario de vacunación será común, pero no es un calendario único pues, a pesar de lo dispuesto en el art. 19.3.a) de la Ley 33/2011, algunas CC. AA. se han apartado de él, respetando los mínimos, sin que concurra justificación epidemiológica, para incorporar otras vacunas, e incluso establecer periodos temporales etarios distintos a los recomendados en el Calendario común. Muchas de estas adiciones se ajustan al calendario de inmunización propuesto y recomendado por la AEP. Y es cierto que cada vez estamos más cerca de lograr ese calendario único al que compelía la LGSP.
Además, a pesar de que existe un calendario de vacunación para el 2024 a nivel estatal, como la gestión del proceso de vacunación está transferido, cada comunidad autónoma las va aplicando en su calendario de modo distinto (por ejemplo, en edades o tiempos). Las Consejerías competentes deciden cómo incorporar esta vacuna, después informan a los profesionales sanitarios y estos, con esas indicaciones, ya informan a los pacientes128. Sin embargo, aunque es cierto que cada vez estamos más cerca de lograr ese calendario único al que compelía la LGSP, y las convergencias son mayores, seguimos manejando en España veintiún calendarios vacunales: el calendario recomendado común del CISNS, los de las 17 CC. AA. y las ciudades de Ceuta y Melilla, y el calendario recomendado por la AEP.
El calendario de vacunas está incluido en la cartera de servicios comunes del SNS, tal y como resulta del Real Decreto 1030/2006, de 15 de septiembre, por el que se establece esta cartera de servicios comunes y el procedimiento para su actualización, en lo relativo a las actividades preventivas, tal y como establece el art. 3.1.a), que incluye:
"a) Vacunaciones en todos los grupos de edad y, en su caso, grupos de riesgo, según el calendario de vacunación vigente aprobado por el Consejo Interterritorial del SNS y las administraciones sanitarias competentes, así como aquellas que puedan indicarse, en población general o en grupos de riesgo, por situaciones que epidemiológicamente lo aconsejen".
El Real Decreto Ley 16/2012 de 20 de abril, de medidas urgentes para garantizar la sostenibilidad del SNS y mejorar la calidad y seguridad de sus prestaciones, modificó en su artículo 2 el Real Decreto 1030/2006, clasificando las prestaciones en:
1. Cartera común básica de servicios asistenciales del SNS
2. Cartera común suplementaria del SNS
3. Cartera común de servicios accesorios del SNS
4. Cartera de servicios complementaria de las comunidades autónomas
Tal y como se establece en el art. 8 quinquies del Real Decreto 1030/2006 (en su redacción por el Real Decreto Ley 16/2012), relativa a la cartera de servicios complementarios de las comunidades autónomas: "1. Las comunidades autónomas, en el ámbito de sus competencias, podrán aprobar sus respectivas carteras de servicios que incluirán, cuando menos, la cartera común de servicios del SNS en sus modalidades básica de servicios asistenciales, suplementaria y de servicios accesorios, garantizándose a todos los usuarios del mismo. 2. Las comunidades autónomas podrán incorporar en sus carteras de servicios una técnica, tecnología o procedimiento no contemplado en la cartera común de servicios del SNS, para lo cual establecerán los recursos adicionales necesarios. 3. Las comunidades autónomas deberán destinar los recursos económicos necesarios para asegurar la financiación de la cartera común de servicios, siendo preceptiva, para la aprobación de la cartera de servicios complementaria de una comunidad autónoma, la garantía previa de suficiencia financiera de la misma en el marco del cumplimiento de los criterios de estabilidad presupuestaria".
De acuerdo con ello, la aprobación del calendario común de vacunación infantil se configura con un carácter de mínimos, estando obligadas todas las comunidades autónomas a garantizar su cumplimiento, si bien es posible (incluso después de la aprobación del Real Decreto Ley 16/2012, de 20 de abril) que las comunidades autónomas fijen prestaciones complementarias, debiendo, eso sí, contar las mismas con la suficiencia financiera que permita hacer frente a las mismas.
__________
127 https://vacunasaep.org/documentos/manual/cap-7#f7.13
128 Por ejemplo, la Comunidad de Madrid ya ha anunciado que desde el 1 de enero de 2023 incluye la vacuna del Meningococo B pero solo para los nacidos a partir del 1 de noviembre de 2022. También a partir del 1 de enero de 2023 se amplía la vacunación frente al virus del papiloma humano a los niños nacidos en 2011, cuando cumplan los 12 años de edad. En el caso de la vacuna de la gripe infantil se pondría en el mes de octubre de 2023. Sobre la vacuna frente al Herpes Zóster, en la Comunidad de Madrid se empezó a administrar ya en mayo de 2022 para grupos de riesgo y para personas de 65 y 80 años de edad (cohortes nacidas en 1942 y 1957 respectivamente) y ahora en 2023 se amplía a las personas entre los 75 y 80 años de edad.
10.2. ¿CUÁLES SON LOS LÍMITES LEGALES QUE TIENE UN PEDIATRA PARA PRESCRIBIR UNA VACUNA FUERA DE CALENDARIO?
La libertad de prescripción médica constituye una manifestación de la libertad profesional, derecho fundamental consagrado en el art. 35 de la Constitución, que regula el derecho a libre elección de profesión u oficio y en el art. 36, que regula el ejercicio de las profesiones tituladas, que sólo puede limitarse por Ley y no por prácticas administrativas.
Así pues, se establece en nuestra Constitución una reserva de ley para determinar una serie de cuestiones: qué profesiones precisan de un título para ser ejercidas; qué título permite ese ejercicio; y la definición del contenido mínimo de actividades que integran esa profesión. De estas cuestiones se ocupa, por lo que se refiere al ámbito sanitario, la Ley 44/2003 de 21 de noviembre, de ordenación de las profesiones sanitarias.
Sin embargo, se trata de una reserva de ley relativa, pues el legislador no está obligado a respetar un contenido esencial, pues el artículo 35 no garantiza el derecho a desarrollar cualquier profesión u oficio, sino el de elegir libremente profesión u oficio, siendo posible que las regulaciones limitativas del ejercicio de las profesiones pueden hacerse mediante normas de naturaleza reglamentaria.
La libertad de prescripción es, en lo que a los médicos se refiere, la principal manifestación de la plena autonomía técnica y científica que se establece para todos los profesionales sanitarios en el art. 4.7 de la Ley 44/2003 y, uno de los principios básicos del ejercicio privado de la profesión, es la libertad de prescripción atendiendo al conocimiento científico y a la observancia de la ley (Art. 40.3.i) Ley 44/2003).
Desde un punto de vista deontológico, la libertad de prescripción se encuentra recogida en el Código de Deontología Médica de diciembre de 2022124 que, en su art. 20.1, se considera como “un elemento esencial del acto médico, por lo que el médico es responsable de realizarla”. El art. 20.2 sentencia que “El médico tiene que disponer de libertad de prescripción, respetando la evidencia científica, las indicaciones autorizadas y la eficiencia” (respecto al Código anterior, ha desaparecido la frase “que le permita actuar con independencia y garantía de calidad”). Y el art. 22.3 recuerda que “la promoción de una actividad preventiva solo es deontológicamente correcta cuando tiene un valor probado científicamente”.
Téngase en cuenta que las previsiones del citado Código deben distinguirse de las imposiciones descritas en las leyes, si bien son normas de obligado cumplimiento para todos los médicos en el ejercicio de la profesión, cualquiera que sea la modalidad en la que la practiquen. El incumplimiento de las normas de este código puede suponer la incursión en falta disciplinaria tipificada en los Estatutos Colegiales cuya corrección se hará a través del procedimiento normativo en ellos establecido.
Ahora bien, la libertad de prescripción no es ilimitada y la misma puede venir condicionada por la ficha técnica del medicamento y por el calendario oficial de vacunación, cuestiones ambas de las que nos ocupamos a continuación.
10.3. LIBERTAD DE PRESCRIPCIÓN EN RELACIÓN CON LA FICHA TÉCNICA DEL MEDICAMENTO
| La prescripción de una vacuna fuera de lo previsto en la ficha técnica (nunca fuera de la indicación de la misma), es posible en base a estudios, ensayos o recomendaciones de la comunidad científica |
La LM (art. 31.2) y el Real Decreto 1345/2007, de 11 de octubre, por el que se regula el procedimiento de autorización, registro y condiciones de dispensación de los medicamentos de uso humano fabricados industrialmente, se ocupan de regular la ficha técnica (o resumen de las características del producto), entendida ésta como el documento autorizado por la AEMPS, donde se reflejan las condiciones de uso autorizadas para el medicamento y recoge la información científica esencial para los profesionales sanitarios.
Por tanto, la ficha técnica aprobada por la AEMPS es un documento administrativo vinculante que garantiza la identidad, la integridad de la información y una correcta praxis médica en relación con el medicamento (en nuestro caso, en relación con las vacunas), condiciona la información, condiciona y determina la prescripción médica, de modo que el pediatra no tiene una facultad ilimitada de prescripción, sino que la misma viene, en principio, determinada por las condiciones de uso en las que la vacuna haya sido autorizada.
No obstante, es posible el uso de medicamentos en condiciones distintas de las autorizadas, tal y como se establece en el Real Decreto 1015/2009, de 19 de junio, por el que se regula la disponibilidad de medicamentos en situaciones especiales, cuyo artículo 13.1 dispone que:
"1. La utilización de medicamentos autorizados en condiciones diferentes a las establecidas en su ficha técnica tendrá carácter excepcional y se limitará a las situaciones en las que se carezca de alternativas terapéuticas autorizadas para un determinado paciente, respetando en su caso las restricciones que se hayan establecido ligadas a la prescripción y/o dispensación del medicamento y el protocolo terapéutico asistencial del centro sanitario. El médico responsable del tratamiento deberá justificar convenientemente en la historia clínica la necesidad del uso del medicamento e informar al paciente de los posibles beneficios y los riesgos potenciales, obteniendo su consentimiento conforme a la Ley 41/2002, de 14 de noviembre".
Por tanto, el pediatra que prescriba una vacuna fuera de la previsión de la ficha técnica debe hacerlo tomando en cuenta que esta práctica tiene carácter excepcional, que debe hacerlo en base a estudios, ensayos o recomendaciones de la comunidad científica (por ejemplo, las del CAV-AEP), dejando constancia de ello en la historia clínica e informando a padres, representantes legales y menores del uso no autorizado de la vacuna.
Si se produce un resultado adverso por la administración de la vacuna fuera de indicación, el fabricante no asumiría el daño al haberse producido al margen de las previsiones de la ficha técnica.
En cambio, cumplidos los requisitos del Real Decreto 1015/2009, la Administración podría ser declarada responsable del daño; sin perjuicio de la posibilidad, prevista en el art. 36.2 de la Ley 40, 2015, de 1 de octubre, de Régimen Jurídico del Sector Público de que la Administración ejercite la acción de regreso contra el profesional del servicio público que hubiera ocasionado el daño interviniendo dolo, culpa o negligencia grave, si bien dicha situación carece de precedentes en el ámbito sanitario público.
Por lo que se refiere al ámbito privado, el Real Decreto 1015/2009 establece en su art. 4 que la cobertura de la responsabilidad por los daños derivados de los supuestos previstos en este Real Decreto se regirá por lo dispuesto en el art. 46 de la Ley 44/2003, que establece el seguro obligatorio de responsabilidad civil para los profesionales sanitarios que ejerzan en el ámbito de la asistencia sanitaria privada.
En fin, debe tenerse en cuenta que el futuro de la inmunización y los avances hacia una medicina cada vez más personalizada (también en este terreno de la vacunación/inmunización) nos pueden llegar a situar en un panorama muy distinto al de las normas clásicas sobre prescripción, uso de medicamentos en situaciones especiales y responsabilidad. Puesto que, en ocasiones, puede que incluso la prescripción fuera de ficha técnica dependiendo de la situación individualizada del paciente venga recomendada por la evidencia científica e incluso por las mismas autoridades sanitarias, como vimos en la introducción de este Manual. En este último caso al menos, deberían imperar las normas de responsabilidad patrimonial sanitaria que cabe exigir a las Administraciones Públicas.
10.4. LIBERTAD DE PRESCRIPCIÓN EN RELACIÓN CON EL CALENDARIO COMÚN DE VACUNACIÓN
El calendario común de vacunación infantil aprobado por el Consejo Interterritorial, así como los calendarios oficiales de las diferentes CC. AA., no son obligatorios, sino meras recomendaciones, tanto para los ciudadanos como para los profesionales, para los que tendrían, desde el punto de vista legal, un papel similar a los protocolos y guías clínicas, debiendo el profesional que se apartara de ellos justificar médicamente los motivos que le llevan a supravacunar (o, en su caso, a infravacunar), siendo lo más seguro desde el punto de vista del riesgo legal ajustarse al calendario de la comunidad autónoma en la que presta sus servicios, tal y como se expone en el apartado 10.2.
El mero hecho de apartarse de las recomendaciones del calendario de vacunación y prescribir una vacuna no incluida en el calendario oficial, sin que el paciente sufra daño alguno, no daría lugar a ningún tipo de responsabilidad para el profesional, pero sí podría determinar actuaciones disciplinarias (ante los Servicios de Salud autonómicos en los que el profesional prestara sus servicios ) o deontológicas (ante las comisiones deontológicas de los Colegios de Médicos) si se estimara que la actuación del profesional supone un riesgo cierto para la salud colectiva de un determinado sector de la población.
Si como consecuencia de apartarse del calendario oficial, el paciente sufriera algún daño provocado por la reacción adversa a una vacuna no recomendada (o desarrollara la enfermedad inmunoprevenible contra la que no se vacunó por decisión del médico), habría que analizar la lex artis del profesional para determinar su responsabilidad, tal y como se expuso en el apartado 10.2, al que nos remitimos. Y con las consideraciones que acabamos de señalar ante el futuro de la inmunización.
11. SITUACIONES ESPECIALES: COMPRA DE VACUNAS FUERA DE ESPAÑA
11.2. La compra de vacunas por internet
11.3. La compra de vacunas en oficinas de farmacia de países limítrofes
11.1. SI LOS PADRES CONSULTAN SOBRE LA COMPRA DE VACUNAS NO DISPONIBLES EN NUESTRO PAÍS, ¿CUÁL DEBE SER LA RECOMENDACIÓN DEL PROFESIONAL, DESDE UN PUNTO DE VISTA LEGAL?
Las restricciones en relación con la vacuna de la varicela y la escasez de dosis de la vacuna del meningococo B —ya superadas—, provocaron la búsqueda de canales alternativos para poder conseguirlas, tanto la compra en Internet, como el turismo sanitario, consistente en acudir a la compra directa en farmacias de países limítrofes (esta situación se sigue manteniendo en regiones próximas a países vecinos donde los precios de las vacunas pueden ser más bajos que los de España). Sin embargo, los problemas de desabastecimiento de medicamentos, en general, es un grave problema global que está afectando a los sistemas sanitarios y a la salud ciudadana129, por lo que está siendo objeto de atención por las instituciones públicas, cuyas actuaciones y previsiones deben aplicarse son lugar a dudas también en el campo de la vacunación130. Sin embargo, recordemos que, frente a otros medicamentos, por regla general las vacunas no son sustituibles, a no ser que existan alternativas y, aun en este caso, deben seguirse las recomendaciones de las autoridades públicas o instituciones especializadas que, por ejemplo, en vacunación pediátrica, recomiendan unas presentaciones frente a otras, de acuerdo a la evidencia científica.
__________
129 https://diariofarma.com/2024/01/30/la-farmacia-mundial-da-la-voz-de-alarma-ante-el-aumento-en-los-problemas-de-suministro
130 Dentro de la EMA, destaca la creación en 2022 del Grupo Directivo Ejecutivo sobre Desabastecimiento y Seguridad de Medicamentos (Executive Steering Group on Shortages and Safety of Medicinal Products, MSSG). Este grupo establece recomendaciones para la implementación de acciones coordinadas a nivel de la UE en relación con los problemas de suministro de medicamentos, además de monitorizar el suministro y la demanda de medicamentos considerados críticos. La directora de la AEMPS colabora activamente en MSSG con sus homólogos de otros Estados miembro, así como con la directora de la EMA y el representante de la Comisión Europea. MSSG toma como base para sus actividades la información proporcionada por EU SPOC (Single Point of Contact) Network, red en la que también participa de forma activa la AEMPS. Esta red lleva a cabo una monitorización continua de problemas de suministro en Europa, permitiendo el intercambio de información entre Estados miembro con el fin de coordinar la búsqueda de soluciones beneficiando a todos los países de manera equilibrada. Una información completa sobre todas las iniciativas en: https://www.aemps.gob.es/profesional-sanitario/problemas-de-suministro-de-medicamentos/
11.2. LA COMPRA DE VACUNAS POR INTERNET
| La compra de vacunas por Internet es ilegal |
La compra de medicamentos por Internet no se puede considerar una compra segura desde el punto de vista sanitario, pues, según datos de la Organización Mundial de Salud, más del 50 % de las medicinas compradas por Internet son falsificadas y hay muchas posibilidades de que el internauta sea engañado131.
Al margen de la seguridad de la compra por Internet, la misma no es legal cuando se trata de medicamentos sujetos a prescripción médica, como es el caso de las vacunas. En este sentido, el art. 3.5. LM establece que: “Se prohíbe la venta por correspondencia y por procedimientos telemáticos de medicamentos y productos sanitarios sujetos a prescripción”.
Así pues, si los padres o tutores consultan sobre la compra de vacunas en Internet deben ser alertados de que dicha práctica es ilegal y, en consecuencia, los profesionales sanitarios deben rechazar la administración de vacunas adquiridas por este canal.
Otra situación bien distinta es la compra por Internet de los medicamentos no sujetos a prescripción, permitida en mismo art. 3.5 LM y desarrollada por el Real Decreto 870/2013, de 8 de noviembre, por el que se regula la venta a distancia al público, a través de sitios web, de medicamentos de uso humano no sujetos a prescripción médica y por el Reglamento de Ejecución (UE) Nº 699/2014 del Parlamento Europeo y del Consejo, de 24 de junio de 2014 sobre el diseño del logotipo común para identificar a las personas que ofrecen al público medicamentos por venta a distancia y los criterios técnicos, electrónicos y criptográficos a efectos de la verificación de la autenticidad de dicho logotipo.
El 1 de julio de 2015, se ha puesto en marcha en toda Europa un sistema de venta de medicamentos de uso humano no sujeto a prescripción médica a través de Internet, utilizando un logotipo común europeo, sistema que ha sido desarrollado en España por la AEMPS en la Web www.distafarma.aemps.es, con el fin de facilitar una compra telemática segura de medicamentos no sujetos a prescripción médica.
__________
131 Sobre los riesgos de la compra de medicamentos por Internet, véase el portal de venta a distancia de la AEMPS y también la noticia publicada por el CAV-AEP sobre este asunto.
11.3. LA COMPRA DE VACUNAS EN OFICINAS DE FARMACIA DE PAÍSES LIMÍTROFES
Descartada la legalidad de la compra de medicamentos sujetos a prescripción médica por Internet, nos corresponde analizar la compra de vacunas fuera de España, lo que constituye una práctica no exenta de serios peligros132.
Desde el punto de vista legal se trata de una cuestión compleja, sin respuestas claras en nuestra normativa.
Una opción es considerar que estamos ante la importación de medicamentos, que debe ajustarse a las exigencias contenidas en la siguiente normativa:
- LM (arts. 63, 72)
- Real Decreto 824/2010, de 25 de junio, por el que se regulan los laboratorios farmacéuticos, los fabricantes de principios activos de uso farmacéutico y el comercio exterior de medicamentos y medicamentos en investigación (arts. 5 a 22)
- Circular 1/2015 AEMPS (Capítulo II, apartado 1)
El régimen impuesto por la citada normativa al importador (autorización de la importación por la AEMPS, comercialización a través de canales farmacéuticos legalmente habilitados o establecerse como mayorista, contar con un director técnico, contar con un seguro o aval financiero) es evidente que, caso de ser el aplicable a esta compra de medicamentos en países vecinos, colocaría la totalidad de estas compras en un régimen de manifiesta ilegalidad, tanto para los particulares que realizaran la importación, como para los profesionales sanitarios que hacen uso de los medicamentos importados ilegalmente.
Si bien se pueden albergar dudas sobre la aplicación de este régimen a la compra de vacunas en el extranjero por particulares, es claro que este es el régimen aplicable a los farmacéuticos que compran vacunas en países extranjeros para venderlas en sus farmacias, por tanto, estas conductas son manifiestamente ilegales y los farmacéuticos que las llevan a cabo quedan expuestos a graves sanciones, tanto administrativas como —en su caso— penales.
Otra opción es entender que la vacuna así adquirida tendrá la consideración legal de medicamentos destinados al tratamiento de los viajeros, de los que se ocupa el art. 74 LM, en el que se establece que:
“ 1. Los medicamentos que acompañen a los viajeros destinados a su propia administración o tratamiento quedan excluidos de las exigencias establecidas en los artículos anteriores (relativas a importación y exportación de medicamentos), sin perjuicio de las medidas de control cuando dichos medicamentos pudieran representar una desviación por su cuantía o destino especialmente en prevención de su utilización ilícita.
2. Las Administraciones públicas adoptarán las medidas oportunas para impedir que los productos objeto de esta Ley, en régimen de tránsito hacia un tercer país, puedan ser desviados para su uso en España sin cumplimiento de las exigencias previstas en esta Ley”.
Así pues, se deja un amplio margen a la decisión individual del viajero, del profesional y de los diferentes servicios de salud, que han resuelto de manera diferente esta cuestión, como se expuso en el apartado 8.2 , al que nos remitimos.
La compra de vacunas en terceros países para ser administradas en España representa una situación de riesgo sanitario para los destinatarios de la vacuna (pues no hay garantía de las adecuadas condiciones de conservación y trazabilidad) e incrementa el riesgo legal para los profesionales que intervienen en la prescripción/administración de las mismas (véase el apartado 8.1 en relación al riesgo legal de prescribir/administrar la vacuna de la varicela), si bien dicho riesgo se ve minimizado en aquellas comunidades autónomas en las que se ha autorizado expresamente dicha práctica, como Madrid y Extremadura.
__________
132 ¿Es peligroso comprar vacunas en el extranjero? - Boticaria García (boticariagarcia.com)
12. BIBLIOGRAFÍA
- Antequera Vinagre JM. Vacuna en pediatría de Atención Primaria; marco legal, responsabilidad y prescripción. Rev Pediatr Aten Primaria. 2005;7 Supl 4:S125-33.
- De Lorenzo R. Responsabilidad por no vacunación. Redacción Médica. 2013.
- Cierco Seira, C. Las vicisitudes del calendario único de vacunación. Revista Derecho y Salud, Vol. 29. Extraordinario - 2019.
- Delgado Garrido C. “El debate sobre la voluntariedad o la obligatoriedad de la vacunación en tiempos de pandemia”. RVAP. 2021;121:17-59.
- Di Prieto ML, et al. Sobre la “responsabilidad“ de la vacunación. En: Cuad Bioét. 2012;XXIII:323-36.
- Faus Santasusana J, et al. Tratado de Derecho Farmacéutico. Estudio del régimen jurídico de los medicamentos. Ed. Aranzadi S.A.U. Cizur Menor (Navarra), 2017. ISBN 978-84-9059-995-2.
- Fernández-Prada M, et al. Redefiniendo el paradigma de la vacunación en inmunodeprimidos después de la pandemia. Enferm Infecc Microbiol Clin (Engl Ed). 2023;41:524-5.
- García Ruiz Y. ¿Vacunaciones obligatorias de menores contra la voluntad de los padres? En Humanitas Humanidades Médicas. 2009;35:1-23.
- Garrido Cuenca NM. A vueltas con la vacuna de la varicela: cuestiones jurídicas, transparencia y salud pública frente a Lobbies e intereses económicos.
- Garrido Cuenca NM. Seguridad, riesgos y efectos adversos en materia de vacunación. Jurisprudencia sobre responsabilidad administrativa. Y reflexión: ¿Es necesario o conveniente un fondo específico de compensación por daños vacunales? REDA Revista española de Derecho Administrativo 2018. Núm. 189 (Enero-Marzo 2018).
- Garrido Cuenca N. Seguridad de pacientes y salud mental en la infancia y la adolescencia: apuntes desde el derecho sanitario para una revisión del consentimiento informado, los tratamientos involuntarios y la respuesta a las conductas autolíticas. Revista Derecho y Salud, Volumen 33. Extraordinario – 2023
- Garrido Cuenca N. Political and regulatory key factors of transparency and independence in terms of vaccination in Spain: information,participation and lobbies. Pharmaceuticals Policy and Law 2017;19:103-20.
- Garrido Cuenca N. Predicaments during a period of health emergency: Waiving patent protections or innovative public procurement? Theexample of advance purchase agreements (APA) for COVID-19 vaccines, Int J Risk Saf Med. 2022;33:145-56.
- González Carrasco C, et al. “Vacunación contra la Covid-19 en menores. La capacidad decisoria en distintos escenarios”, CESCO, Noticias, diciembre 2021.
- González Carrasco MC. La prestación del consentimiento informado en materia de salud en el nuevo sistema de apoyos al ejercicio de la capacidad. Derecho Privado y Constitución, 39, julio-diciembre (2021), pp. 213-47.
- González Carrasco MC, et al. “El servicio autonómico de salud no responde por las lesiones causadas a un paciente como consecuencia de la utilización de un producto sanitario defectuoso autorizado por la AEMPS”, CESCO, febrero 2021.
- Macía Morillo A. La responsabilidad civil médica. Las llamadas acciones de wrongful birth y wrongful life. Revista de Derecho Barranquilla. 2007;27:3-37.
- Montalvo Jääskeläinen F, et al. Aspectos legales de las vacunas. En: Comité Asesor de Vacunas de la Asociación Española de Pediatría (CAV-AEP). Vacunas en Pediatría. Manual de la AEP 2012, 5.ª ed. Madrid: Exlibris ediciones SL; 2012. p. 565-77.
- Medina Alcoz L. “Responsabilidad patrimonial por reacción adversa a la vacunación: régimen general con referencia especial al caso del covid-19”. Revista de Derecho Público: Teoría y Método. 2022;6:51-91.
- Moreno Alemán J, et al. Claves actuales de la responsabilidad patrimonial sanitaria. Colección Los Diez Esenciales de Aranzadi, 2023. En particular, la responsabilidad en materia de vacunación, pp.244 y ss.
- Moreno Soler V. “El régimen jurídico de la vacuna contra la covid-19 en la actualidad: de la imposición general a la resolución de conflictos entre progenitores”. Actualidad Jurídica Iberoamericana N.º 17 bis, diciembre 2022.
- Ramos González S. “Daños vacunales: responsabilidad patrimonial y fondos de compensación”. En P. de Barrón Arniches (dir.). La salud y los derechos de la persona. Thomson Reuters-Aranzadi, Cizur Menor, 2022, pp. 207-42.
- Rebollo PuigM. “Responsabilidad y ayudas públicas por daños de las vacunas contra la covid”. El Cronista del Estado Social y Democrático de Derecho. 2021;93-94:68-79.
- Sancho Gargallo I. Tratamiento legal y jurisprudencial del consentimiento informado. InDret: Revista para el análisis del Derecho. 2004; 209:1-24.
- Tolosa Triviño C. Vacunas. Aspectos Legales. En: Hidalgo Vicario I, Montón Álvarez JL, eds. Vacunas. Algo más que el calendario vacunal. Cuestiones y respuestas. Madrid: Ed. Undergraf; 2014. p 525- 38.
13. Enlaces de Interés
14. Historial de actualizaciones
| 2 de octubre de 2018 | Actualización de todos los apartados. Nuevas citas bibliográficas |
| 26 de abril de 2021 | Actualización de todos los apartados. Nuevas citas bibliográficas |
| 13 de agosto de 2021 | Aclaración del subapartado 3.6 |
| 17 de enero de 2022 | Aclaraciones del apartado 5.2 |
| 25 de enero de 2023 | Cambio de nombre a Manual de Inmunizaciones |
| 18 de abril de 2024 | Actualización de todos los apartados. Nuevas citas bibliográficas |
-oOo-