La investigación de la vacuna MTBVAC frente a la tuberculosis en la hora de la verdad
| Contenido |
|---|
| ● Introducción ● Tuberculosis [ver] ● Panorama general de las vacunas de la tuberculosis en desarrollo [ver] ● La vacuna MTBVAC [ver] ● Ensayo aleatorizado de fase 3 ● Comparativa con la BCG: efectos heterólogos de MTBVAC ● Referencias bibliográficas clave ● Más información en esta web y referencias bibliográficas [ver] |
| En pocas palabras |
|---|
| ● En el Día Mundial de la tuberculosis (24 de marzo) se ha recordado que esta enfermedad vuelve a ser, una vez que la covid ha perdido fuerza, la principal causa de muerte por causa infecciosa en el mundo. ● La vacuna BCG, en uso desde hace unos 100 años, es eficaz en la prevención de formas graves de la enfermedad en la edad pediátrica, pero ha fracasado contra la TBC pulmonar en adolescentes y adultos, que es la principal fuente de difusión de la infección. ● La investigación de nuevas vacunas viene de décadas atrás y, en general, con escaso éxito, aunque en los últimos años se ha constatado un mayor interés y algunos avances. ● Además de las que se destinan a adolescentes y adultos, dos vacunas atenuadas destinadas a recién nacidos y lactantes se encuentran en estudios de fase 3. ● Una de estas es MTBVAC, una vacuna basada en M. tuberculosis, ha sido desarrollada en la Universidad de Zaragoza, por el equipo de Carlos Martín Montañés. ● El estudio de fase 3 de MTBVAC se desarrolla en Sudáfrica, Madagascar y Senegal y se prevé una duración de 5-6 años. ● Se han depositado muchas esperanzas en que esta vacuna, diseñada y desarrollada por investigadores españoles, pueda contribuir de forma sólida al control de la tuberculosis a nivel global. |
-oOo-
Introducción
La vacuna MTBVAC ha sido desarrollada por el equipo de Carlos Martín Montañés en la Universidad de Zaragoza, con la participación del consorcio TBVI y la empresa biofarmacéutica española Biofabri.
El desarrollo clínico de MTBVAC comenzó en octubre de 2013 (ver la imagen que encabeza esta nota), y ahora, inicia la fase crucial, la fase 3. De confirmarse las expectativas, podría constituir un hito en la historia de las vacunas. Se comentan en esta nota algunos pormenores de esta etapa crucial en el desarrollo de MTBVAC en el contexto de la intensa y prolongada investigación de nuevas vacunas frente a la TBC.
[volver al principio]
Tuberculosis
La tuberculosis (TBC) está causada por Mycobacterium tuberculosis. En 2021, hubo más de 10 millones de casos nuevos y, aproximadamente, 1,6 millones de personas murieron por esta enfermedad, según el Informe mundial de la TBC de 2022. A medida que la pandemia de COVID-19 ha reducido su presión, la TBC ha recuperado el puesto de principal causa infecciosa de muerte en gran parte del mundo (más de 4000 muertes diarias a nivel global); la tuberculosis mata a más personas cada año que el VIH y el paludismo (malaria) juntos.
Según la OMS, 30 países representaron el 87 % de todos los casos nuevos en el mundo, y ocho de estos países reúnen más de dos tercios del total: India (28 %), Indonesia (9,2 %), China (7,4 %), Filipinas (7,0 %), Pakistán (5,8 %), Nigeria (4,4 %), Bangladesh (3,6 %) y República Democrática del Congo (2,9 %).
En el Dia Mundial de la tuberculosis (24 de marzo), algunos informes señalan un incremento de la incidencia en EE. UU. y Europa y una reducción en la región de África de la OMS.
Fuentes: IAVI, International AIDS Vaccine Initiative; OMS, 24 de marzo de 2023, Día Mundial de la tuberculosis; CIDRAP, 23 de marzo y 24 de marzo de 2023.
[volver al principio]
Panorama general de las vacunas de la tuberculosis en desarrollo
 La única vacuna autorizada contra la TBC es la BCG, que se desarrolló hace más de 100 años. Esta vacuna tiene eficacia en la protección contra la TBC grave, como la meningitis tuberculosa y la TBC miliar en bebés y niños pequeños, pero ofrece una protección variable y en su mayoría deficiente contra la TBC pulmonar en adolescentes y adultos. Dado que esta forma es el principal medio por el cual se propaga la infección, es esencial contar con vacunas nuevas y efectivas capaces de prevenir el desarrollo de la TBC pulmonar en estas poblaciones para controlar y finalmente poner fin a la pandemia de TB en curso.
La única vacuna autorizada contra la TBC es la BCG, que se desarrolló hace más de 100 años. Esta vacuna tiene eficacia en la protección contra la TBC grave, como la meningitis tuberculosa y la TBC miliar en bebés y niños pequeños, pero ofrece una protección variable y en su mayoría deficiente contra la TBC pulmonar en adolescentes y adultos. Dado que esta forma es el principal medio por el cual se propaga la infección, es esencial contar con vacunas nuevas y efectivas capaces de prevenir el desarrollo de la TBC pulmonar en estas poblaciones para controlar y finalmente poner fin a la pandemia de TB en curso.
La investigación de vacunas frente a la tuberculosis viene de décadas atrás y con escaso éxito. Sin embargo, en los últimos años ha ganado fuerza e intensidad. En 2018, un ensayo de fase 2 realizado en Sudáfrica mostró que la revacunación de los adolescentes con la misma BCG que recibieron cuando eran bebés redujo significativamente la incidencia de infecciones sostenidas de TBC. Otro estudio de eficacia de fase 2b, realizado por Aeras (posteriormente, IAVI) en colaboración con GSK, mostró que la vacuna M72 administrada junto con el adyuvante AS01E, protegía contra la tuberculosis pulmonar activa en adultos con infección latente, con una eficacia del 50%. Estos hallazgos, si se confirman en estudios de seguimiento, representarían un gran avance en la búsqueda para desarrollar una vacuna eficaz contra la TB.
Se exploran también otros enfoques (ver imagen adjunta [fuente: TBVI]). En cuanto a las vacunas destinadas a recién nacidos y lactantes hay dos productos candidatos en la fase 3 de desarrollo: son MTBVAC y VPM1002, ambas vacunas atenuadas.
La vacuna VPM1002 está siendo desarrollada por entidades alemanas (Instituto Max Planck y Vakzine Projekt Management GmbH, VPM), a las que se han unido Serum Institute of India y European and Development Clinical Trial Partnership (EDCTP) para la puesta en marcha del ensayo de fase 3 actualmente en marcha (NCT04351685). Los recién nacidos son la población diana principal ya que el objetivo es reemplazar a la BCG actual. VPM1002 está basada en la cepa de M. bovis de la BCG modificada genéticamente (introducción de listeriolisina -un gen de Listeria monocytogenes- y eliminación simultánea del gen de la ureasa C) para buscar un mejor reconocimiento por el sistema inmunológico. En junio de 2022 finalizó el reclutamiento de casi 7000 recién nacidos sanos de ambos sexos en Sudáfrica, Tanzania, Kenia, Uganda y Gabón. El estudio evaluará la eficacia y seguridad y comparará a recién nacidos expuestos y no expuestos al VIH vacunados con BCG o con VPM1002. Aún no se han publicado resultados intermedios.
[volver al principio]
La vacuna MTBVAC
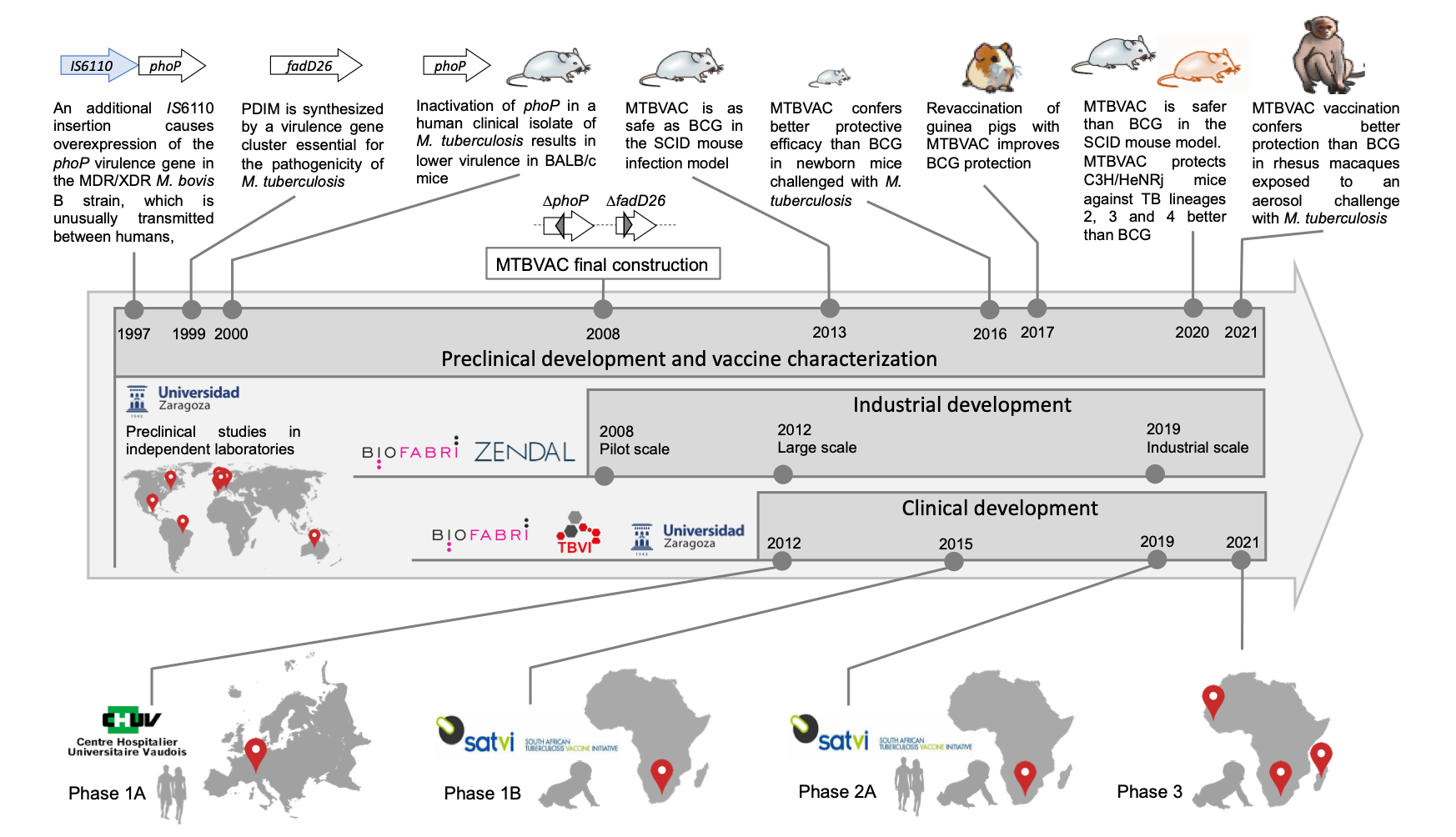
Es una vacuna atenuada preparada a partir de la cepa Mt103 de M. tuberculosis (linaje 4: europeo-africano-americano) obtenida a partir de una muestra clínica. Mediante ingeniería genética se le han retirado 2 genes relacionados con la virulencia de la bacteria: phoP y fadD26. Ha sido segura y eficaz en estudios preclínicos. Esta vacuna es la primera y única vacuna atenuada basada en M. tuberculosis que ha alcanzado la fase 3 de investigación en humanos. En las Jornadas de Vacunas de la AEP, celebradas en 2019, Carlos Martín Montañés presentó una ponencia sobre el desarrollo de MTBVAC y la situación y perspectiva en ese momento sobre las vacunas contra la TBC (Martín C, Vaccine 2021).
MTBVAC fue diseñada siguiendo los principios de Pasteur: aislamiento de un patógeno humano, atenuación mediante la inactivación de genes previamente seleccionados, protección demostrada en animales y evaluación en humanos. Una vez superados los estudios preclínicos, en 2013 comenzaron los estudios clínicos. Tras mostrar eficacia y seguridad suficientes en los estudios de fases 1 (Tameris M, Lancet Respir Med 2019, NCT02729571; Spertini F, Lancet Respir Med 2015, NCT02013245) y 2 (NCT03536117 y NCT02933281), recientemente se ha iniciado la fase 3 (Martín C, Vaccine 2021). Al final se muestran algunas de las referencias clave en el camino del desarrollo clínico de la vacuna MTBVAC.
Ensayo aleatorizado de fase 3
Esta nueva fase incluye bebés en Sudáfrica, Madagascar y Senegal (NCT04975178). El objetivo de esta etapa de los ensayos clínicos es comprobar directamente si la vacuna MTBVAC ofrece mejores resultados que la conocida vacuna BCG. Para ello, se vacunarán a 7120 recién nacidos de los tres países mencionados con cada una de las vacunas y se observará su evolución durante los siguientes 5 a 6 años. Tras este periodo, se podrá evaluar cuál de las dos ofrece una mayor protección comparando el número de casos de tuberculosis que se han producido en los dos grupos. El reclutamiento ha comenzado a finales de 2022, pero hay un factor que podría poner en peligro todo el esfuerzo realizado hasta ahora: la financiación. La fase 3 requiere, en este caso, más de 53 millones euros. El EDCTP cubre algo menos de la mitad. Queda, por tanto, pendiente una cantidad importante necesaria para completar el proceso.
Hace un año, la biofarmacéutica india Bharat Biotech se sumó al proyecto comprometiéndose a fabricar y distribuir la vacuna a más de 70 países africanos en caso de culminar con éxito los estudios en marcha, según han asegurado la Universidad de Zaragoza y la propia Bharat Biotech.
Comparativa con la BCG: efectos heterólogos de MTBVAC
El estándar hasta ahora en la protección con vacunas frente a la TBC es la BCG. Y una de las vertientes a comparar es la de los efectos heterólogos demostrados por la BCG. En la tabla adjunta se muestra una comparativa de ambas vacunas en este aspecto, mostrando que MTBVAC también mostraría efectos heterólogos de forma análoga a BCG (Martín C, Vaccine 2021).
Referencias bibliográficas clave
Algunas de las referencias bibliográficas más importantes en el camino de MTBVAC (por orden cronológico) son:
- Martín C, et al. MTBVAC, a live TB vaccine poised to initiate efficacy trials 100 years after BCG. Vaccine. 2021;39(50):7277-85.
- Tameris M, et al. Live-attenuated M. tuberculosis vaccine MTBVAC versus BCG in adults and neonates: a randomised controlled, double-blind dose-escalation trial. Lancet Respir Med. 2019;7(9):757-70.
- Gonzalo-Asensio J, et al. New insights into the transposition mechanisms of IS6110 and its dynamic distribution between Mycobacterium tuberculosis Complex lineages. PLoS Genet. 2018:14(4):e1007282.
- Aguilo N, et al. Reactogenicity to major tuberculosis antigens absent in BCG is linked to improve protection against Mycobacterium tuberculosis. Nat Commun. 2017;8:16085.
- Aguilo N, et al. Pulmonary but Not Subcutaneous Delivery of BCG Vaccine Confers Protection to Tuberculosis-Susceptible Mice by an Interleukin 17-Dependent Mechanism. J Infect Dis. 2016;213(5):832-9.
- Spertini F, et al. First Human Immunization with A Live-Attenuated Mycobacterium tuberculosis: a randomized, double-blind, controlled phase I trial. Lancet Respir Med. 2015;3(12):953-62.
- Arbues A, et al. Construction, characterization and preclinical evaluation of MTBVAC, the first live-attenuated M. tuberculosis-based vaccine to enter clinical trials. Vaccine. 2013;31(42):4867-73.
- Martin C, et al. The live Mycobacterium tuberculosis phoP mutant strain is more attenuated than BCG and confers protective immunity against tuberculosis in mice and guinea pigs. Vaccine. 2006;24(17):3408-19.
- Pérez E, et al. An essential role for phoP in M. tuberculosis virulence. Mol Microbiol. 2001;41(1):179-87.
- van Embden JD, et al. Strain identification of Mycobacterium-tuberculosis by DNA fingerprinting - recommendations for a standardized methodology. J Clin Microbiol. 1993;31(2):406-9.
- Martín C, et al.Transposition of an antibiotic-resistance element in mycobacteria. Nature. 1990;345(6277):739-43.
[volver al principio]
-oOo-
Más información en esta web
- CAV-AEP. Tuberculosis. BCG. Manual de inmunizaciones en línea de la AEP.
- CAV-AEP, 27 de marzo de 2023. Historia de las inmunizaciones en el Manual de inmunizaciones en línea de la AEP.
- CAV-AEP, 13 de abril de 2020. La vacuna MTBVAC contra la tuberculosis muestra efectos heterólogos en modelos animales.
- CAV-AEP, 25 de marzo de 2019. Día Mundial de la Tuberculosis, se abre paso una nueva vacuna de investigación española.
- CAV-AEP. Noticias sobre la tuberculosis y sus vacunas.
Referencias bibliográficas
- Bharat Biotech, Biofabri tie up to develop, make, distribute TB vaccine ‘MTBVAC’. Partnership would guarantee the supply of TB vaccines in more than 70 countries. The Tribune of India, 16 de marzo de 2022.
- CDC, 24 de marzo de 2023. World TB Day.
- Corral Ó, et al. El laboratorio donde nace una vacuna para la tuberculosis. El País, 24 de marzo de 2022.
- Hierro L, et al. El remedio a la enfermedad infecciosa más mortal se investiga en un pueblo de Galicia. El País, 24 de marzo de 2022.
- Infosalud, 22 de marzo de 2023. La vacuna 'española' contra la tuberculosis inicia su fase 3 en más de 7000 niños en tres países africanos.
- Martín Montañés C, 25 de marzo de 2023. Hilo en Twitter sobre el inicio de la fase 3 con la vacuna MTBVAC.
- Martín C, et al. MTBVAC, a live TB vaccine poised to initiate efficacy trials 100 years after BCG. Vaccine. 2021;39(50):7277-85.
- OMS. Tuberculosis.
- OMS, 24 de marzo de 2023. World Tuberculosis Day 2023.
- MTBVAC. T.END.
- TuBerculosis Vaccine Initiative (TBVI).
- Universidad de Zaragoza, 16 de marzo de 2022. La biofarmacéutica española Biofabri y la india Bharat Biotech firman un acuerdo para desarrollar, fabricar y distribuir la vacuna contra la tuberculosis, MTBVAC.
Otras referencias
- Lacámara S, et al. MTBVAC: A Tuberculosis Vaccine Candidate Advancing Towards Clinical Efficacy Trials in TB Prevention. Arch Bronconeumol. 2023;59(12):821-8.
- Martín C. La hora de la verdad para las vacunas contra la tuberculosis. Aunque el tratamiento de esta enfermedad ha mejorado significativamente, la falta de inversión en el desarrollo de nuevas inmunizaciones sigue siendo el principal obstáculo para detener esta epidemia silenciosa. El País, 7 de julio de 2023.
- Pichel J. La vacuna española de la tuberculosis la paga Alemania: "Necesitamos apoyo aquí". MTBVAC, desarrollada en la Universidad de Zaragoza, está en ensayos clínicos en fase 3 y podría ser la primera vacuna para la enfermedad infecciosa más mortal en 100 años. El Confidencial, 20 de julio de 2023.
[volver al principio]