Vacunas del COVID-19 en estudio con datos publicados
El ruido en torno a las vacunas de la COVID-19 es considerable; a las declaraciones (y supuestas presiones) de las máximas autoridades políticas de algunos de los países que lideran la investigación y la rivalidad y competencia entre las empresas implicadas en la eventual fabricación posterior de un producto de elevado valor comercial, se suma el gran interés de los medios de comunicación y de la propia población.
Las expectativas levantadas son muy altas, sin duda demasiadas para la necesaria prudencia que pide la realidad de enfrentar un reto de dimensiones extraordinarias, como es el desarrollo de una nueva vacuna segura y eficaz que, aplicada con carácter amplio, pudiera cambiar el rumbo de la pandemia de COVID-19 y revertir o paliar sus efectos.
A continuación se muestra el estado de la cuestión de forma esquemática: productos en investigación, estudios en marcha y datos publicados.
Productos candidatos a vacuna del COVID-19 en investigación
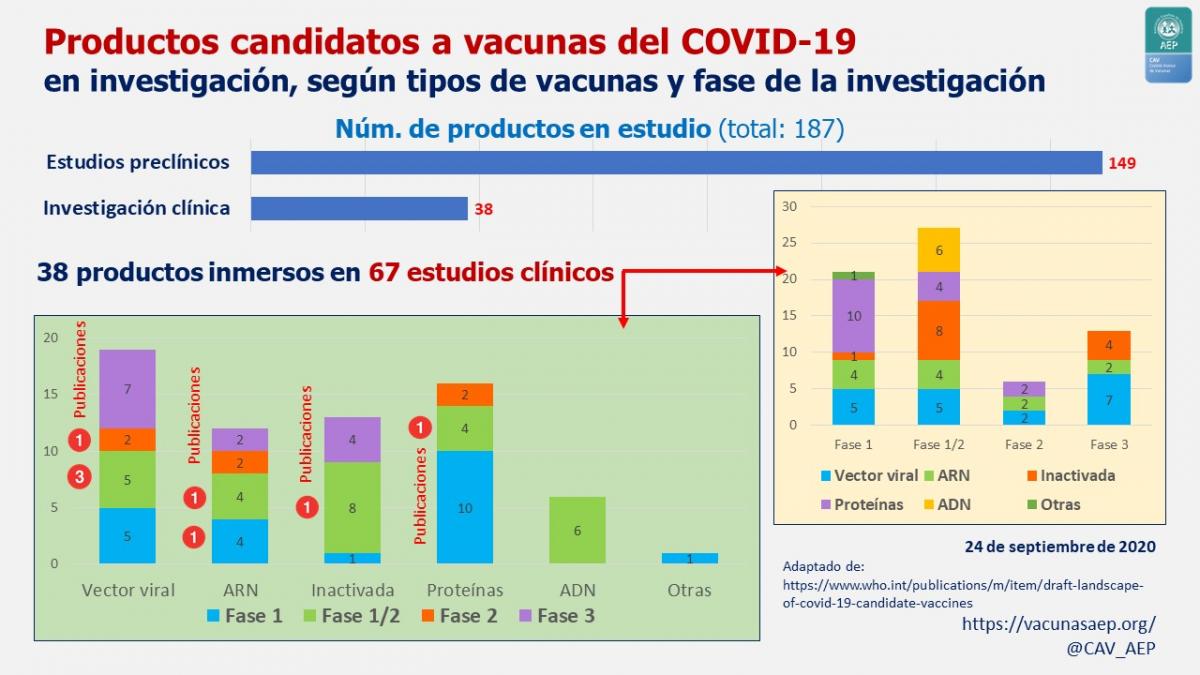
Según la OMS, con fecha 25 de septiembre de 2020, un total de 187 productos se encuentran en investigación. De ellos, 149 en investigación preclínica y otros 38 ya inmersos en estudios clínicos, que implican la participación voluntaria de un limitado, aunque variable, número de personas.
Los 38 productos en investigación clínica están implicados en un total de 67 estudios registrados: 21 en fase 1, 27 en fase 1/2, 6 en fase 2 y, finalmente, 13 en fase 3. Desde la perspectiva del tipo de productos: 17 estudios con vacunas de vectores virales (de ellos 15, vectores virales no replicantes), 18 estudios con vacunas de ARN/ADN, 16 con vacunas de subunidades proteicas y 13 más con vacunas de viriones inactivados (ver imagen adjunta).
Datos publicados hasta el momento
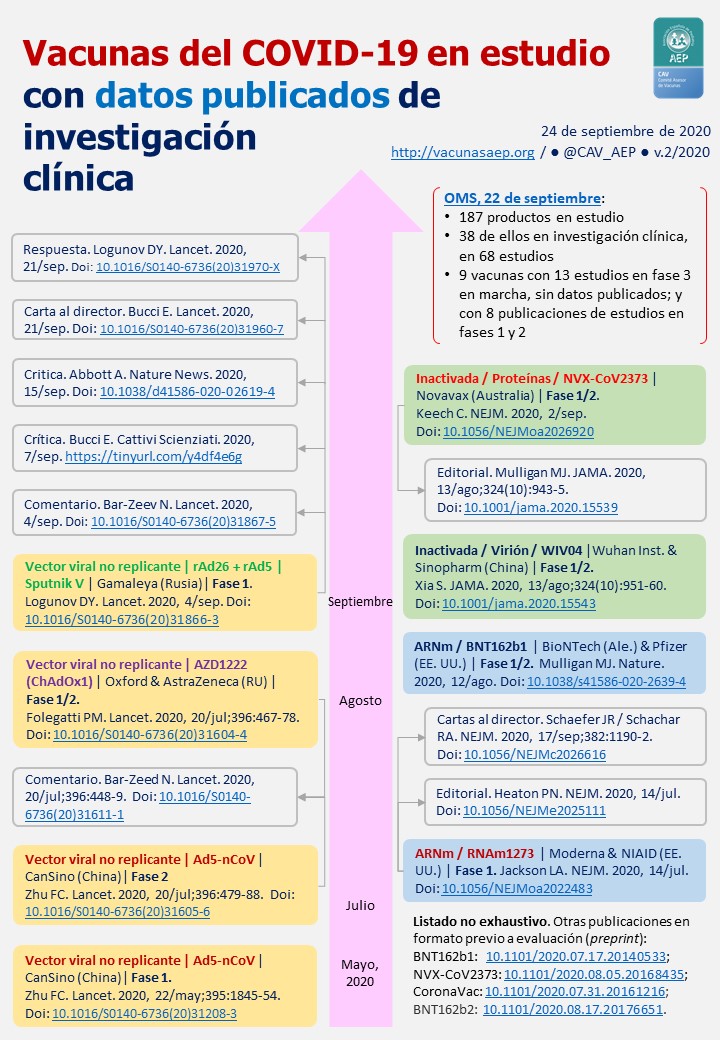
Los estudios en marcha que han mostrado resultados en publicaciones de alto nivel de confianza se muestran en la tabla adjunta; son 8 publicaciones originales, dos editoriales y ocho más del tipo de comentarios y cartas al director a proposito de los trabajos originales. Es lo que hay, mucho desde el punto de vista de donde nos encontrábamos hace pocos meses, pero no tanto mirándolo desde el punto de vista de las elevadas expectativas levantadas y el ruido mediático.
Además están disponibles, al menos, otras cuatro publicaciones en formato previo a la revisión por pares (preprint):
- [BNT162b1] Sahin U, et al. Concurrent human antibody and TH1 type T-cell responses elicited by a COVID-19 RNA vaccine. MedRxiv. 2020, 20/jul. doi: 10.1101/2020.07.17.20140533.
- [NVX-CoV2373] Keech C, et al. First-in-Human Trial of a SARS CoV 2 Recombinant Spike Protein Nanoparticle Vaccine. MedRxiv. 2020, 6/ago. doi: 10.1101/2020.08.05.20168435.
- [CoronaVac] Zhang YS, et al. Immunogenicity and Safety of a SARS-CoV-2 Inactivated Vaccine in Healthy Adults Aged 18-59 years: Report of the Randomized, Double-blind, and Placebo-controlled Phase 2 Clinical Trial. MedRxiv. 2020, 10/ago. doi: 10.1101/2020.07.31.20161216.
- [BNT162b2] Walsh EE, et al. RNA-Based COVID-19 Vaccine BNT162b2 Selected for a Pivotal Efficacy Study. MedRxiv. 2020, 28/ago. doi: 10.1101/2020.08.17.20176651.
Adenda, 26 de septiembre de 2020: las empresas promotoras de cuatro de los principales candidatos a vacunas del COVID-19 han publicado los protocolos de los estudios en fase 3 en marcha, lo que no es habitual, empujados por la necesidad de preservar la confianza de la comunidad científica y de la población, tras el compromiso adquirido previamente según el cual solo solicitarían la aprobación para sus productos si cuentan con suficientes datos sobre la seguridad y la eficacia en los estudios en curso, en respuesta a las presiones para acelerar los procesos sin el debido rigor y a las preocupaciones despertadas por ello:
- Janssen, Ad26.CoV2.S, 15 de septiembre de 2020.
- Moderna, mRNA-1273, 20 de agosto de 2020.
- Pfizer & BioNTech, BNT162, septiembre de 2020.
- AstraZeneca & Oxford, AZD1222, 17 de septiembre de 2020.
Comentarios sobre la cuestión en: Nature, 25 de septiembre; Science, 21 de septiembre; Medscape, 22 de septiembre; Forbes, 23 de septiembre; The New York Times, 19 de septiembre. BMJ. 2020;371:m4058.
-oOo-
Más información:
- Poland GA, et al. SARS-CoV-2 immunity: review and applications to phase 3 vaccine candidates. Lancet. 2020;396(10262):1595-606.
- Krammer F. SARS-CoV-2 vaccines in development. Nature. 2020;586:516-27.
- The Medical Letter, 22 de septiembre de 2020. Treatments Considered for COVID-19 (págs. 88-93).
- CAV, 20 de agosto de 2020. Vacunas de la COVID-19: hasta ahora resultados predecibles, lo cual es una buena noticia.
- Otras noticias anteriores sobre el nuevo coronavirus en esta web.