CAV-AEP
| Contenido |
|---|
| Introducción [ver [2]] ● Sarampión [ver [3]] ● Vacunación frente al sarampión [ver [4]] ● Respuesta de la Ponencia de Programa y Registro de Vacunaciones y la Comisión de Salud Pública del CISNS a la propuesta del CAV-AEP [ver [5]] ● Recomendación del CAV-AEP (4 de mayo de 2022) [ver [6]] ● Referencias bibliográficas [ver [7]] |
-oOo-
Recomendación del CAV-AEP
La vacuna triple vírica administrada, en circunstancias especiales, entre los 11 y los 12 meses de edad es válida a efectos del calendario vacunal infantil.
- La pauta de vacunación estándar frente al sarampión, rubeola y parotiditis permanece sin cambios: la primera dosis con vacuna triple vírica debe administrarse tan pronto como sea posible tras cumplir 12 meses; la segunda, con vacuna triple o cuádruple vírica, a los 3-4 años.
- Pero si, por circunstancias extraordinarias, se administra entre los 11 y los 12 meses de edad puede considerarse válida a los efectos del cumplimiento del calendario vacunal infantil.
9 de mayo de 2022
[volver al inicio [8]]
Introducción
En enero de 2022 el CAV-AEP se dirigió al Área de Programas de Vacunación de la Subdirección General de Promoción de la Salud y Vigilancia en Salud Pública (Dirección General de Salud Pública, Calidad e Innovación, Ministerio de Sanidad) con una propuesta razonada destinada a la Ponencia de Programas y Registros de Vacunaciones (la Ponencia en adelante) y la Comisión de Salud Pública (CSP, Consejo Interterritorial del Sistema Nacional de Salud, CISNS) para modificar el criterio de considerar no válida a efectos del cumplimiento del calendario vacunal la administración de la vacuna triple vírica en lactantes de entre 11 y 12 meses de edad. La propuesta se basaba en las consideraciones expuestas a continuación.
A finales del mes de abril se ha recibido la respuesta indicando que la Ponencia y la Comisión de Salud Pública del CISNS han aceptado la propuesta, incorporando así el criterio mencionado entre las especificaciones del calendario vacunal para toda la vida.
[volver al inicio [8]]
Sarampión
Algunos aspectos destacados del sarampión1,2:
- El sarampión es una enfermedad altamente contagiosa, potencialmente fatal, pero prevenible con una vacuna muy efectiva y segura.
- Los síntomas incluyen fiebre, erupción maculopapular y, al menos, uno de los siguientes: tos, coriza o conjuntivitis, aunque las personas vacunadas pueden tener síntomas más leves o incluso ningún síntoma.
- El diagnóstico de laboratorio se basa en la detección de anticuerpos IgM específicos en suero, gotas de sangre seca o fluido oral, o la detección de ARN viral en frotis faríngeo o nasofaríngeo, orina o fluido oral.
- Las complicaciones pueden afectar a muchos órganos y, a menudo, incluyen otitis media, laringotraqueobronquitis, neumonía, estomatitis y diarrea. Las complicaciones neurológicas son poco comunes, pero graves y pueden ocurrir durante o poco después de la enfermedad aguda (p. ej., encefalomielitis aguda diseminada) o meses o incluso años después (p. ej., encefalitis por cuerpos de inclusión y panencefalitis esclerosante subaguda).
- El manejo del paciente implica principalmente terapia de apoyo, como suplementos de vitamina A, vigilancia y tratamiento de infecciones bacterianas secundarias y rehidratación en caso de diarrea grave.
- No existe una terapia antiviral específica para el sarampión y el control de la enfermedad depende en gran medida de la prevención. Sin embargo, a pesar de la disponibilidad de una vacuna segura y eficaz, el sarampión sigue siendo endémico en muchos países y causa una morbilidad y mortalidad considerables, especialmente entre los niños en países de escasos recursos.
- El bajo número de casos notificados en 2020 y 2021, después de un resurgimiento mundial del sarampión entre 2017 y 2019, debe interpretarse con cautela debido al efecto de la pandemia de COVID-19 en la vigilancia de la enfermedad.
[volver al inicio [8]]
Vacunación frente al sarampión
Los calendarios de vacunación infantil (calendario de vacunación a lo largo de toda la vida del CISNS3, los calendarios de las comunidades y ciudades autónomas4 y el calendario vacunal del CAV-AEP5) contemplan la vacunación frente al sarampión con pauta de dos dosis, la primera a los 12 meses de edad con vacuna triple vírica y la segunda a los 3-4 años de edad con vacuna triple o tetravírica. En España se mantienen coberturas vacunales buenas desde hace más de una década; en 2020, primer año de pandemia, 96,3 % para la primera dosis (cohorte de 2018), aunque solo 93,9 % para la segunda (cohorte de 2015)6.
En algunos países europeos, la primera dosis se administra antes de los 12 meses de edad7: Alemania (11-14 meses), Austria (10-13 meses), Eslovenia (11-18 meses) y Suiza (9 meses)8. En el resto, la primera dosis se administra entre los 12 y 18 meses. En Reino Unido9, se aplica a los 12 meses, y en Canadá10 y EE. UU.11 a los 12-15 meses.
Aparte del debate, en el plano académico, sobre la necesidad de adelantar o no la primera dosis frente al sarampión, en la práctica vacunal son relativamente frecuentes las dudas referidas a tres situaciones: 1) la administración por error de la primera dosis de vacuna triple vírica poco antes de cumplir los 12 meses y la contabilización de dicha dosis; 2) la adaptación del calendario de niños procedentes de países donde administran la primera dosis antes de los 12 meses; y 3) la necesidad de administrar una dosis de vacuna triple vírica en lactantes de menos de 12 meses de edad que van a emprender un viaje internacional con estancia en países con alto riesgo de transmisión de sarampión.
Mientras que la mayoría de los países que administran la primera dosis una vez cumplidos los 12 meses, se decantan por no contabilizar cualquier dosis puesta antes de la edad citada (como en España, hasta ahora12), algún otro, como Australia13, admiten como válida la primera dosis administrada entre los 11 y 12 meses de edad. La OMS, en su position paper de 201714, indica que las vacunas administradas antes de los 9 meses de edad no deben ser contabilizadas a los efectos de la inmunización del sarampión.
En España la recomendación actual de los servicios de salud y de este comité, hasta ahora, es que cualquier dosis de esta vacuna administrada antes de cumplir los 12 meses no debe ser contabilizada a los efectos del calendario vacunal, y se deben administrar dos dosis de dicha vacuna una vez cumplidos los 12 meses, con el intervalo mínimo entre dosis de un mes. La razón aducida ha sido que la persistencia de los anticuerpos antisarampión recibidos de la madre a través de la placenta en los últimos meses de la gestación, especialmente en madres que habían pasado la infección natural, podría comprometer la respuesta inmunológica a la vacunación del lactante menor de un año con la vacuna triple vírica.
Sin duda, el argumento expuesto ha quedado superado y no puede mantenerse en la actualidad. Después de numerosos años con elevadas coberturas vacunales en nuestro entorno, la gran mayoría de las mujeres en edad fértil están vacunadas y, como consecuencia de la vacunación infantil sistemática, la incidencia de la infección natural se ha reducido de forma muy importante. Además, se ha comprobado, mediante estudios propios15 y de otros países de nuestro entorno16-20, que la persistencia de anticuerpos antisarampión en el suero de los lactantes nacidos de madres vacunadas es menor que en los hijos de madres que han pasado la enfermedad natural, antes de la extensión de la vacunación. De este hecho se derivan dos consecuencias: por una parte, reconocer que los lactantes tienen una mayor susceptibilidad al sarampión antes de iniciar la vacunación, y, por la otra, que habría un menor riesgo de interferencia sobre la inmunogenicidad de la vacuna atenuada administrada en el segundo semestre del primer año de vida. Y, efectivamente, varios estudios han demostrado que la vacunación entre los 6 y 12 meses de edad es suficientemente inmunógena y segura21-23 en nuestro medio.
Por lo tanto, para asegurar la protección insuficiente de los lactantes antes de cumplir los 12 meses se podría valorar la necesidad de un adelanto de la primera dosis del calendario. Este es un debate abierto desde hace algunos años en países que mantienen una elevada cobertura vacunal24 porque es una medida que, si bien podría cubrir la brecha mencionada, también podría tener inconvenientes.
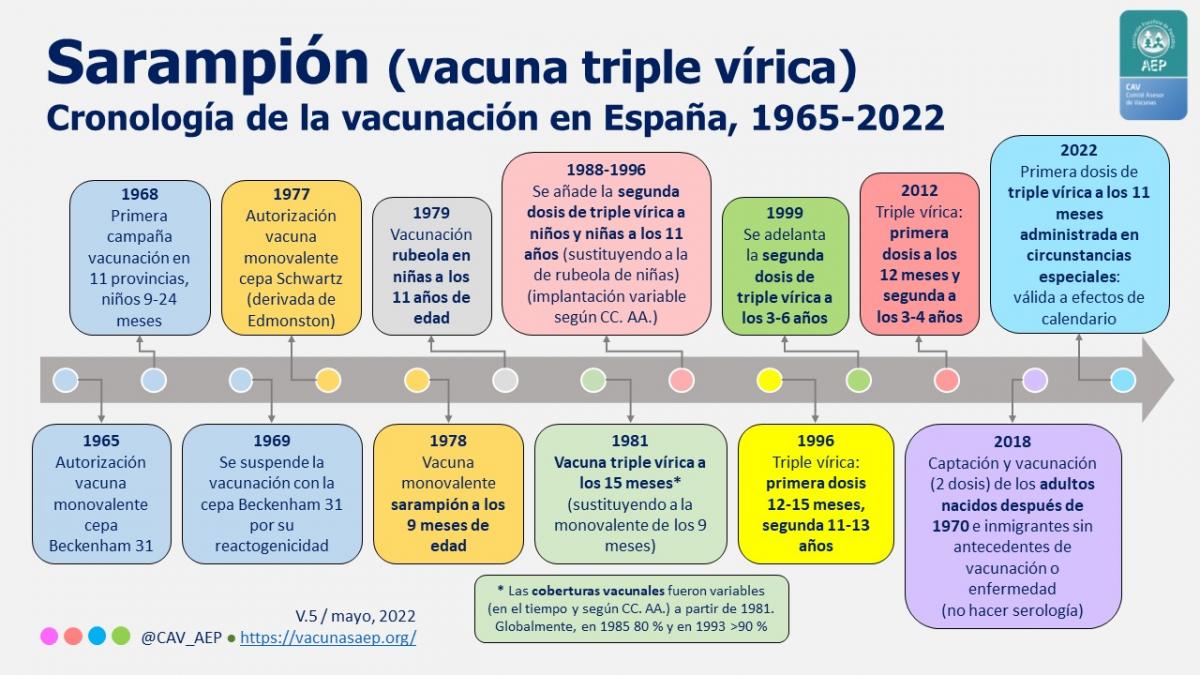
En España desde 1996 la primera dosis se administraba en el periodo de 12-15 meses de edad (ver imagen adjunta). En 2012 se fijó en los 12 meses por las mismas razones que, ahora, empujan a evaluar un nuevo adelanto en esta vacunación. Sin embargo, desde entonces se ha comprobado a través de los estudios poblacionales de seroprevalencia que, con el transcurso de los años, hay un descenso progresivo de la proporción de seropositivos en adultos jóvenes, comprometiendo, de esta forma, la protección vacunal a largo plazo22,23,25,26. Esta circunstancia obliga a enmarcar el debate de la edad de la primera dosis en otro más amplio cuyo objetivo sea el de evaluar la estrategia global de mantenimiento del estatus de eliminación del sarampión, cubriendo también la mayor susceptibilidad de los extremos de la línea de edad, desde los lactantes hasta la edad avanzada, pasando por la edad media de la vida, período en el que se concentra actualmente la mayor susceptibilidad.
El último estudio español de seroprevalencia, publicado por el Ministerio de Sanidad en enero de 2021 y correspondiente a muestras poblacionales obtenidas en 2017-2018 en personas de 2-80 años de edad (2-49 años en el caso del sarampión)27, muestra un descenso de la población con títulos de anticuerpos protectores a partir del grupo de edad de 10-15 años hasta los 30-39 años (cohortes nacidas entre 1978 y 2002), siendo más pronunciado en el grupo de 20-29 años de edad (nacidos entre 1988 y 1997), que puede deberse a la pérdida de protección serológica a medida que pasa el tiempo desde la vacunación con la segunda dosis de vacuna triple vírica (3-4 años de edad), posiblemente por la ausencia de contactos con el virus salvaje28.
En 2019, con datos del Centro Nacional de Epidemiología (CNE)29, en España se confirmaron 287 casos de sarampión: de ellos el 39,7 % en personas ≥20 años de edad, y el 11,1 % (n=32) en las de <12 meses de edad, siendo este último grupo de edad el que mayor tasa de incidencia presenta (8,97/100 000). En 2020, según la misma fuente30, fueron 90 casos confirmados, de ellos solo 7 (7,8 %) en menores de 12 meses, y la gran mayoría en adultos no vacunados y en el primer trimestre del año. En este informe ya se advierte de la distorsión de la pandemia del SARS-CoV-2 que irrumpió al comienzo del año.
En el momento actual, mayo de 2022, dominado aún por los efectos a todos los niveles de la pandemia de covid causada por el SARS-CoV-2, tanto la incidencia del sarampión como las coberturas vacunales no han quedado fuera de su poder transformador. Hemos asistido a una extraordinaria reducción de la detección de nuevos casos31 (aunque las cifras pueden subestimar la realidad, por la distorsión de las funciones de sospecha y detección de casos en el nivel asistencial y del funcionamiento de la cadena de vigilancia epidemiológica) y una reducción de las coberturas vacunales en los primeros meses de 202032 que se han recuperado en parte finalmente en nuestro medio6. En 2020, el Centro Nacional de Epidemiología registró un total de 90 casos30, en 2021 solo dos33 y en 2022 hasta el momento ninguno34, llevando al extremo la tendencia señalada a mediados de 202031.
A nivel global, los efectos de la pandemia son extraordinarios, comprometiendo la salud de millones de niños, por la demora o suspensión de las vacunaciones, y con ello, los objetivos marcados en las estrategias de eliminación y erradicación del sarampión en el mundo35. En los primeros dos meses de 2022 se ha advertido del aumento de los casos del 79 % respecto a 2021 a nivel global, lo que señala un cambio de tendencia una vez que la relajación de las medidas de restricción social impuestas por la pandemia deja al descubierto la mayor vulnerabilidad de amplias poblaciones36.
[volver al inicio [8]]
Respuesta de la Ponencia de Programa y Registro de Vacunaciones y la Comisión de Salud Pública del CISNS a la propuesta del CAV-AEP

El 29 de abril de 2022 las responsables del Área de Programas de Vacunación de la Subdirección General de Promoción de la Salud y Vigilancia en Salud Pública (Dirección General de Salud Pública, Calidad e Innovación, Ministerio de Sanidad) han comunicado que tanto la Ponencia como la CSP han aprobado la propuesta del CAV-AEP, siendo la redacción final del acuerdo tal como se muestra a continuación.
El CAV-AEP se congratula de la oportunidad de colaboración con la Ponencia y la CSP, del debate técnico y del acuerdo final.
[volver al inicio [8]]
Recomendación del CAV-AEP (4 de mayo de 2022)
 [9]Teniendo en cuenta los argumentos expuestos y la aprobación de la Ponencia y la CSP del CISNS, puede llevarse a cabo un cambio en la recomendación actual, en el siguiente sentido.
[9]Teniendo en cuenta los argumentos expuestos y la aprobación de la Ponencia y la CSP del CISNS, puede llevarse a cabo un cambio en la recomendación actual, en el siguiente sentido.
Cuando se ha administrado una dosis de vacuna triple vírica entre los 11 y los 12 meses de edad, en circunstancias especiales (bien de forma inadvertida -por error-, por proceder de un país donde la primera dosis se administra a los 11 meses o bien por la proximidad de un viaje a un país con circulación activa del sarampión), puede contabilizarse dicha dosis como válida a los efectos del calendario vacunal estándar.
- La vacuna del sarampión (triple vírica) puede administrarse en situaciones extraordinarias (por ej. viajes a países endémicos o con elevado riesgo de exposición), atendiendo a las recomendaciones de los servicios de salud pública, a partir de los 6 meses de edad. Cuando se administra entre los 6 y los 10 meses (hasta el día anterior a cumplir los 11 meses), no debe contabilizarse a los efectos del calendario vacunal, y se deben administrar dos dosis siguiendo la pauta habitual a partir de los 12 meses.
- Cuando se administra la vacuna triple vírica una vez cumplidos los 11 meses de edad y antes de cumplir los 12 meses, debe considerarse válida y contabilizarse dicha dosis a los efectos del calendario vacunal, siguiendo después con la segunda dosis a los 3-4 años de edad.
Debe recordarse, sin embargo, que se mantiene la recomendación de que la primera dosis de vacuna triple vírica se administre de forma rutinaria tan pronto como sea posible una vez cumplidos los 12 meses de edad 3,5.
[volver al inicio [8]]
-oOo-
 [10]Referencias bibliográficas
[10]Referencias bibliográficas
- Strebel PM, et al. Measles. N Engl J Med. 2019;381:349-57 [11].
- Hübschen JM, et al. Measles. Lancet. 2022;399(10325):678-90 [12].
- Ministerio de Sanidad. Calendario vacunal de toda la vida, 2022 [13] (consultado el 4 de mayo de 2022).
- AEPap. Calendarios vacunales españoles [14] (consultado el 14 de enero de 2022).
- AEP. Calendario vacunal de la AEP, 2022 [15] (consultado el 14 de enero de 2022).
- Ministerio de Sanidad. Coberturas de vacunación de primera y segunda dosis de triple vírica. Año 2020 [16] (consultado el 4 de mayo de 2022).
- ECDC. Vaccine Scheduler. Measles: Recommended vaccinations [17] (consultado el 4 de mayo de 2022).
- Bundesamt für Gesundheit BAG. Masern [18] (consultado el 3/may de 2022).
- UK Health Security Agency, 10 de julio de 2020. Guidance. Routine childhood immunisation schedule. Information for health professionals on childhood immunisations [19] (consultado el 14 de enero de 2022).
- Canadian Immunization Guide. Measles vaccine, septiembre de 2020 [20] (consultado el 14 de enero de 2022).
- CDC. Immunization schedules. Table 1. Recommended Child and Adolescent Immunization Schedule for ages 18 years or younger, United States, 2021 [21] (consultado el 14 de enero de 2022).
- Ministerio de Sanidad. Consejo Interterritorial del Sistema Nacional de Salud, enero de 2021. Plan estratégico para la eliminación del sarampión y la rubeola en España [22].
- Australian Immunisation Handbook. Table. Minimum acceptable age for the 1st dose of scheduled vaccines in infants [23] (actualizado el 27 de septiembre de 2021) (consultado el 4 de mayo de 2022).
- WHO. Measles vaccination, position paper, 2017 [24].
- Cilleruelo MJ, et al. Duration of immunity to measles, rubella and mumps during the first year of life. Vaccine. 2019;37(30):4164-71 [25].
- Leuridan E, et al. Passive transmission and persistence of naturally acquired or vaccine-induced maternal antibodies against measles in newborns. Vaccine. 2007;25:6296-304 [26].
- Leuridan E, et al. Early waning of maternal measles antibodies in era of measles elimination: longitudinal study. BMJ. 2010;340:c1626 [27].
- Waaijenborg S, et al. Waning of Maternal Antibodies Against Measles, Mumps, Rubella, and Varicella in Communities With Contrasting Vaccination Coverage. J Infect Dis. 2013;208(1):10-6 [28].
- Guerra FM, et al. Waning of measles maternal antibody in infants in measles elimination settings – A systematic literature review. Vaccine. 2018;1248-55 [29].
- Kanakoudi-Tsakalidou F, et al. Humoral Immunity against Measles in Mother-Infant Pairs during the First Year of Life in Greece: A Cross-Sectional Study. Vaccines (Basel). 2021;9(2):143 [30].
- Lochlainn LMN, et al. Effect of measles vaccination in infants younger than 9 months on the immune response to subsequent measles vaccine doses: a systematic review and meta-analysis. Lancet Infect Dis. 2019;19(11):1246-1254 [31].
- Brinkman ID, et al. Early Measles Vaccination During an Outbreak in the Netherlands: Short-Term and Long-Term Decreases in Antibody Responses Among Children Vaccinated Before 12 Months of Age. J Infect Dis. 2019;220:594-602 [32].
- Xu J, et al. Effect of early measles vaccination on long-term protection: A systematic review. Vaccine. 2021;39(22):2929-37 [33].
- Norwegian Institute of Public Health, 22 de octubre de 2021. When is there a need to bring forward MMR vaccination? [34] (consultado el 14 de enero de 2022).
- Bitzegeio J, et al. Estimating age-specific vaccine effectiveness using data from a large measles outbreak in Berlin, Germany, 2014/15: evidence for waning immunity. Euro Surveill. 2019;24(17):1800529 [35].
- Huges SL, et al. The effect of time since measles vaccination and age at first dose on measles vaccine effectiveness – A systematic review. Vaccine. 2020;38:460-9 [36].
- Ministerio de Sanidad. Segundo estudio de seroprevalencia en España, 2020 [37] (consultado el 14 de enero de 2022).
- CAV-AEP, 28 de marzo de 2021. Estudio de seroprevalencia de España. Parte 1: sarampión, rubeola y parotiditis [38] (consultado el 14 de enero de 2022).
- Centro Nacional de Epidemiología, Red Nacional de Vigilancia Epidemiológica (RENAVE). Plan de Eliminación del Sarampión y la Rubeola en España. Informe anual 2019 [39] (consultado el 14 de enero de 2022).
- Centro Nacional de Epidemiología, Red Nacional de Vigilancia Epidemiológica (RENAVE). Laboratorio Nacional de Referencia de Sarampión y Rubeola del Centro Nacional de Microbiología (CNM). Informe preliminar de casos y brotes sarampión y la rubeola notificados en España, año 2020 [40] (actualizado el 11 de febrero de 2021) (consultado el 14 de enero de 2022).
- CAV-AEP, 27 de julio de 2020. Cae la detección de casos de sarampión en España [41] (consultado el 14 de enero de 2022).
- CAV-AEP, 24 de abril de 2020. Otros efectos de la pandemia de COVID-19: caída de las vacunaciones [42] (consultado el 14 de enero de 2022).
- Centro Nacional de Epidemiología. Red Nacional de Vigilancia Epidemiológica (RENAVE). Boletín epidemiológico semanal en red, núm. 52, 2021 [43].
- Centro Nacional de Epidemiología. Red Nacional de Vigilancia Epidemiológica (RENAVE). Boletín epidemiológico semanal en red, núm. 18, 2022 [44].
- OMS, 10 de noviembre de 2021. Global progress against measles threatened amidst COVID-19 pandemic. The largest increase in unvaccinated children in 20 years and critical gaps in disease surveillance increase risk of measles outbreaks, putting lives at risk: WHO, CDC [45] (consultado el 14 de enero de 2022).
- UNICEF, OMS, 27/abr de 2022. UNICEF and WHO warn of ‘perfect storm’ of conditions for measles outbreaks, affecting children [46].
[volver al inicio [8]]