Efectividad de Comirnaty en un estudio poblacional
Efectividad vacunal de Comirnaty en un entorno no controlado
Ayer 24 de febrero de 2021 se han publicado los primeros resultados de efectividad de un programa vacunal frente a la covid a escala nacional, en este caso con la vacuna BNT162b2 (Comirnaty):
- Dagan N, et al. BNT162b2 mRNA Covid-19 Vaccine in a Nationwide Mass Vaccination Setting. N Engl J Med. 2021, 24/feb. DOI: 10.1056/NEJMoa2101765.
Métodos
Estudio observacional, llevado a cabo en Israel. Se incluyeron las personas vacunadas entre el 20/dic de 2020 y el 1/feb de 2021, emparejadas con controles en proporción 1:1 según características demográficas y clínicas. De un total de un millón y medio de personas vacunadas, se incluyeron un total de 596.618 personas con sus correspondientes controles. Variables estudiadas:
- Infección documentada por SARS-CoV-2.
- Covid sintomática.
- Hospitalización por covid.
- Covid grave.
- Muerte.
Resultados
- Durante un periodo medio de 15 días se documentaron 10.561 infecciones (0,6/1000 personas/día), de las cuales 5996 (57 %) fueron sintomáticas, 369 necesitaron hospitalización y 229 fueron graves.
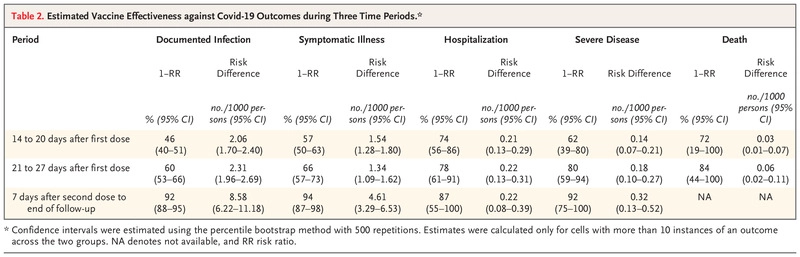
- Se calculó la efectividad vacunal en los siguientes periodos de tiempo: entre los días 14 y 20 tras la primera dosis; entre los 21 y 27 después de la primera dosis; y después de 7 o más días desde la segunda dosis. Los resultados obtenidos se muestran en la siguiente tabla.
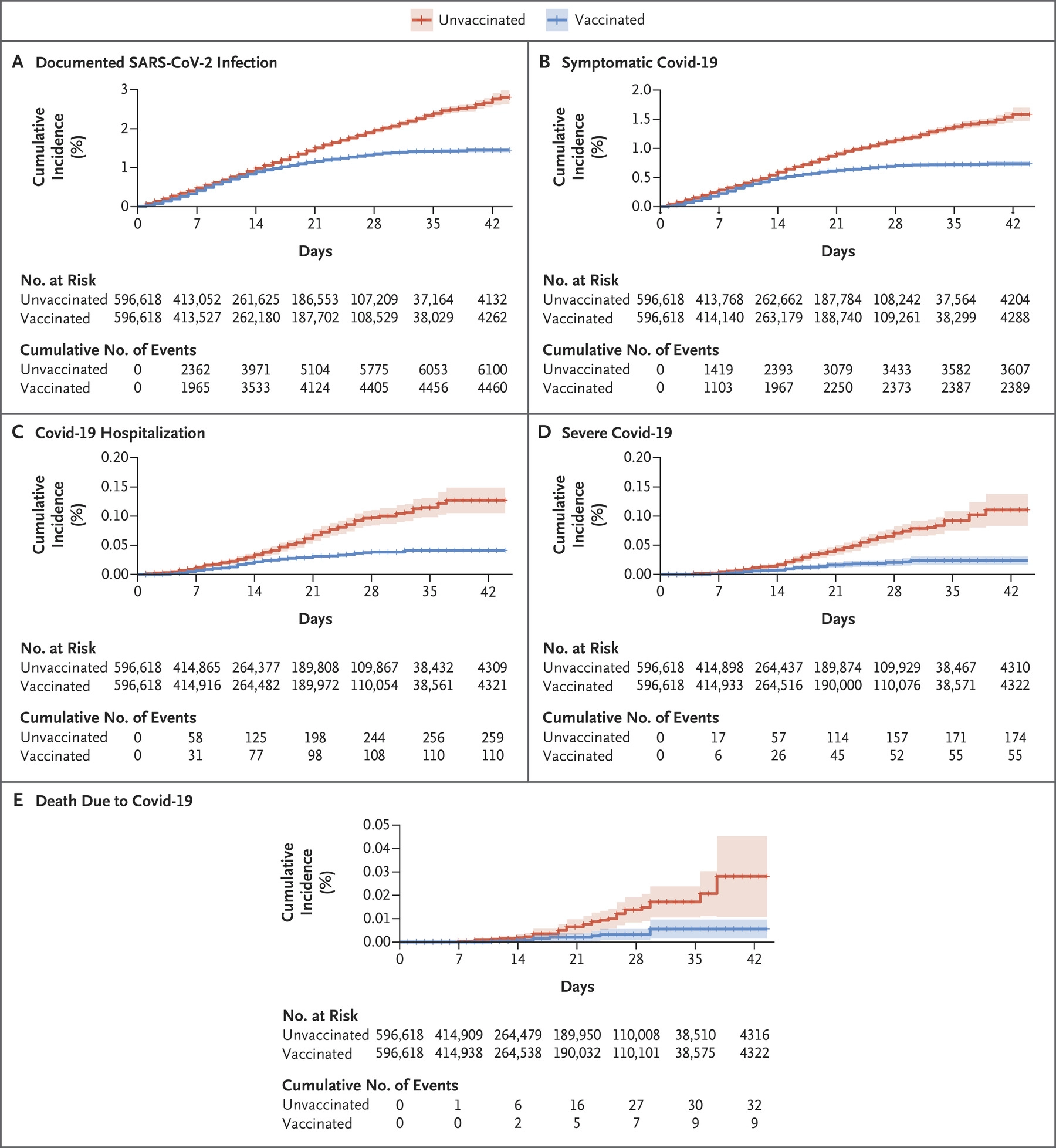
- Las curvas de incidencia acumulada según los resultados citados antes se muestran en la figura de arriba.
- En el período de seguimiento que comienza 7 días después de la segunda dosis, la efectividad de la vacuna para infecciones documentadas, enfermedad sintomática, hospitalización y enfermedad grave fue del 92 % (IC 95 %: 88 a 95), 94 % (IC 95 %: 87 a 98), 87 % (IC 95 %: 55 a 100) y 92 % (IC 95 %: 75 a 100), respectivamente.
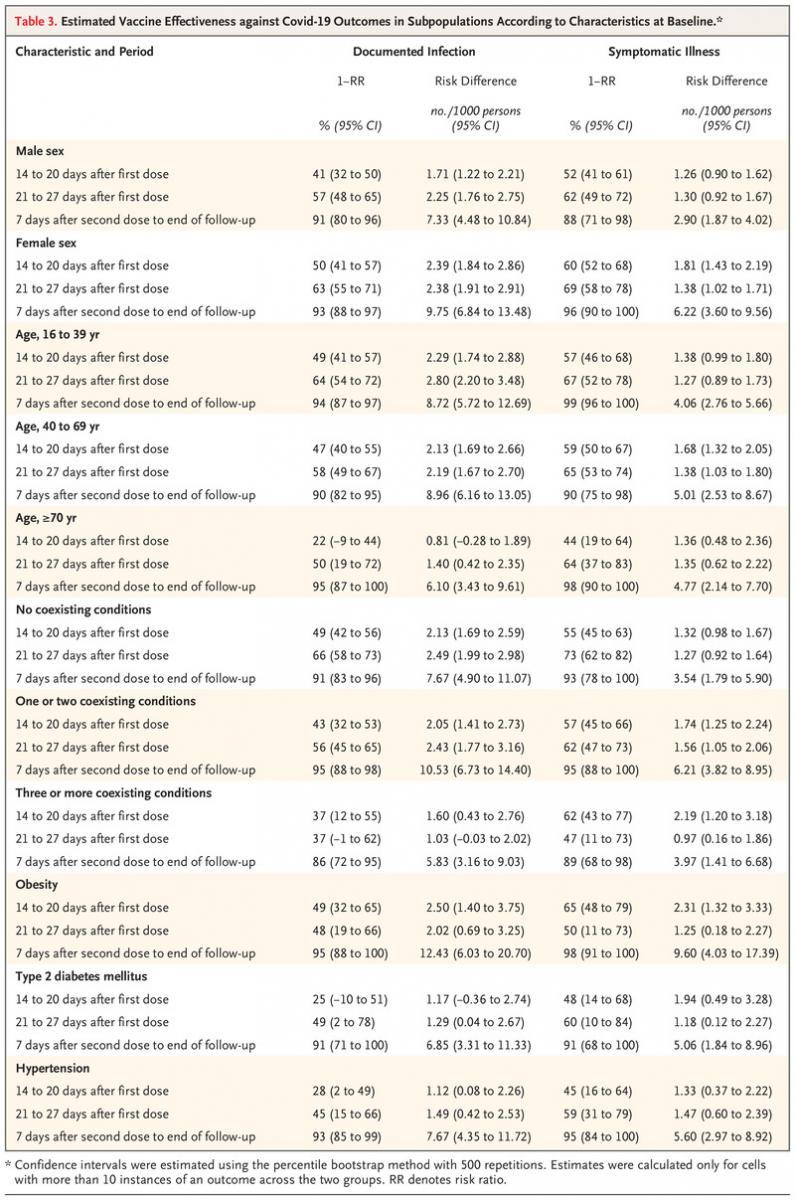
- En la siguiente tabla se muestra la efectividad estimada de la vacuna para la infección documentada por SARS-CoV-2 y los resultados de covid-19 en subpoblaciones definidas por edad, sexo y condiciones coexistentes.
Comentarios de los autores
- Este estudio evalúa la eficacia de la nueva vacuna de ARNm BNT162b2 (Comirnaty) contra covid en un entorno de vacunación masiva a nivel nacional.
- La efectividad estimada de la vacuna después de 7 días tras la segunda dosis fue del 92 % para la infección documentada, el 94 % para la covid sintomática, el 87·% para la hospitalización y el 92 % para la covid grave.
- La efectividad estimada durante los días 14 a 20 (después de la primera dosis) y los días 21 a 27 (cambio gradual entre la primera y la segunda dosis de vacuna) fue del 46·% y 60 % para la infección documentada, 57 % y 66 % para covid sintomático, 74·% y 78 % para la hospitalización, 62 % y 80 % para covid grave y 72 % y 84 % para muerte relacionada con covid, respectivamente.
- Igual que en los ensayos previos a la autorización de la vacuna (Polack FP, et al. N Engl J Med. 2020;383:2603-15), las curvas de incidencia acumulada de covid sintomática comenzó a diverger a partir de los 12 días tras la primera dosis.
- La eficacia estimada de la vacuna para covid sintomática a partir del día 7 después de la segunda dosis fue del 95 % en el ensayo aleatorizado, en comparación con el 94 % en este estudio.
- La eficacia estimada entre la primera y la segunda dosis fue del 52 % en el ensayo, en comparación con el 29 % en este estudio (aunque en este fue del 57·% entre los 14 y 20 días después de la primera dosis).
- En el ensayo, la eficacia estimada de la vacuna para covid grave (89 % durante todo el período de estudio) se basó en solo 10 casos. El estudio actual registró 229 casos de covid grave: 55 en el grupo de vacunados y 174 en el de los no vacunados, lo que resultó en una efectividad estimada del 62 % para los días 14 a 20 después de la primera dosis, 80 % para los días 21 a 27, y 92·% durante 7 o más días después de la segunda dosis.
- Durante el período de este estudio, una proporción cada vez mayor de aislamientos de SARS-CoV-2 en Israel, hasta un 80 % en los días previos a la extracción de datos, eran de la variante B.1.1.7. Por lo tanto, este estudio estima una efectividad promedio de la vacuna sobre múltiples cepas. Aunque no se proporciona una estimación de la eficacia específica para la variante B.1.1.7, la meseta observada durante los últimos períodos en la curva de incidencia acumulada para las personas vacunadas sugiere que la vacuna BNT162b2 también es eficaz para esta variante, una observación consistente con informes anteriores.
- Se tomaron precauciones para evitar la disparidad y los sesgos en la selección de los grupos de vacunación y sus controles; en especial, se puso interés en reducir los sesgos en cuanto a los comportamientos de las personas incluidas en lo que se refiere a las precauciones tomadas contra el contagio de la infección.
Conclusión de los autores
- Este estudio estima una alta eficacia de la vacuna BNT162b2 (Comirnaty) para prevenir la covid sintomática en un entorno no controlado, similar a la eficacia de la vacuna registrada en el ensayo aleatorizado previo (Polack FP, et al. N Engl J Med. 2020;383:2603-15).
- Este estudio también sugiere que la efectividad es alta para los resultados más graves: hospitalización, enfermedad grave y muerte.
- Además, el beneficio estimado aumenta en magnitud a medida que pasa el tiempo.
- Estos resultados refuerzan la expectativa de que las vacunas recientemente aprobadas puedan ayudar a mitigar los profundos efectos globales de la pandemia Covid-19.
-oOo-
Más información:
- Otras noticias sobre el nuevo coronavirus y sus vacunas en esta web.
- PHE, 22/feb de 2021. First real-world UK data shows Pfizer-BioNTech vaccine provides high levels of protection from the first dose. PHE has today published the first independent analysis in the UK showing the Pfizer-BioNTech vaccine is effective against COVID-19 from the first dose.
- Polack FP, et al. Safety and efficacy of the BNT162b2 mRNA Covid-19 vaccine. N Engl J Med 2020;383:2603-15.
- Baden LR, et al. Efficacy and safety of the mRNA-1273 SARS-CoV-2 vaccine. N Engl J Med 2020;384:403-16.