Fecha de actualización: 26 de mayo de 2021
 La European Medicines Agency (EMA) ha informado ayer lunes 3 de mayo de 2021, a través de una escueta nota de prensa [5], de que se ha iniciado el estudio de la solicitud de Pfizer & BioNTech para ampliar la edad autorizada de uso de la vacuna de la covid Comirnaty, e incluir a los adolescentes de 12 a 15 años de edad.
La European Medicines Agency (EMA) ha informado ayer lunes 3 de mayo de 2021, a través de una escueta nota de prensa [5], de que se ha iniciado el estudio de la solicitud de Pfizer & BioNTech para ampliar la edad autorizada de uso de la vacuna de la covid Comirnaty, e incluir a los adolescentes de 12 a 15 años de edad.
La EMA [6] es la entidad responsable de la autorización de uso de las vacunas [7] en el ámbito de la Unión Europea (UE) y del Espacio Económico Europeo [8] (en el cual se incluyen, además de la UE, Islandia, Liechtenstein y Noruega).
La investigación de las vacunas de la covid en niños y adolescentes [9] está lanzada. Con el paso dado ahora por la EMA se acerca el momento en el que, si esta accede a la autorización, pueda contarse por primera vez con una vacuna de la covid disponible para la edad pediátrica [10].
Antecedentes
- La vacuna Comirnaty [11] obtuvo una autorización condicional de uso en personas de 16 o más años de edad en la Unión Europea el pasado 21 de diciembre de 2020.
- El 31 de marzo de 2021, Pfizer & BioNTech anunciaron los primeros datos preliminares de un estudio en fase 3 sobre 2600 adolescentes [12], con una elevada eficacia y seguridad. También que habían solicitado a la FDA la autorización en el rango de edad de 12-15 años de edad.
- Ayer 3 de mayo de 2021, según medios de comunicación, se anunció que la FDA estadounidense preve aprobar en pocos días esta vacuna en los adolescentes [13], mediante una enmienda a la autorización previa, lo que acerca el momento de la incorporación de los adolescentes a la vacunación.
Declaraciones de responsables de BioNTech aseguran que se dispondrá de datos de niños de 5-11 años en el próximo mes de julio y de menores de esa edad en el tercer trimestre de este año.
Evolución de la vacunación de la covid en España
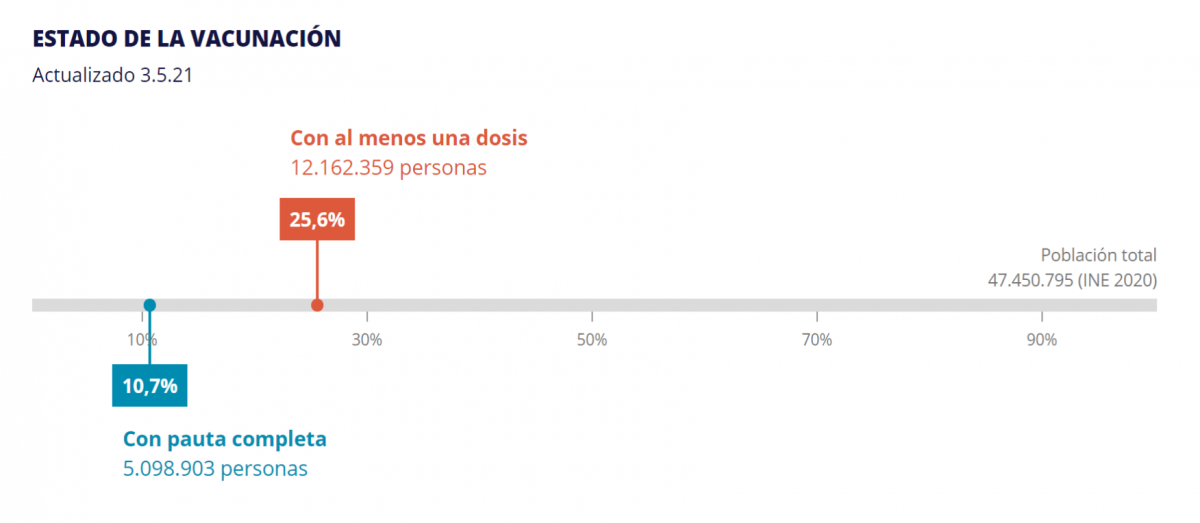
Con fecha 3 de mayo de 2021 y según datos de la Estrategia de vacunación COVID-19 en España [14] un 25,6 % de la población española ha recibido, al menos, una dosis de alguna vacuna de las autorizadas, y el 10,7 % (casi 5,1 millones de personas) ha recibido la pauta completa (ver imagen adjunta).
Uso de la vacuna Comirnaty
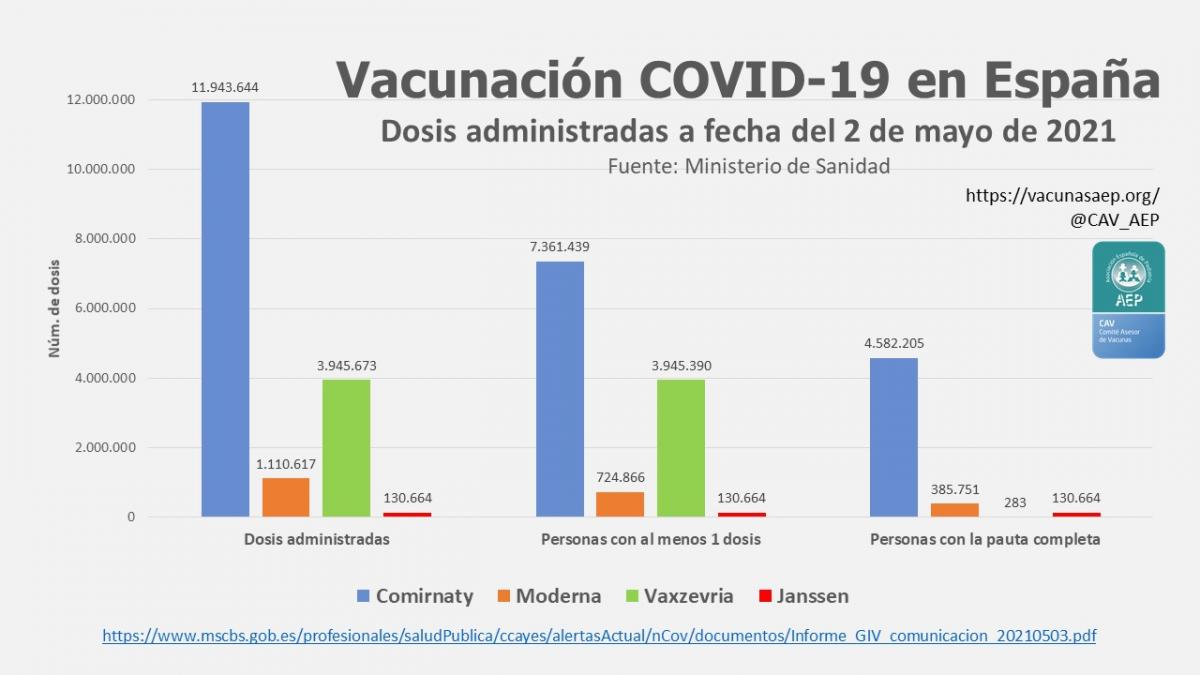
La vacuna Comirnaty es la más usada hasta el momento: el 60,5 % de las personas que han recibido, al menos, una dosis, y el 89,8 % de las que han recibido dos dosis (ver imagen adjunta).
Vacuna Comirnaty
Información general
En la web dedicada a la vacunación COVID-19 de la Consejería de Salud y Familias de la Junta de Andalucía [16] se han publicado unas muy prácticas infografías sobre la cada una de las vacunas covid, además de otras informaciones prácticas. La infografía dedicada a la vacuna Comirnaty puede verse abajo.
Adenda, 5 de mayo de 2021. Health Canada ha ampliado la autorización de uso de la vacuna Comirnaty a los adolescentes de 12-15 años de edad, según aseguran sendos comunicados de Health Canada [18] y de Pfizer & BioNTech [19], datados en esta fecha.
Adenda, 10 de mayo de 2021. En esta fecha, la FDA estadounidense ha autorizado la ampliación del uso de emergencias de la vacuna de Pfizer & BioNTech [20] a los adolescentes de 12-15 años de edad, con la misma pauta vacunal. Según la nota de la FDA, la aprobación está basada en los datos aportados por Pfizer, de los cuales destacan:
- Participantes en el estudio 2260 adolescentes de 12-15 años; de ellos 1131 recibieron de forma ciega y aleatoria la vacuna y otros 1129 solo placebo (suero salino fisiológico). Seguimiento de al menos 2 meses tras acabar la pauta vacunal en al menos la mitad de los participantes.
- Inmunogenicidad. Se compararon 190 participantes con 170 de 16-25 años, encontrando pruebas de no inferioridad.
- Eficacia clínica en adolescentes sin antecedentes de infección previa: 7 días o más después de la segunda dosis, cero casos en 1005 vacunados frente a 16 casos en 978 del grupo placebo (EV: 100 %, IC 95 %: 75,3-100 %).
- Seguridad: solo manifestaciones leves-moderadas, 1-3 días tras la vacunación, de mayor intensidad tras la segunda dosis (excepto dolor en el lugar de inyección). Síntomas usuales: dolor en el brazo, cansancia, dolor de cabeza, escalofrios, mialgia y artralgia, fiebre. En general similar a los de 16-25 años, salvo la fiebre que fue algo más frecuente (20 % vs. 17 %).
- Contraindicación: alergia grave a una dosis previa de la misma vacuna o a algún componente.
- Tras la reunión del ACIP del 12 de mayo [21], se prevé que pueda comenzar la vacunación en pocos días, aunque se espera que las dudas y reticencias de las familias y los adolescentes [22] pueda ser una barrera relevante.
Adenda, 15 de mayo de 2021. El ACIP de EE. UU. en su reunión del 12 de mayo de 2021 (documentos presentados [23]) recomendó ampliar el uso de Comirnaty a los adolescentes de 12-15 años de edad. Otros documentos relacionados:
- Wallace M, et al. The Advisory Committee on Immunization Practices’ Interim Recommendation for Use of Pfizer-BioNTech COVID-19 Vaccine in Adolescents Aged 12–15 Years — United States, May 2021. MMWR Morb Mortal Wkly Rep. 2021, 14/may. DOI: 10.15585/mmwr.mm7020e1 [24].
- Pfizer-BioNTech COVID-19 Vaccine EUA Amendment Review Memorandum. Emergency Use Authorization (EUA) Amendment for an Unapproved Product. Review Memorandum [25], 9 de abril de 2021.
- FDA. Pfizer-BioNTech COVID-19 Vaccine [26].
Adenda, 26 de mayo de 2021. Moderna presenta los resultados preliminares en adolescentes de 12-17 años de edad [27]:
- Estudio en fase 2/3 con 3732 participantes de 12-17 años de edad, distribuidos (2:1) en un grupo de vacunación (2 dosis) y placebo.
- Desde 14 días después de la segunda dosis hubo 4 casos frente a cero en el grupo de vacunación, lo que se traduce en un eficacia vacunal del 100 %.
- Usando los criterios del CDC (síntomas leves y confirmación microbiológica), la eficacia vacunal resultante es del 93 %.
- La compañía prevé solicitar la autorización de uso en este grupo de edad, en el mes de junio.
-oOo-
Más información
- Fichas técnicas [28] de las vacunas de la covid. Ficha técnica de Comirnaty [29].
- Ministerio de Sanidad. Guía técnica de uso de la vacuna Comirnaty [30] (versión vigente del 31 de marzo de 2021).
- Otras noticias sobre el SARS-CoV-2 y sus vacunas [31] en esta web.
Historial de actualizaciones
- 26 de mayo de 2021. Moderna presenta resultados preliminares en adolescentes de 12-17 años de edad.
- 15 de mayo de 2021. Se añade información relacionada con la aprobación del uso de Comirnaty en adolescentes en EE. UU.
- 10 de mayo de 2021. Se añade la noticia de que la FDA de EE. UU. ha autorizado el uso de de Comirnaty en adolescentes de 12-15 años.
- 5 de mayo de 2021. Se añade la noticia de la autorización del uso de Comirnaty por parte de Canadá.