| En pocas palabras |
|
-oOo-
Introducción
La gonorrea es una infección de transmisión sexual (ITS) causada por la bacteria Neisseria gonorrhoeae (gonococo). Su incidencia está aumentando de forma alarmante a nivel mundial, con más de 82 millones de casos registrados en 2020 y se observa igualmente un incremento en la resistencia a antibióticos. La gonorrea causa una morbilidad significativa y sigue siendo un importante problema de salud pública a nivel mundial, por lo que la OMS ha desarrollado una estrategia mundial para reducir la gonorrea [1] en un 90 % para 2030.
El pasado 2 de junio de 2025, la Xunta de Galicia [2] ha iniciado un programa dirigido a personas menores de 65 años con elevado riesgo de contraer gonorrea, convirtiéndose así, en la primera jurisdicción del mundo en implementar un programa estructurado de salud pública para prevenir dicha enfermedad mediante la vacunación.
Se incluirán en el programa personas de 19 a 65 años con:
- Diagnóstico reciente (< 12 meses) de infección de transmisión sexual (ITS) por Neisseria gonorrhoeae, Chlamydia trachomatis, Treponema pallidum, Mpox virus o VIH
- Antecedentes de 2 o más ITS en los últimos 5 años
- Sospecha clínica de gonorrea
- Comportamiento o prácticas de riesgo en el último año
El 10 de noviembre de 2023 [4], el JCVI (Joint Scientific Committee on Vaccination and Immunisation) del Reino Unido acordó que se debía iniciar un programa específico con 4CMenB para prevenir la gonorrea en personas con riesgo de infección que acudían a servicios de salud sexual en dicho Estado. Esta decisión se tomó tras revisar la evidencia de estudios observacionales retrospectivos y prospectivos, datos clínicos y de laboratorio, informes nacionales de vigilancia y análisis económicos de la salud. En el pasado mes de agosto de 2025 se ha publicado la decisión de iniciar en el Reino Unido el programa de vacunación dirigido inicialmente a población muy seleccionada de riesgo elevado: hombres homosexuales o bisexuales con historia de múltiples contactos sexuales y/o ITS de diagnóstico en el último año (Wise J, BMJ 2025 [5]).
Es importante resaltar que la política regional gallega ofrece un programa de vacunación más amplio e inclusivo que el británico (Martinón-Torres F, Lancet Infect dis 2025 [6]).
¿En qué estudios se basa el empleo de 4CMenB para la prevención de la gonorrea?
La ficha técnica de 4CMenB [7] no incluye la indicación de prevención de gonorrea, pero varios estudios apoyan el uso de esta vacuna con ese objetivo en pacientes de riesgo.
A finales de la década de 1990 y principios de la década de 2000, Nueva Zelanda sufrió una epidemia de meningitis causada por la cepa del grupo B de Neisseria meningitidis. Para intentar controlar la infección, el Ministerio de Salud del país lanzó el programa de inmunización MeNZB, una vacuna “a la carta” frente a MenB, y se ofreció vacunación gratuita a todos los menores de 20 años (Sexton K, N Z Med J 2004 [8]). La campaña, que se desarrolló entre 2004 y 2006, redujo los casos de meningitis relacionados con la cepa del grupo B, y, sorprendentemente, se objetivó un descenso claro de casos de gonorrea entre la población que recibió la vacuna.
En 2017, un estudio retrospectivo de casos – control publicado en Lancet comparó la incidencia de gonorrea en quienes recibieron la vacuna MeNZB con quienes no la recibieron. Los investigadores estimaron una eficacia del 31 % de la vacuna MeNZB contra la ITS (Petoussis-Harris H, Lancet 2017 [9]).
Estudios observacionales realizados en EE.UU. (Abara WE, Lancet Infect Dis 2022 [10]) (Bruxvoort KJ, Clin Infect Dis 2023 [11]), Australia (Marshall HS, Vaccines 2022 [12]) y Canadá (Longtin J, Open Forum Infect Dis. 2017 [13]) han mostrado una efectividad del 32-47 % (IC95·% 23–53) en la prevención de gonorrea en adolescentes con una pauta de dos dosis de vacuna 4CMenB. La duración de la protección es un determinante importante del efecto y coste-efectividad de la vacunación, así como de la necesidad y el momento de la vacunación de refuerzo requerida para mantener una protección suficiente de la población. En este sentido, el programa de inmunización contra la gonorrea propuesto en el Reino Unido incluirá un seguimiento sistemático de los casos en personas vacunadas, utilizando protocolos estandarizados.
Cabe destacar que Australia ha publicado en julio de 2025 un estudio de datos reales del programa para adolescentes del sur del país informando una eficacia de la vacuna del 41,8 % (IC del 95 %: 34,0-48,7) contra la gonorrea en los primeros 5 años posteriores a la vacunación, con una protección del 27,0 % (1,2-46) contra la reinfección (Wang B, Clin Infect Dis 2025 [14]).
En una reciente revisión sistemática y metaanálisis, autores australianos han publicado también estudios existentes sobre la efectividad de la vacuna 4CMenB en el control de la gonorrea (Wang B, J Infect 2024 [15]). Se evalúa la efectividad vacunal (VE) y el impacto poblacional (VI) de las vacunas meningocócicas, especialmente las basadas en vesículas de membrana externa (OMV) frente a infecciones por Neisseria gonorrhoeae. Se incluyeron 12 estudios (nueve sobre VE y cuatro sobre VI), principalmente centrados en adolescentes y adultos jóvenes (15-30 años). Los resultados muestran que:
- Las vacunas MenB-OMV (como 4CMenB, MeNZB, MenBvac y VA-MENGOC-BC) ofrecen una protección cruzada moderada frente a la gonorrea, con una VE estimada entre el 22 % y el 46 %. El metaanálisis reporta una VE agrupada de 33-34 % tras la pauta completa de vacunación
- Las vacunas no basadas en OMV, como MenB-FHbp, no muestran eficacia frente a gonorrea (VE ~3%)
- El impacto poblacional (VI) se ha evidenciado en países como Canadá, Cuba, Noruega y Australia, con reducciones de incidencia que oscilan entre el 30 % y el 59 %
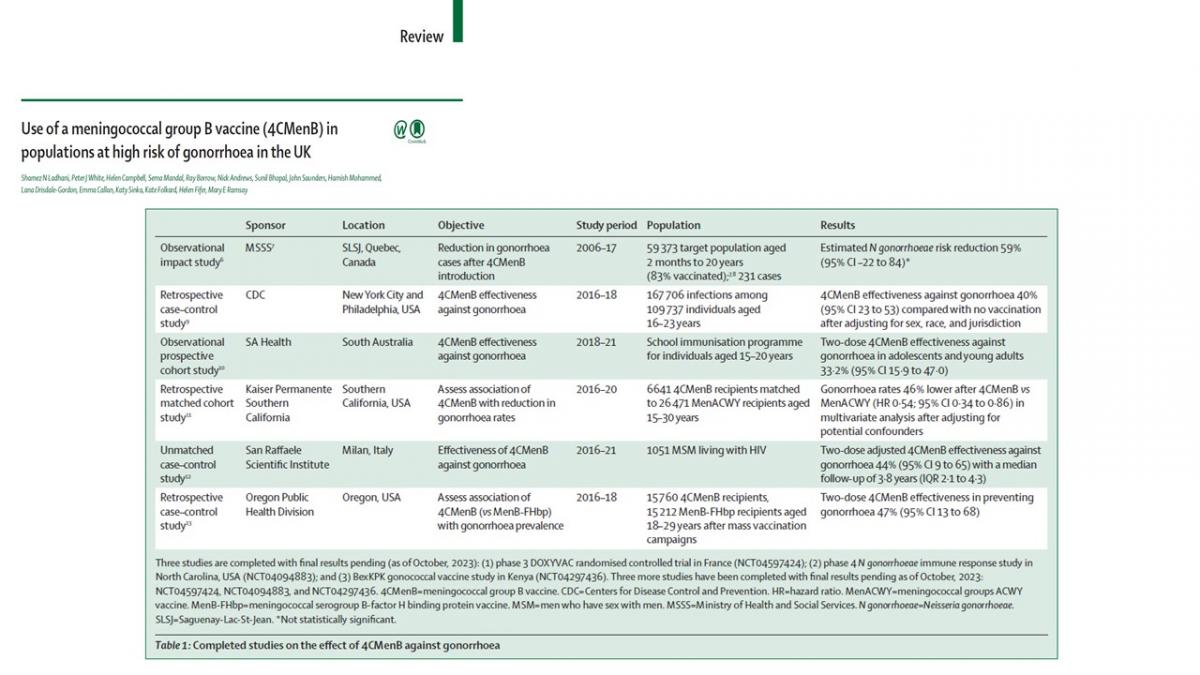
En esta publicación del Lancet Infectious Diseases de 2024 (Ladhani SN, Lancet Infect Dis 2024 [16]), los autores resumen la evidencia que respalda el uso de 4CMenB para la protección contra la gonorrea (Tabla 1) y los datos necesarios para fundamentar la planificación de programas a largo plazo y su extensión a la población en general.
Tabla 1. Estudios completados sobre el efecto de 4CMenB frente a la gonorrea.
¿Será posible el control de la gonorrea mediante la vacunación con 4CMenB?
La investigación para el desarrollo de una vacuna contra la gonorrea se encuentra en fases muy iniciales debido a la dificultad de identificar antígenos que generen respuestas inmunitarias protectoras, y en más de 30 años no se ha llegado a completar ningún ensayo clínico de vacunas frente a Neisseria gonorrhoeae. Sin embargo, a pesar de no existir una vacuna específica para hacer frente al gonococo, la evidencia científica confirma la protección cruzada que ofrece la vacuna 4CMenB empleada para proteger a la población de la Neisseria meningitidis del serogrupo B. Las bacterias que provocan ambas enfermedades están estrechamente relacionadas genéticamente al pertenecer al mismo género (Neisseria) y contar con una homología de secuencia próxima al 90 %. Esta semejanza ofrece la posibilidad de protección cruzada contra Neisseria gonorrhoeae mediante vacunas contra el meningococo B que contienen vesículas de membrana externa (OMV) (Leduc I, PLoS Pathog 2020 [18]). De hecho, la evidencia de protección solo se ha observado en vacunas que contienen OMV, como 4CMenB y MeNZB. Un estudio observacional demostró que la vacuna MenB-FHbp no tuvo efecto sobre la infección por gonorrea (Abara WE, Sex Transm Dis 2023 [19]).
Bases inmunológicas
Recientemente se ha publicado un amplio estudio (Zeppa JJ, mSphere 2025 [20]) que evalúa los mecanismos inmunológicos subyacentes a la protección cruzada observada entre la vacuna antimeningocócica 4CMenB y la infección por Neisseria gonorrhoeae. Los autores confirman que 4CMenB induce una respuesta humoral robusta, con producción de IgG (especialmente IgG1, IgG2a y 2b) y cierto reconocimiento antigénico cruzado entre N. meningitidis y N. gonorrhoeae, aunque con variabilidad individual y sin correlación clara con protección efectiva. El hallazgo más relevante es la identificación de una respuesta celular compleja, con incremento significativo de células CD4+ de memoria (Tem y Tcm) en el tracto genital, y una producción destacada de citoquinas tipo TH1 (IL-2, IFN-γ, TNF-α), especialmente por linfocitos no convencionales (CD3− CD19−), presumiblemente NK o ILC tipo 1.
El estudio plantea que la protección inducida por 4CMenB frente a Neisseria gonorrhoeae no depende únicamente de anticuerpos, sino de una inmunidad adaptativa multifacética, en la que la respuesta celular desempeña un papel clave. Estos hallazgos aportan nuevas pistas sobre los correlatos de protección y refuerzan la hipótesis de que vacunas frente a gonococo deberán inducir respuestas celulares además de humorales.
Por su parte, el grupo investigador del Prof. Rappuoli ha publicado recientemente los resultados preliminares de un estudio en el que han demostrado que un subconjunto de anticuerpos generados por la vacuna 4CMenB puede presentar reacción cruzada contra epítopos relacionados del gonococo. Estos anticuerpos fueron capaces de eliminar el gonococo in vitro, lo que se tradujo en una eficacia protectora in vivo. Estos datos ayudan a explicar por qué la vacunación con 4CMenB confiere cierta protección contra el gonococo y ofrecen una vía terapéutica para la infección gonocócica (Troisi M, Sci Transl Med 2025 [21]).
Perspectivas futuras
Actualmente, se están llevando a cabo varios ensayos clínicos para evaluar la eficacia de 4CMenB contra la gonorrea en poblaciones con mayor riesgo de infección, con el objetivo de proporcionar evidencia que pueda considerarse más sólida que los estudios observacionales a gran escala (Tabla 2).
Tabla 2. Estudios en curso con 4CMenB y gonorrea.
Quedan, por supuesto, muchos aspectos por desarrollar. Así, en una publicación reciente (White PJ, Open Forum Infect Dis 2025 [24]) se exponen nuevas evidencias sobre la protección parcial que ofrece la vacuna 4CMenB frente a Neisseria gonorrhoeae. Aunque estudios previos ya sugerían una cierta eficacia protectora, no estaba claro si dicha protección seguía un modelo “all-or-nothing” (protección completa en algunos individuos y nula en otros) o “leaky” (protección parcial en todos los vacunados). Los datos recientes de varios estudios (Raccagni AR. Open Forum Infect Dis 2024 [25]) apuntan claramente a un patrón “leaky”. Este hallazgo valida supuestos clave utilizados en modelos de impacto poblacional y coste-efectividad aplicados previamente, especialmente en el contexto del asesoramiento del JCVI británico para implementar un programa de vacunación frente a gonorrea con 4CMenB.
En conclusión
La experiencia acumulada en Galicia, junto con la del Reino Unido, en la implementación de programas de inmunización selectiva con la vacuna 4CMenB frente a la gonorrea, constituirá una base de evidencia esencial para respaldar la estrategia y fortalecer las medidas de control de la enfermedad.
La vigilancia posterior a la puesta en marcha permitirá obtener datos más robustos, fundamentales para orientar los análisis de economía de la salud y las decisiones de política internacional. Si ambos programas demuestran ser exitosos, será imprescindible avanzar en iniciativas que garanticen que la vacuna sea accesible y asequible, especialmente en aquellos países con mayor incidencia de gonorrea (Ladhani SN, Lancet Infect Dis. 2025 [26]).
-oOo-
Bibliografía
- Abara WE, et al. Effectiveness of a serogroup B outer membrane vesicle meningococcal vaccine against gonorrhoea: a retrospective observational study. Lancet Infect Dis. 2022; 22(7):1021-1029 [10]
- Abara WE, et al. Healthy Vaccinee Bias and MenB-FHbp Vaccine Effectiveness Against Gonorrhea. Sex Transm Dis. 2023; 50(6): e8-e10 [19]
- Anderer S. The Meningitis Vaccine Appears to Protect Against Gonorrhea-Scientists May Now Know Why. JAMA. 2025; 334(5):377-378 [27]
- Bruxvoort KJ, et al. Prevention of Neisseria gonorrhoeae with meningococcal B vaccine: a matched cohort study in southern California. Clin Infect Dis 2023; 76: e1341–49 [11]
- Ladhani SN, et al. The United Kingdom meningococcal vaccine (4CMenB) programme against gonorrhoea: A review of the evidence and knowledge gaps. Journal of Infection, Volume 91, Issue 3, 106582 [28]
- Ladhani SN, et al. Use of a meningococcal group B vaccine (4CMenB) in populations at high risk of gonorrhoea in the UK. Lancet Infect Dis. 2024;24(9):e576-e583 [16]
- Ladhani SN, et al. What can be learnt from the world's first national vaccination programme against gonorrhoea. The Lancet Infectious Diseases 2025, Volume 25, Issue 11, 1168 – 1170 [16]
- Leduc I, et al. The serogroup B meningococcal outer membrane vesicle-based vaccine 4CMenB induces cross-species protection against Neisseria gonorrhoeae. PLoS Pathog. 2020; 16(12):e1008602 [18]
- Longtin J, et al. Possible Impact of Wide-scale Vaccination Against Serogroup B Neisseria Meningitidis on Gonorrhea Incidence Rates in One Region of Quebec, Canada. Open Forum Infect Dis. 2017; 4: S734-S735 [29]
- Marshall HS, et al. An Observational Study to Assess the Effectiveness of 4CMenB against Meningococcal Disease and Carriage and Gonorrhea in Adolescents in the Northern Territory, Australia-Study Protocol. Vaccines (Basel). 2022; 10(2):309 [12]
- Martinón-Torres, F, et al. Galicia's gonorrhoea vaccination programme. The Lancet Infectious Diseases 2025, Volume 25, Issue 11, e625 [6]
- Petoussis-Harris H, et al. Effectiveness of a group B outer membrane vesicle meningococcal vaccine against gonorrhoea in New Zealand: a retrospective case-control study. Lancet. 2017;390 (10102):1603-1610 [30]
- Sexton K, et al. The New Zealand Meningococcal Vaccine Strategy: a tailor-made vaccine to combat a devastating epidemic. N Z Med J. 2004; 117(1200):U1015 [8]
- Troisi M, et al. Human monoclonal antibodies targeting subdominant meningococcal antigens confer cross-protection against gonococcus. Sci Transl Med. 2025;17(799): eadv0969 [21]
- White PJ, et al. New Insights into Gonorrhea Natural History and Protection by 4CMenB, and a Call for More Analyses of Existing Studies and Enhanced Data Collection. Open Forum Infect Dis. 2025; 12(5): ofaf214 [24]
- Zeppa JJ, et al. Meningococcal vaccine 4CMenB elicits a robust cellular immune response that targets but is not consistently protective against Neisseria gonorrhoeae during murine vaginal infection. mSphere. 2025; 10(5):e0094024 [20]
- Wang B, et al. Long-Term Protection Against Invasive Meningococcal B Disease and Gonococcal Infection 5 Years After Implementation of Funded Childhood and Adolescent 4CMenB Vaccination Program in South Australia: An Observational Cohort and Case-Control Study. Clin Infect Dis. 2025 Nov 6;81(4):e202-e210 [14]
- Wang B, et al. Vaccine effectiveness and impact of meningococcal vaccines against gonococcal infections: A systematic review and meta-analysis. J Infect. 2024; 89(3):106225 [15]
- Wise J. Gonorrhoea: England rolls out "world first" vaccination programme. BMJ. 2025; 22:389: r1064 [5]
Enlaces web
- La Xunta comienza a vacunar frente a la gonorrea a la población con alto riesgo de contraer esta infección de transmisión sexual [2]
- Ficha técnica de Bexsero (4CMenB [7])
- OMS. Gonorrea (infección por Neisseria gonorrhoeae) [1], 4 de julio de 2024,
- JCVI. JCVI advice on the use of meningococcal B vaccination for the prevention of gonorrhoea [4]. 10 November 2023.
- NHS England. NHS and local government to roll out world-first vaccine programme to prevent gonorrhoea [31] 21 may 2025.