 [1]
[1]
Desde 2015 la OMS viene advirtiendo de los riesgos de emergencia de epidemias y pandemias [2] y de la necesidad de hacer preparativos para afrontarlos a nivel global. También señaló una serie de microorganismos [3] con conocidas capacidades de difusión e infectividad y elevado impacto poblacional. La, entonces llamada, “enfermedad X” representaba riesgos desconocidos que también necesitaban ser previstos e investigados. La reciente irrupción del nuevo coronavirus SARS-CoV-2 [4] es una materialización de este tipo de riesgo.
En 2014, un blog científico español aventuró que un coronavirus podría protagonizar la siguiente pandemia [5]. En 2015, fue Bill Gates quien advirtió [6] que la mayor amenaza a la que se enfrenta el mundo sería una enfermedad infecciosa y no una gran guerra u otro tipo de catástrofe.
Tras la irrupción del brote de infección respiratoria por el nuevo coronavirus SARS-CoV-2 (declarado por la OMS como “emergencia de salud pública de interés internacional”, PHEIC, el 30 de enero de 2020 [7]) y su difusión pandémica (declaración de la OMS del 11 de marzo [8]), la investigación está siendo intensísima. Todos los frentes están abiertos, virológico, inmunológico, clínico, etc., siendo uno de ellos el desarrollo de vacunas capaces de proporcionar protección individual y poblacional frente al virus y de frenar su, por el momento imparable, avance.
Reflejo de la labor investigadora desarrollada es que en los tres primeros meses del brote, una búsqueda de publicaciones en PubMed [9] relacionadas con el nuevo coronavirus muestra 1670 publicaciones, a fecha del 29 de marzo de 2020 con los términos de búsqueda de "COVID19 o SARSCov2". Afortunadamente, la gran mayoría de las publicaciones se ofrecen en modo de acceso libre, como expresión de la solidaridad científica ante la amenaza global que el mundo afronta.
Prioridades en la investigación
Un grupo de expertos reunidos por la OMS ha señalado los objetivos prioritarios en la investigación [10] del nuevo coronavirus y la COVID-19, que son: el origen y la historia natural del virus y su transmisión; epidemiología; caracterización clínica y tratamiento; prevención y control de la infección, especialmente en los centros sanitarios; productos terapéuticos y vacunas; y, finalmente, las consideraciones éticas y la integración de estudios sociales relacionados con la respuesta a los brotes.
Vacunas
Las vacunas frente al SARS-Cov-2 se presentan como uno de los pilares principales de lucha contra el avance del virus, pero su desarrollo lleva tiempo, por lo que no será un arma disponible en la práctica hasta por lo menos un año, en palabras de Anthony Fauci [11], director del NIAID [12] estadounidense (siempre con permiso de la industria científica china [13], que podría sorprender con avances en un tiempo menor). Las entidades reguladoras (EMA, FDA) ya han anunciado que disponen de procedimientos prioritarios para acelerar los procesos de evaluación y eventual autorización.
La experiencia y los desarrollos logrados en la búsqueda de vacunas frente al SARS (2003) y el MERS (desde 2012) van a resultar de gran importancia en la carrera por encontrar una para el nuevo coronavirus surgido en este 2020.
Muy probablemente, a medio y largo plazo, las vacunas jugarán un papel primordial en las estrategias de control de la transmisión y los brotes causados por el SARS-CoV-2. En esta dirección, son numerosas las entidades que ya han destinado importantes fondos económicos a la investigación de vacunas frente a este virus [1]. Por ejemplo, CEPI [14] (Coalition For Epidemic Preparedness Innovations), una entidad enfocada a la promoción de la investigación de vacunas frente a potenciales amenazas pandémicas, ha comenzado a financiar ocho proyectos [15], como son: vacuna recombinante que usa como vector al virus del sarampión [16] (Instituto Pasteur, Themis y la Universidad de Pittsburgh); vacuna recombinante basada en el virus de la gripe [17] (Universidad de Hong Kong); vacuna recombinante que emplea como vector un adenovirus del chimpancé, ChAdOx1 (Jenner Institute, Universidad de Oxford); vacuna de proteína recombinante obtenida por tecnología de nanopartículas, adyuvada (Novavax); vacuna de proteína quimérica recombinante mediante la tecnología de la “pinza molecular” (Universidad de Queensland); vacuna mRNA-1273 (Moderna); vacuna de ARNm (CureVac); y vacuna DNA INO-4800 (Inovio Pharmaceuticals).
A fecha del 20 de marzo de 2020, la OMS contabiliza al menos 44 productos candidatos a vacuna frente al nuevo coronavirus [18] en investigación.
| Productos candidatos a vacunas frente al SARS-CoV-2 (fuente: OMS [18], 20 de marzo de 2020) | |||
|---|---|---|---|
| Fase | Plataforma | Tipo | N.º de productos |
| Investigación clínica, fase 1 (n=2)* | Vector viral no replicante | Adenovirus tipo 5 | 1 |
| ARN | ARNm | 1 | |
| Investigación preclínica (n=42) | ADN | Plásmido ADN | 3 |
| Inactivada | Formaldehído, Al | 1 | |
| Atenuada | 1 | ||
| Vector viral no replicante | MVA, adenovirus, otros | 6 | |
| Subunidades | Varios | 15 | |
| Vector viral replicante | Sarampión, otros | 3 | |
| ARN | ARNm | 7 | |
| Otros | 6 | ||
| Total | 44 | ||
| * Con fecha 28/marzo, en ClinicalTrials.gov se contabilizan ya tres estudios en fase 1 | |||
Candidatos a vacuna en investigación clínica
En ClinicalTrials.gov [19], a fecha del 28/marzo y con los términos “vaccine / COVID-19” se encuentran cinco estudios sobre productos candidatos a vacuna frente a la COVID-19.
Dos productos destacan porque han comenzado ya el reclutamiento de participantes. Se trata de estudios en fase 1 que se proponen estudiar la seguridad, reactogenicidad e inmunogenicidad de:
- Una vacuna recombinante basada en un vector constituido por un adenovirus sin capacidad de replicación (Ad5-nCoV, NCT04313127 [20], ChiCTR2000030906 [21]).
- Otra basada en el ARNm (mRNA-1273, NCT04283461 [22]).
 [23]Un tercer estudio en fase 1-2, (ChAdOx1 nCoV-19, NCT04324606 [24], registrado el 27/marzo), que aún no ha comenzado el reclutamiento utiliza una vacuna recombinante con un adenovirus del chimpancé ChAdOx1 como vector.
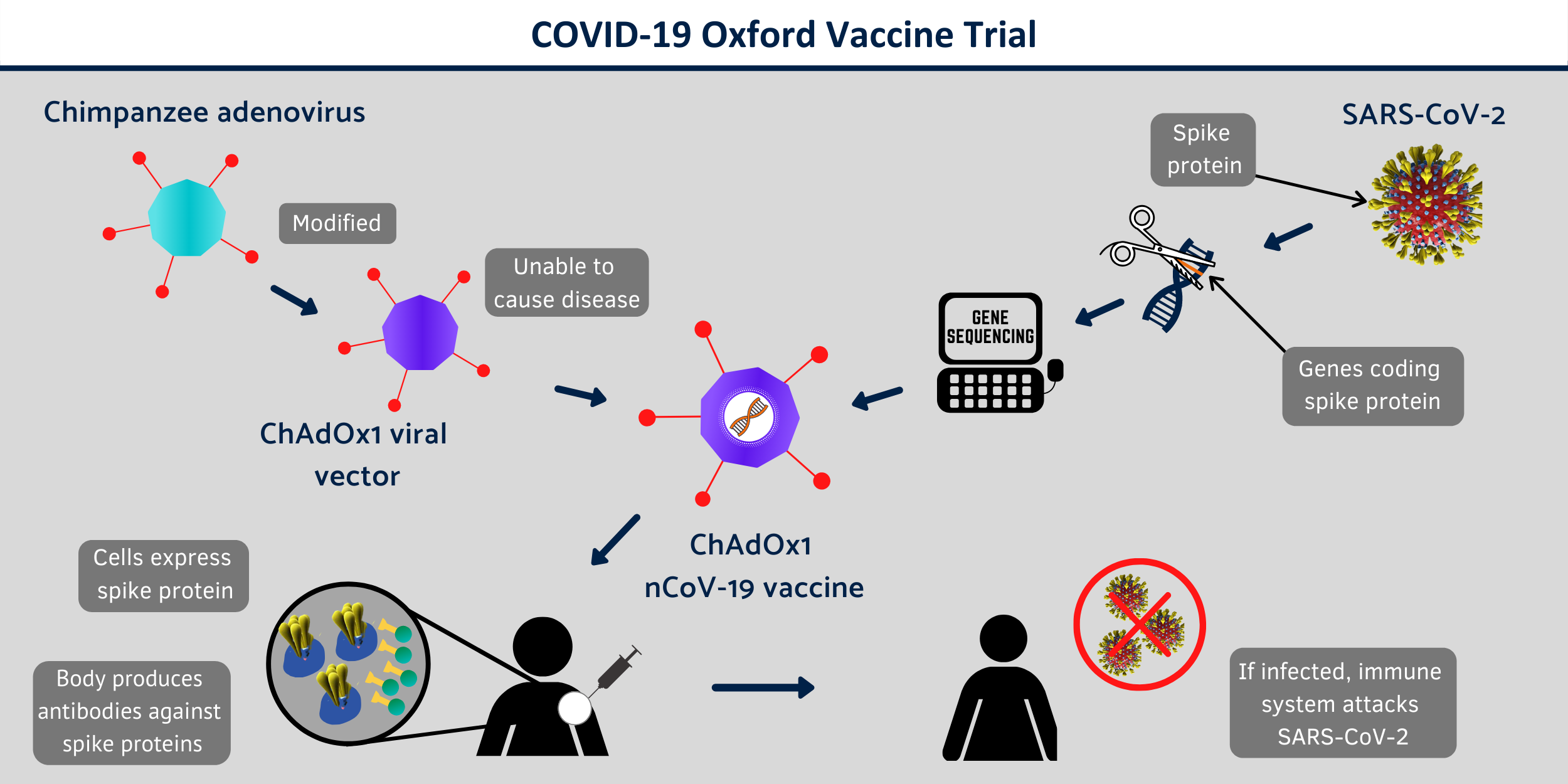
[23]Un tercer estudio en fase 1-2, (ChAdOx1 nCoV-19, NCT04324606 [24], registrado el 27/marzo), que aún no ha comenzado el reclutamiento utiliza una vacuna recombinante con un adenovirus del chimpancé ChAdOx1 como vector.  [25]Este es un ensayo controlado y aleatorizado, simple ciego, frente a un placebo salino, dirigido por Andrew Pollard y la Universidad de Oxford (COVID-19 Oxford Vaccine Trial [23]).
[25]Este es un ensayo controlado y aleatorizado, simple ciego, frente a un placebo salino, dirigido por Andrew Pollard y la Universidad de Oxford (COVID-19 Oxford Vaccine Trial [23]).
En los tres casos citados, la diana es la proteína S (spike) de la superficie del nuevo coronavirus. Bien mediante la inserción de genes en los vectores o por el propio ARNm, se pretende inducir la síntesis natural del mencionado antígeno, que finalmente ocasionaría la respuesta del sistema inmune del huésped, en forma de anticuerpos neutralizantes protectores.
| Estudios (fase 1) con candidatos a vacunas frente a SARS-CoV-2 (fuente: ClinicalTrials [19], 26 de marzo de 2020) | |||
|---|---|---|---|
| NCT04313127 [20] | NCT04283461 [22] | NCT04324606 [24] | |
| Fase | Fase 1, sin enmascaramiento | Fase 1, sin enmascaramiento | Fase 1-2, aleatorizado, controlado frente a placebo, simple ciego |
| Fecha registro | 18/marzo | 25/febrero | 27/marzo |
| Patrocinador | CanSino Biologics Inc. [26], China | NIAID, EE. UU. | Universidad de Oxford, Reino Unido |
| Producto | Ad5-nCoV | mRNA-1273 | ChAdOx1 nCoV-19 |
| Comienzo, situación | 16/marzo, reclutando | 3/marzo, reclutando | |
| Final estimado | Dic/2020 a dic/2022 | Jun/2021 | May/2021 |
| Participantes | 108, de 18-60 años, sanos | 45, de 18-55 años, sanos | 510, 18-55 años, sanos |
| Pautas | 1 dosis, IM | 2 dosis (0 y 28 días), IM | 1-2 dosis (0 y 0-28 días), IM |
Además, otros dos productos en estudio están enfocados al tratamiento y prevención de la neumonía grave en pacientes con COVID-19: uno en fase 1 (NCT04299724 [27]) y otro en fase 1-2 (NCT04276896 [28]). Son productos que se administran por vía subcutánea e intravenosa, compuestos de fragmentos de genes del SARS-CoV-2 en sistemas de lentivirus que buscan estimular y modular la respuesta inmune.
mRNA-1273
El compuesto mRNA-1273 es un producto de investigación de Moderna [29], una empresa estadounidense que ha desarrollado una plataforma basada en el ARN mensajero (ARNm). Un español, Juan Andrés [30], formado en Farmacia en la Universidad de Alcalá de Henares (Madrid), forma parte de su equipo directivo. Entre sus productos en investigación [31] más adelantados (fase 2) se encuentran una vacuna frente al CMV, otra contra el cáncer y un producto cuyo objetivo es la regeneración miocárdica. El producto en investigación (fase 1) destinado a prevenir la COVID-19 se denomina mRNA-1273 [32].
Este compuesto incluye un fragmento de ARN en una nanopartícula lipídica que induciría a las células huésped a sintetizar proteína S (spike) en su conformación prefusión, la cual a su vez despertaría la producción de anticuerpos neutralizantes específicos. Esta investigación está dirigida y financiada por el NIAID [33] estadounidense.
Las vacunas producidas en plataformas basadas en ADN (vehiculizado por plásmidos) y, sobre todo, las de ARN (ARNm en moléculas transportadoras, liposomas, nanopartículas u otras) tienen notables ventajas [34], como su versatilidad y adaptación a distintos microorganismos, así como su mayor capacidad de producción y con un coste menor que los sistemas tradicionales. Las vacunas de ARNm tienen un potencial extraordinario (Nat Rev Drug Discov. 2018;17(4):261-79 [35]). Esta es una cuestión crucial en la respuesta a emergencias sanitarias, como lo es también el de poder contar con suficiente número de dosis vacunales en almacenamiento permanente [36] para responder a contingencias.
Productos que iniciarán la fase 1 en los próximos 2-3 meses
| Productos que iniciarán la fase 1 en los próximos 2-3 meses (fuente: COVID-19 Treatment and Vaccine Tracker, 27 de marzo de 2020) | |||
|---|---|---|---|
| Producto / tipo | INO-4800 / Plásmido ADN | RNA / mRNA | RNA / BNT162 |
| Plataforma común con otros candidatos a vacunas | Virus Lassa, Nipah, HIV, filovirus, VPH, cancer, Zika, y HB | Rabia, virus Lassa y Nipah, fiebre amarilla, MERS, zika y dengue | |
| Promotores | Inovio Pharmaceuticals / Beijing Advaccine Biotechnology | CureVac (Alemania) | BioNTech / Fosun Pharma / Pfizer |
| Financiación | CEPI | CEPI, Unión Europea | |
| Fechas de inicio prevista | Abril 2020 | Junio 2020 | Abril 2020 |
También se investiga si la vacuna BCG (tuberculosis) puede proteger del coronavirus
Se ha incorporado a la investigación si los efectos no específicos observados con la vacunación de la tuberculosis con BCG se pueden extender a la protección frente al nuevo coronavirus [37].
 [38]El CSIC español trabaja en el desarrollo de vacunas frente a los coronavirus
[38]El CSIC español trabaja en el desarrollo de vacunas frente a los coronavirus
En el Centro Nacional de Biotecnología [39] (Centro Superior de Investigación Científica, CSIC, Ministerio de Ciencia e Innovación) se investiga en varias líneas relacionadas con el desarrollo de vacunas frente a la COVID-19. Por una parte el grupo de Mariano Esteban [40] trabaja en el uso de un vector vaccinia en el que se ha insertado el gen que expresa la proteína S (spike) del SARS-CoV-2, y, por otra, el grupo de Luis Enjuanes e Isabel Sola [41] lo hace con una variedad hiperatenuada del SARS-CoV-2.
 [42]
[42]
Ambos grupos han recibido financiación extra de la Unión Europea, el gobierno español y otras entidades para intensificar la investigación e integrarla en proyectos colaborativos con otros grupos de investigación a nivel internacional.
Consideraciones éticas
Aunque no hay aún ni siquiera aproximaciones a las opciones estratégicas en el uso de vacunas para el control de la COVID-19, sí se destaca que un uso universal de la vacunación frente al SARS-CoV-2 exigiría no sacrificar la seguridad por la urgencia del momento, de modo que no queda más que reconocer que el desarrollo de un producto con garantías exige tiempo, el tiempo necesario (Nature. 2020;579:321 [43]; Nature Biotech, 20 de marzo [44]).
Algunas alternativas para acelerar el desarrollo de una vacuna en este caso, como la exposición intencional de voluntarios al virus, despierta gran controversia (Nature. 2020;580:17 [45] y su traducción al español [46]; J Infect Dis. 2020, 31 de marzo [47]). Uno de los objetivos de la investigación y uso de vacunas en pandemias, sin duda debe ser el de conseguir la confianza de la población, desechando atajos de dudoso resultado (Nature Med. 2020;26:301 [48]).
-oOo-
- Recopilación de investigaciones en marcha con el objetivo de desarrollar vacunas frente al nuevo coronavirus. El Confidencial, 1 de abril de 2020 [50].
- OMS. Nuevo coronavirus y COVID-19 [51].
- Ministerio de Sanidad. Información actualizada [49].
- CEPI. Developing Covid-19 Vaccines at Pandemic Speed. NEJM. 2020, 30 de marzo [52].
- A. Galocha, N. Domínguez. Así infecta el coronavirus [25]. El País, 11 de marzo de 2020.
- Otras noticias anteriores sobre el coronavirus [53] en esta web.
- Otras noticias anteriores sobre emergencias globales [54] en esta web.
- Research and Development on Therapeutic Agents and Vaccines for COVID-19 and Related Human Coronavirus Diseases. ACS Cent Sci. 2020;6(3):315-31 [55].
- International Federation of Pharmaceutical Manufacturers & Associations (IFPMA [56]). Backgrounder – COVID-19 [57], 27 de marzo de 2020.

